Презентація на тему «Вищі карбонові кислоти» (варіант 2)
Вищі карбонові кислоти
C17H33COOH олеїнова
насичені
ненасичені
C15H31COOH пальмітинова
C17H35COOH стеаринова
C17H33COOH олеїнова
Вищі карбонові кислоти раніше добували тільки з рослинних і тваринних жирів, тому їх ще називають
Жирними кислотами
Пальмітинова кислота
Пальмітинова кислота -найбільш поширена в природі одноосновна насичена карбонова кислота.
безбарвні кристали; t пл 63,1°, t кіп351,5° ; нерозчинна у воді, помірно розчинна в спирті, бензолі, ацетоні.
Фізичні та хімічні властивості
Застосування
Пальмітинову кислоту використовують у виробництві стеарину, напалму, миючих і косметичних засобів, мастил.
Знаходження в природі
Пальмітинова кислота входить до складу гліцеридів більшості тваринних жирів і рослинних олій, наприклад, коров'яче масло містить 25%, свиняче сало - 30%)
C15H31COOH

Стеаринова кислота
Стеаринова кислота — одноосновна карбонова кислота аліфатичного ряду. Назва походить від грецького слова stéar що означає сало.
Була відкрита у свинячому салі в 1816 році французьким хіміком Шеврелем.
Фізичні та хімічні властивості
Білі кристали, нерозчинні у воді і розчинні в діетиловому ефірі. t пл 69,6 °C , t кіп 383 °C;
Застосування
Стеаринова кислота широко застосовується у хімічній, нафтохімічній, паперової, гумової та інших галузях промисловості. Її застосовують для одержання спиртів. Стеаринова кислота використовується у харчовій промисловості при виготовленні маргаринів, при додаванні жирів у тісто, як кремова основа випічки.
Синтез в організмі
C17H35COOH
Синтезується в організмі з пальмітинової кислоти під дією ферментів - елонгаз, що відповідають за подовження алифатической ланцюга жирних кислот.
олеїнова кислота
Безбарвна в'язка рідина, tпл 13,4 °C,tкип 286 °C. Окислюється перманганатом калія з розщеплюванням подвійного зв'язку,
Властивості
Знаходження в природі
Міститься в багатьох тваринних жирах у вигляді складних ефірів — гліцеридів: яловичому жирі (41-42%), в свинячому (37-44%), а також міститься в багатьох рослинних оліях: масло лісового горіха (70-84%), масло папайї (79%)
Застосування
Олеїнова кислота і її ефіри застосовують для отримання лакофарбних матеріалів. У промисловості олеїнову кислоту широко використовують для одержання натрієвої солі — основного компонента багатьох видів мила. Її фармацевтиці її застосовують в якості наповнювача, а у виготовленні різних аерозолів вона використовується як емульсіфікатор і розчинник.
Олеїнова кислота —міститься у багатьох продуктах рослинного і тваринного походження. Вона відноситься до жирних кислот омега-9 і вважається одним з найбільш корисних для здоров'я джерел жиру в дієті. Її часто використовують як замінник тваринного жиру, який переважно складається з насичених жирів.
C17H33COOH
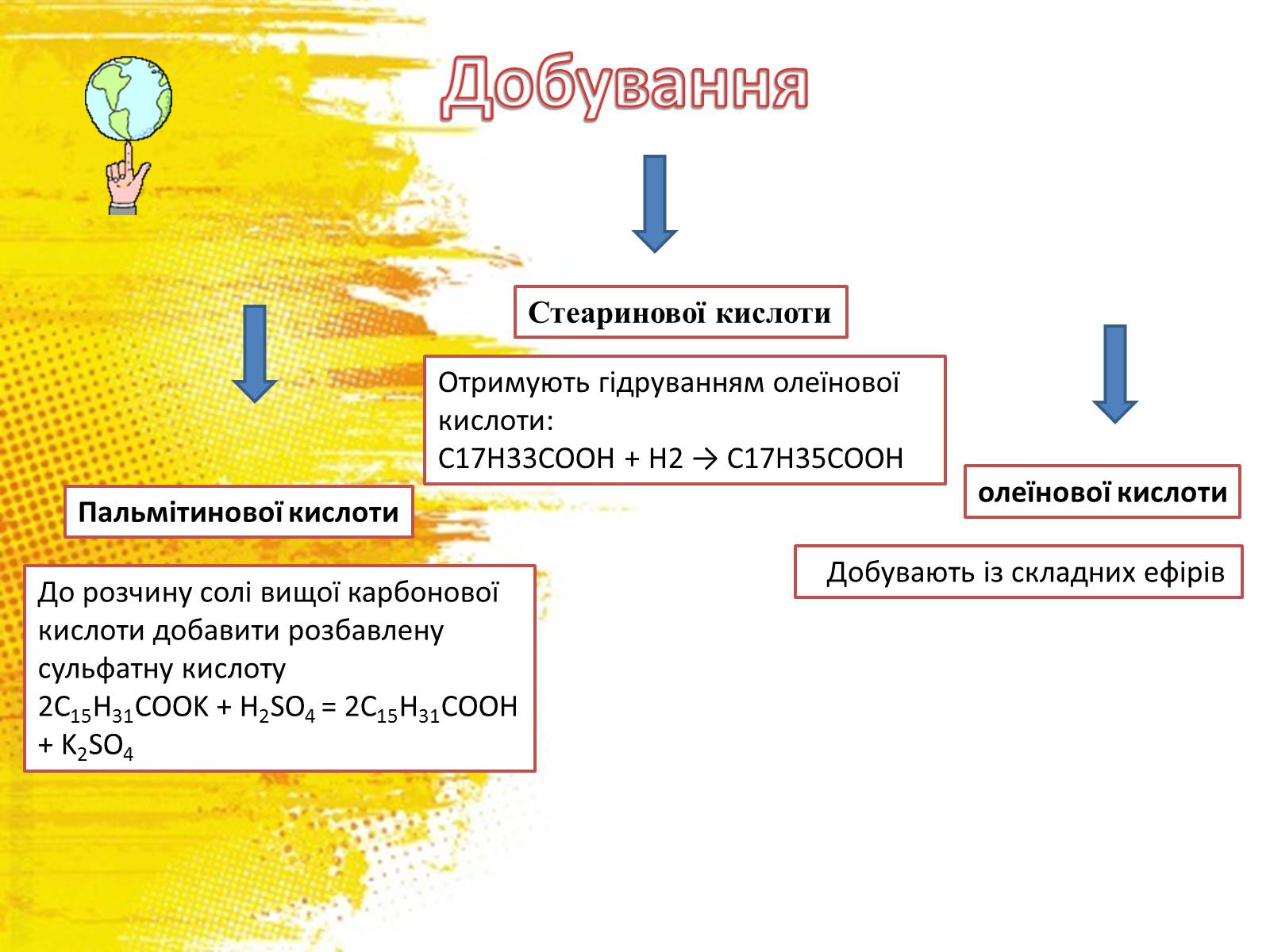
Добування
Пальмітинової кислоти
Стеаринової кислоти
олеїнової кислоти
Отримують гідруванням олеїнової кислоти:
C17H33COOH + H2 → C17H35COOH
До розчину солі вищої карбонової кислоти добавити розбавлену сульфатну кислоту
2С15H31COOK + H2SO4 = 2C15H31COOH + K2SО4
Добувають із складних ефірів

Хімічні властивості
Реагують із лугами:
C17H35COOH + NaOH= C17H35COONa+H2O
Якщо до розчину солі вищої карбонової кислоти добавити розбавлену сульфатну кислоту то відбудеться реакція обміну:
2С15H31COOK + H2SO4 = 2C15H31COOH + K2SО4
Олеїнова кислота є ненасиченою сполукою і тому виступає в реакції приєднання з галогенами,галогеноводнями, воднем
C17H33COOH + H2 = C17H35COOH