Презентація на тему «Окисно-відновні реакції»

Окисно-відновні реакції, їхнє значення.
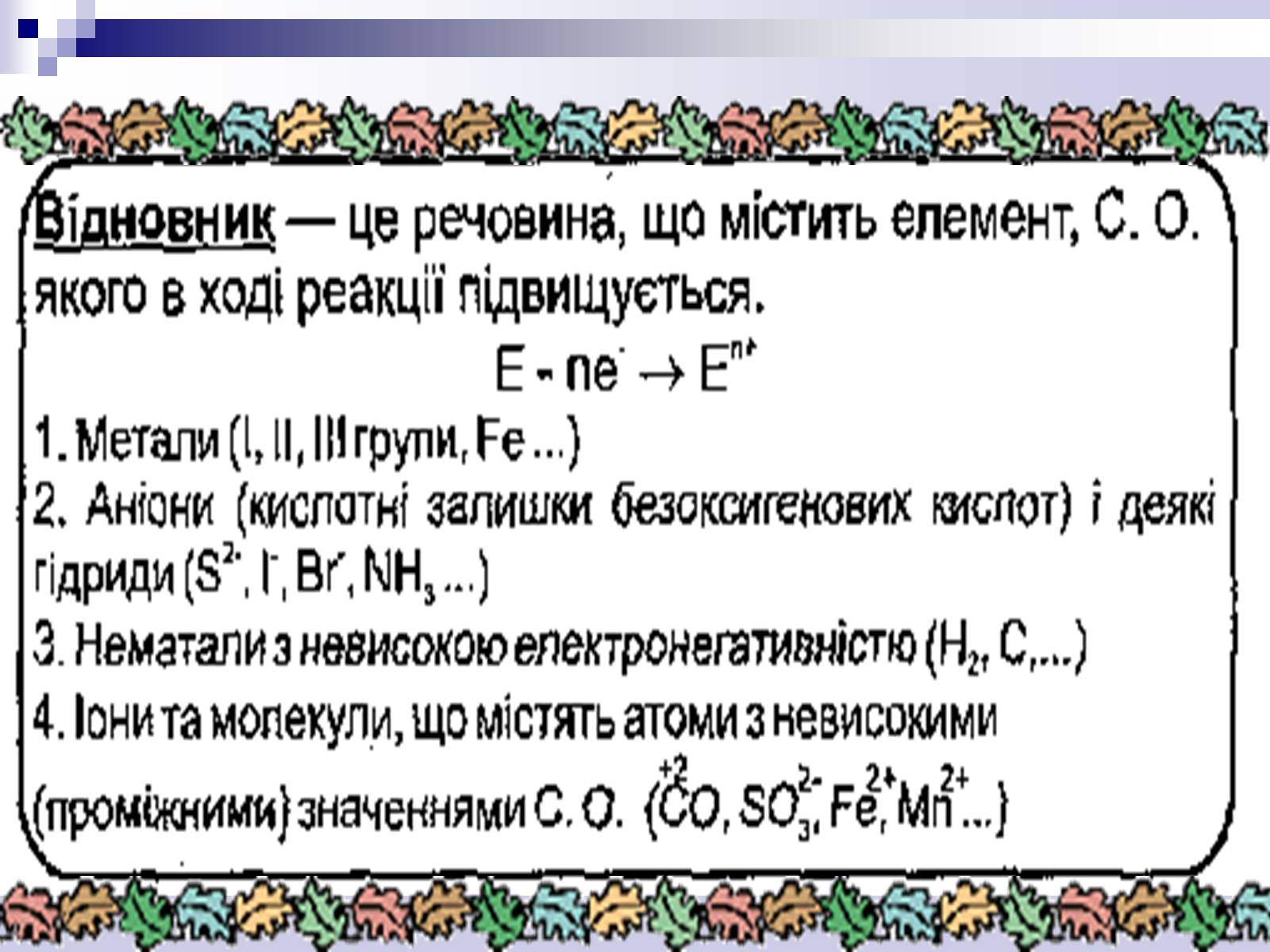
Процеси окиснення, відновлення, окисники, відновники.

Мета.
Сформувати знання про окисно-відновні реакції.
Сформувати поняття про процеси окиснення, відновлення.
Навчити розрізняти які з речовин є окисниками, а які відновниками

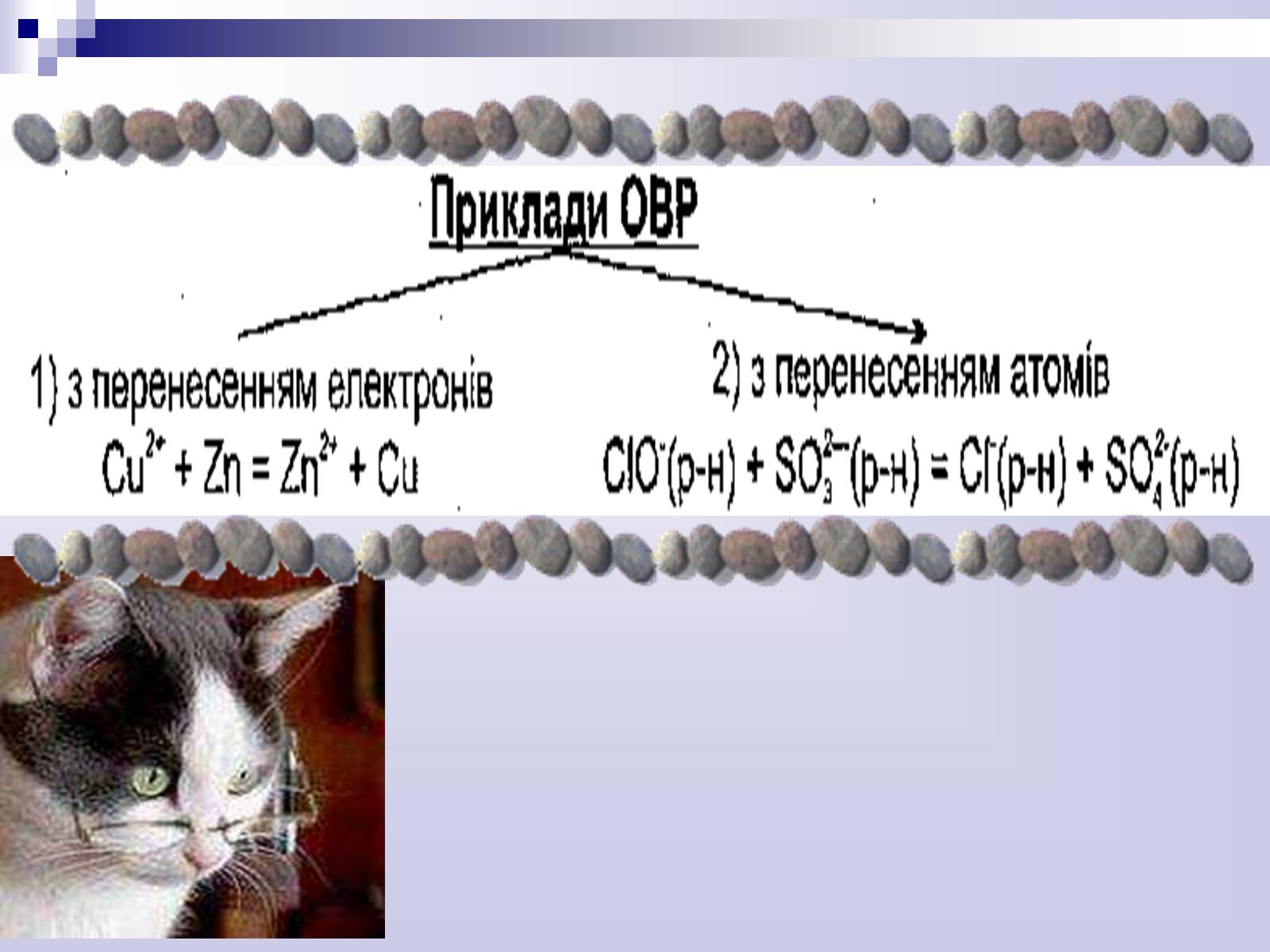
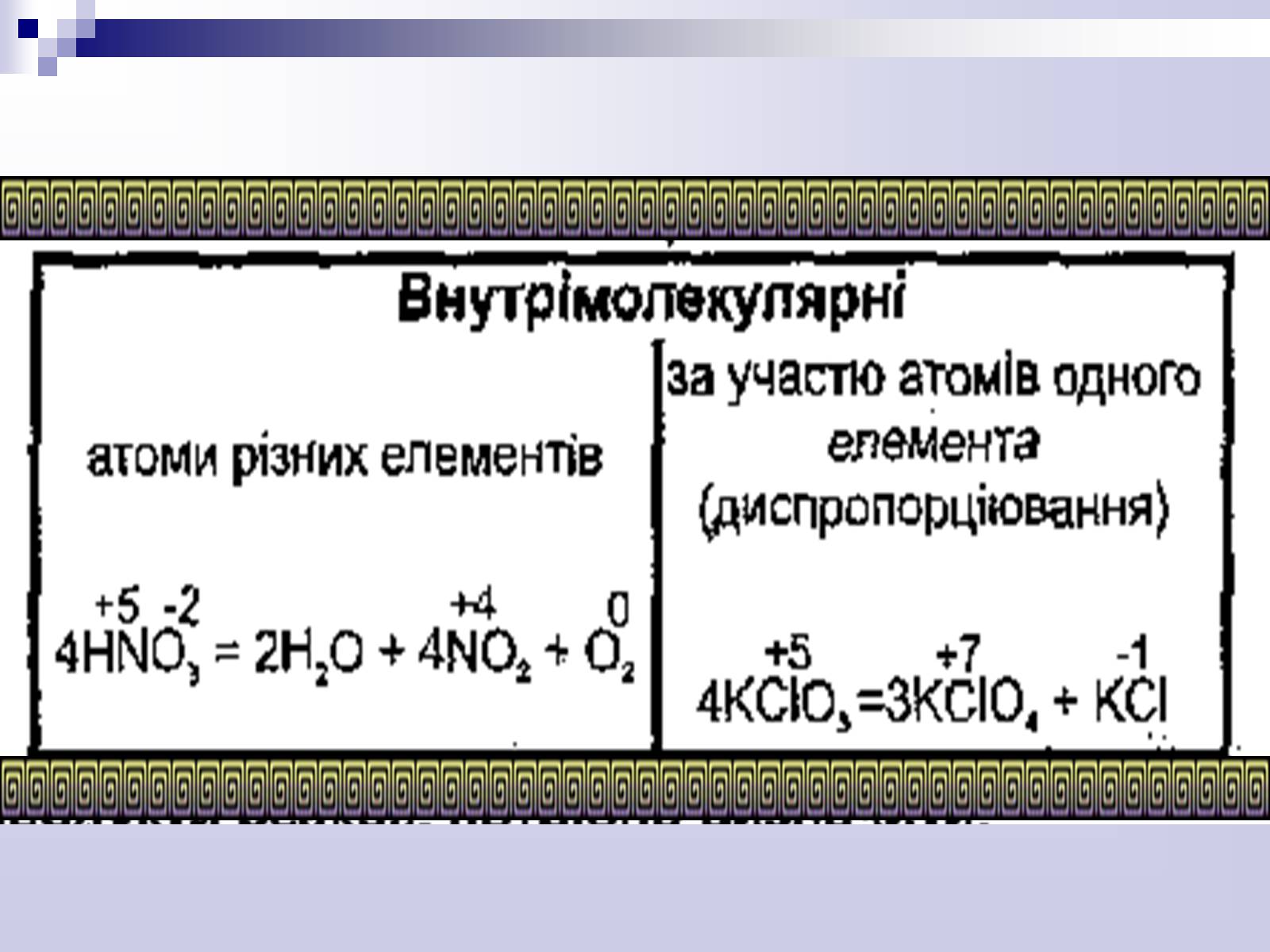
Окисно - відновними реакціями (ОВР)
називають процеси, які здійснюються при переході електронів або атомів від одних частинок до інших, що призводить до зміни ступенів окиснення атомів елементів, які беруть участь у реакції.
Окисно - відновними реакціями (ОВР)
називають процеси, які здійснюються при переході електронів або атомів від одних частинок до інших, що призводить до зміни ступенів окиснення атомів елементів, які беруть участь у реакції.
Окисно - відновними реакціями (ОВР)
називають процеси, які здійснюються при переході електронів або атомів від одних частинок до інших, що призводить до зміни ступенів окиснення атомів елементів, які беруть участь у реакції.

Окисно - відновними реакціями (ОВР)
називають процеси, які здійснюються при переході електронів або атомів від одних частинок до інших, що призводить до зміни ступенів окиснення атомів елементів, які беруть участь у реакції.

Окисно - відновними реакціями (ОВР)
називають процеси, які здійснюються при переході електронів або атомів від одних частинок до інших, що призводить до зміни ступенів окиснення атомів елементів, які беруть участь у реакції.
Окисно - відновними реакціями (ОВР)
називають процеси, які здійснюються при переході електронів або атомів від одних частинок до інших, що призводить до зміни ступенів окиснення атомів елементів, які беруть участь у реакції.

Окисно - відновними реакціями (ОВР)
називають процеси, які здійснюються при переході електронів або атомів від одних частинок до інших, що призводить до зміни ступенів окиснення атомів елементів, які беруть участь у реакції.

Окисно - відновними реакціями (ОВР)
називають процеси, які здійснюються при переході електронів або атомів від одних частинок до інших, що призводить до зміни ступенів окиснення атомів елементів, які беруть участь у реакції.
Окисно - відновними реакціями (ОВР)
називають процеси, які здійснюються при переході електронів або атомів від одних частинок до інших, що призводить до зміни ступенів окиснення атомів елементів, які беруть участь у реакції.

Окисно - відновними реакціями (ОВР)
називають процеси, які здійснюються при переході електронів або атомів від одних частинок до інших, що призводить до зміни ступенів окиснення атомів елементів, які беруть участь у реакції.

Окисно - відновними реакціями (ОВР)
називають процеси, які здійснюються при переході електронів або атомів від одних частинок до інших, що призводить до зміни ступенів окиснення атомів елементів, які беруть участь у реакції.

Окисно - відновними реакціями (ОВР)
називають процеси, які здійснюються при переході електронів або атомів від одних частинок до інших, що призводить до зміни ступенів окиснення атомів елементів, які беруть участь у реакції.

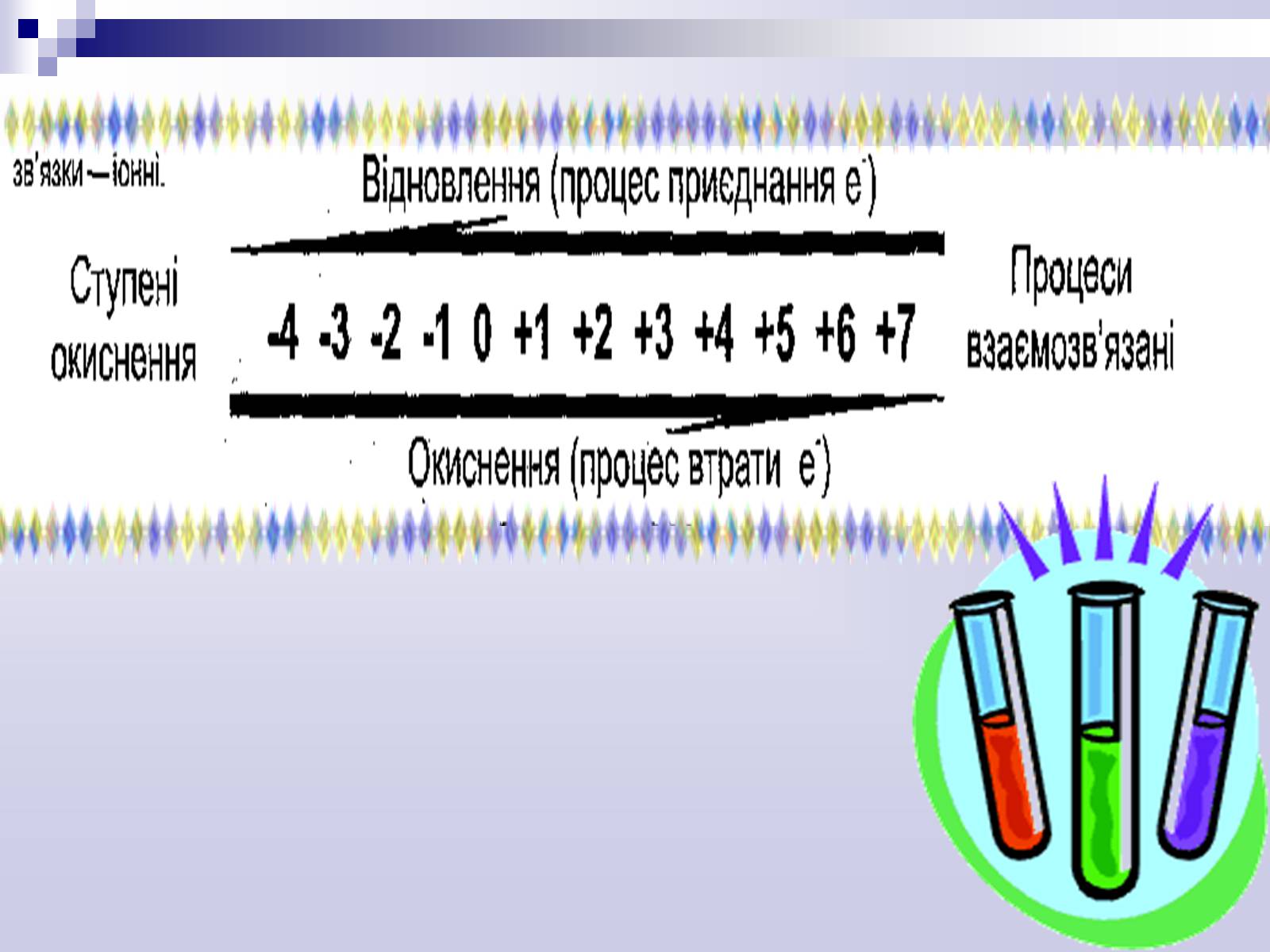
Ступінь окиснення (С.О.) — умовна величина, що показує заряд того чи іншого елемента в сполуці .
1. Ступінь окиснення элемента в прості речовині = 0.
H20 ; O20 ; F20 ; Cl20 ; Ca0.
2. Ступінь окиснення деяких элементів в сполуці:
- H+1
- О-2
Ступінь окиснення металу співпадає з його валентністю :
Na+1 ; K+1 ; Ca+2 ; Mg+2 ; Ba+2 ; Al+3 .
3. Сума ступенів окисненя элементів в сполуці, з врахуванням коэфіціентів= 0.

Низша с.о.= 8 – № групи
Нульова с.о.в простих речовинах.
Позитивна с.о.= номеру групи.

С.о. оксигену в оксиді =-2.
С.о. водню в сполучені з неметалами=+1.
С.о. металів 1 групи гол.підгр. =+1.
С.о. металів 2 гр. гол. підгр. =+2.
С.о. алюмінію =+3.

H2O
-2
+1
H2SO4
+1
-2
+6
Правила складання хімічної формули:
1. На першому місці знаходиться элемент с позитивним ступенем окиснення.
2. На останьому місці знаходиться элемент с негативним ступенем окиснення
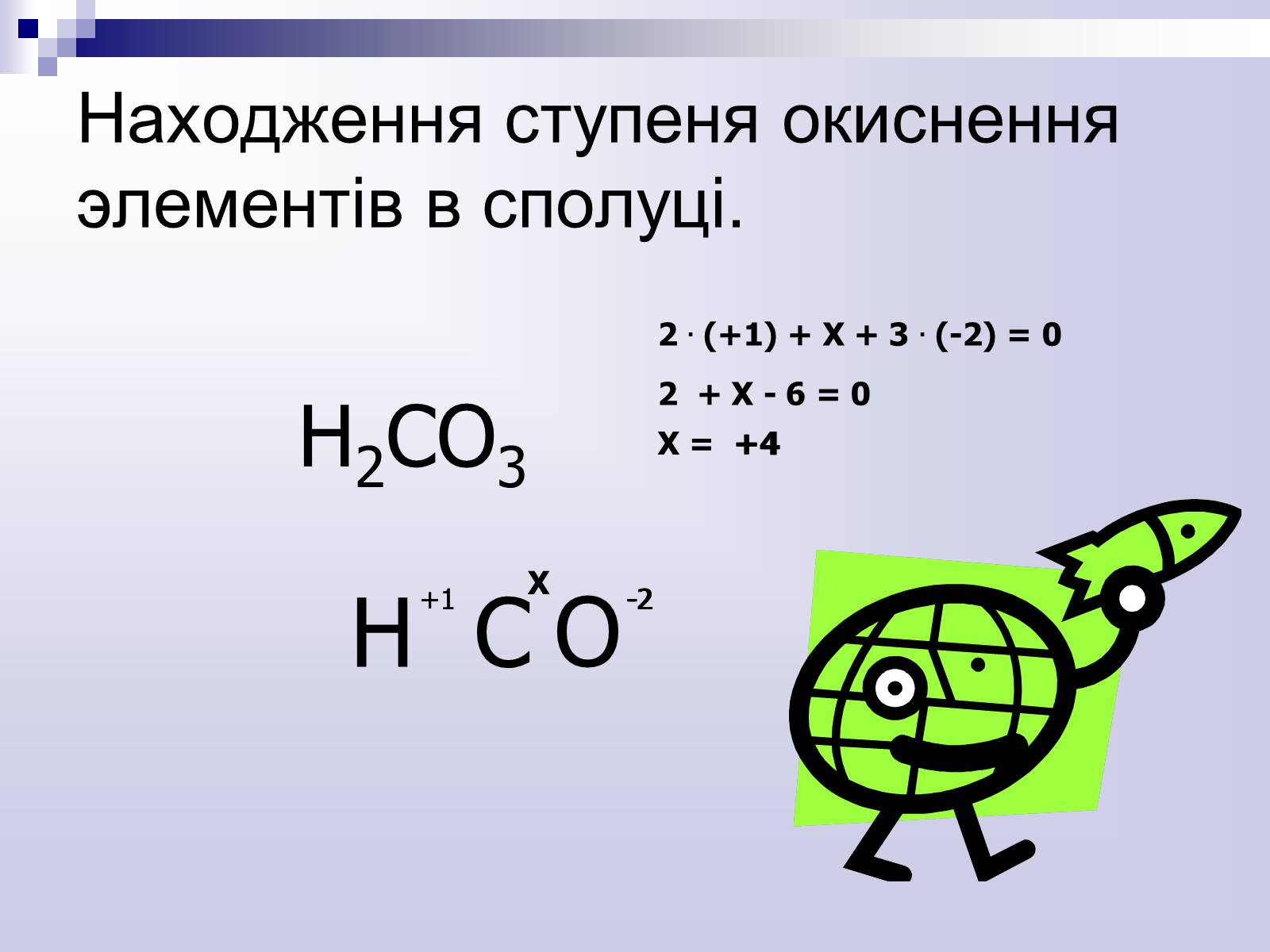
H2СO3
H С
+1
О
-2
+1
-2
Х
2 . (+1) + Х + 3 . (-2) = 0
2 + Х - 6 = 0
Х = +4
+4
Находження ступеня окиснення элементів в сполуці.

Бинари –
Оксиди
Гідриди
Хлориди
Сульфіди
Нітриди
Фосфіди
Карбіди
Силіциди
-2
O
-1
H
-1
Cl
-2
S
-3
N
-3
P
-4
C
-4
Si
Це речовини що складаються з двох элементів.
+2 -2 +4 -2 +1 -2 +4 -2
CaO, SiO2, H2O, CO2,
+1 -1 +2 -1
NaH , CaH2 ,
+1 -1 +1 -1 +3 -1
HCl, NaCl, FeCl3,
+1 -2 +1 -2 +2 -2
H2S, Na2S, FeS,
+1 -3 +2 -3 +3 -3
H3N, Ca3N2, AlN,
+1 -3 +2 -3 +3 -3
H3P, Ca3P2 AlP,
+1 -4 +2 -4 +3 -4
H4C, Ca 2C, Al4C3,
+2 -4 +3 -4
Mg2Si, Al4Si3.
+1 -3 +2 -3 +3 -3
H3P, Ca3P2 AlP,
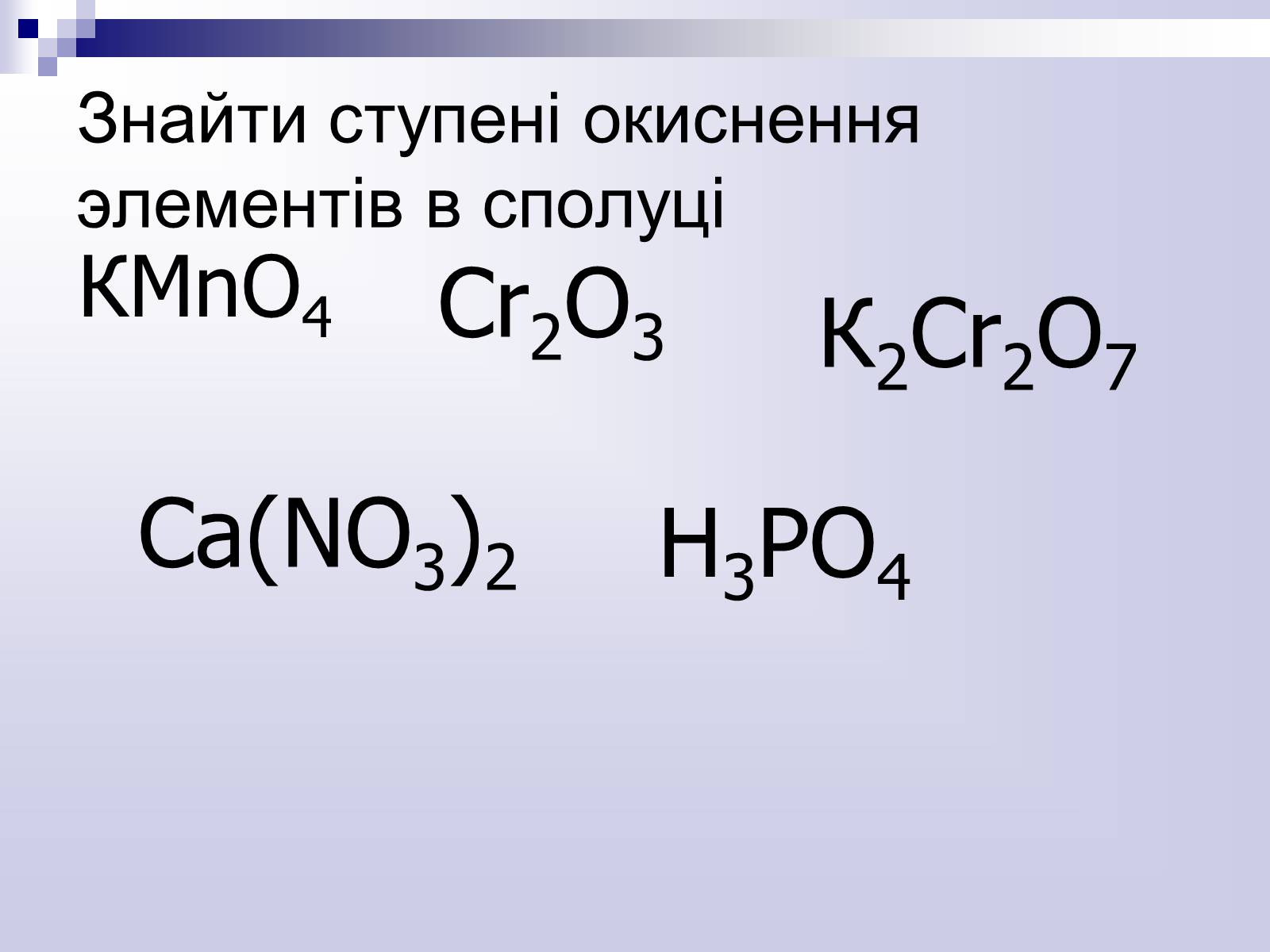
КMnO4
Cr2O3
H3PO4
К2Cr2O7
Ca(NO3)2
Знайти ступені окиснення элементів в сполуці