Презентація на тему «Оксиди» (варіант 1)

Оксиди, їх склад, назви.

Мета.
На прикладі найпростіших за складом і будовою хімічних сполук почати вивчення основних класів неорганічних сполук. Закріпити навички складання формул оксидів та називати їх. Поглибити знання про реакції сполучення, їх роль в утворенні оксидів.

БІНАРНІ СПОЛУКИ
Оксиди – це складні речовини, утворені двома елементами, одним з яких обов'язково є Оксиген.

За складом оксиди поділяють на оксиди металів і оксиди неметалів.
Оксиди дуже поширені в природі, оскільки кисень є однією з найактивніших речовин.
Найважливішим природним оксидом є вода – джерело життя на Землі, сировина для промисловості, джерело енергії, чинник, що визначає погоду, клімат Землі.
метали і неметали з киснем утворюють оксиди.

Загальна формула оксидів
Еn Оm
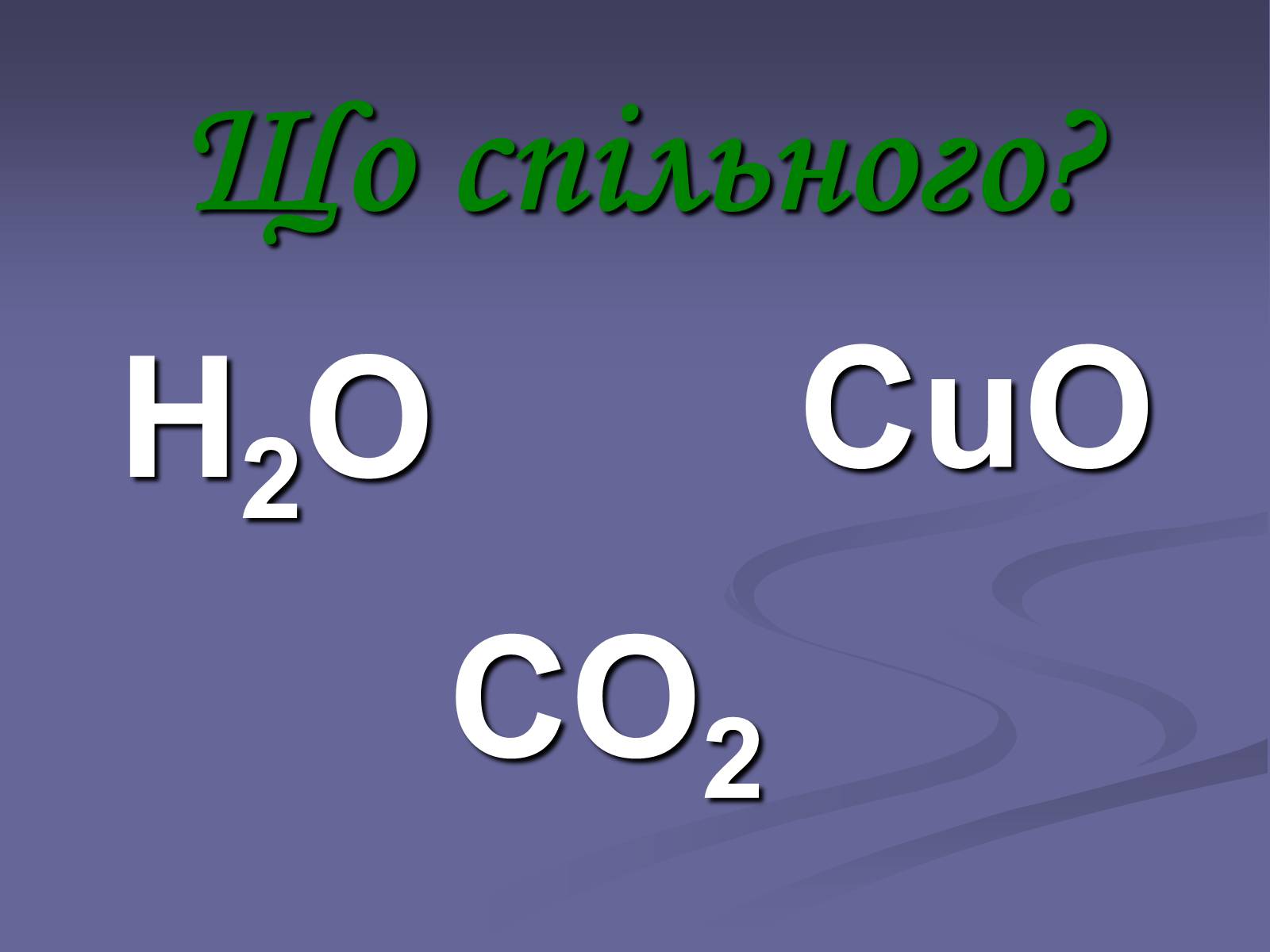
Н2О
CO2
CuO
Що спільного?
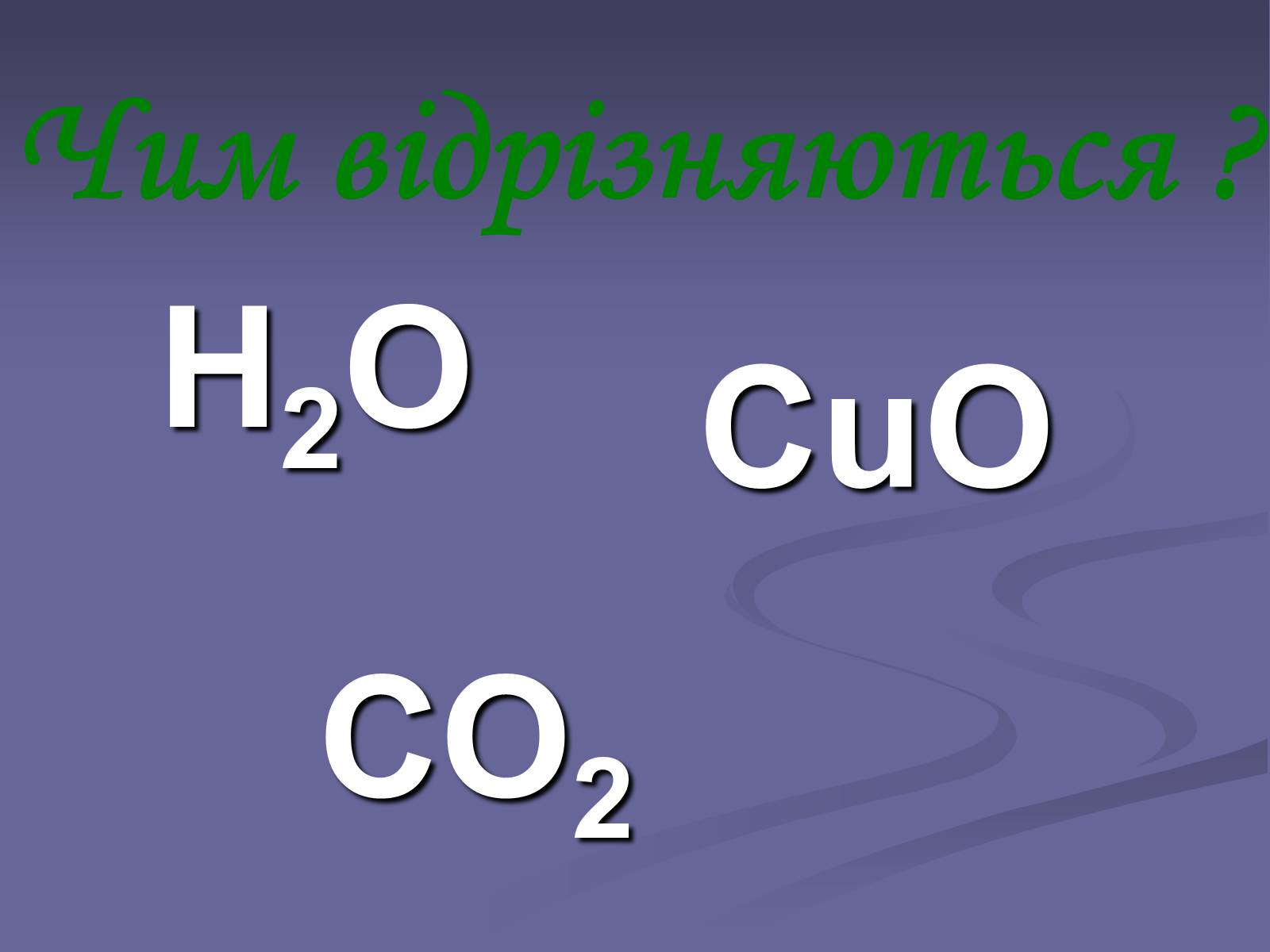
Н2О
CO2
CuO
Чим відрізняються ?
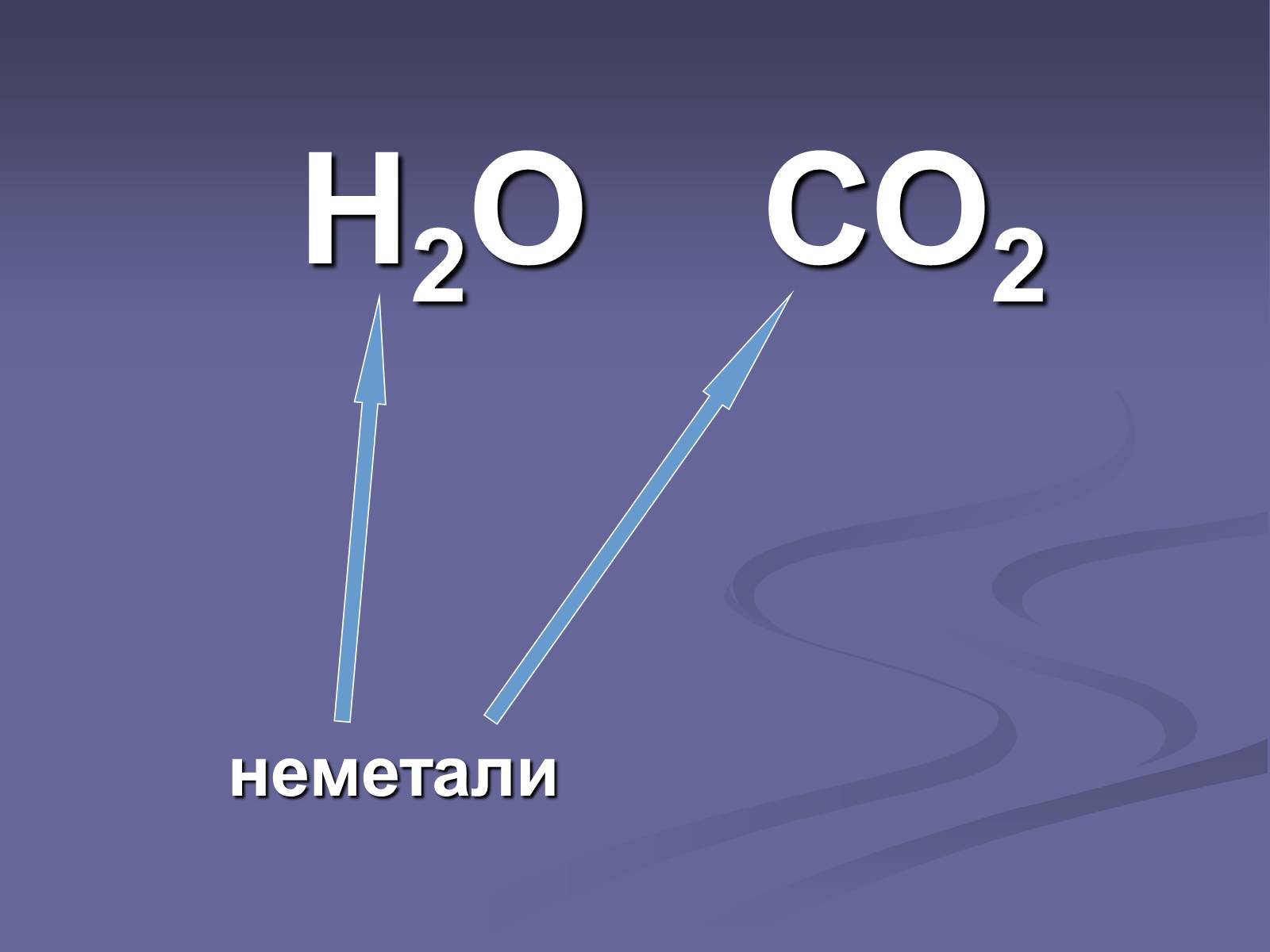
Н2О СО2
неметали
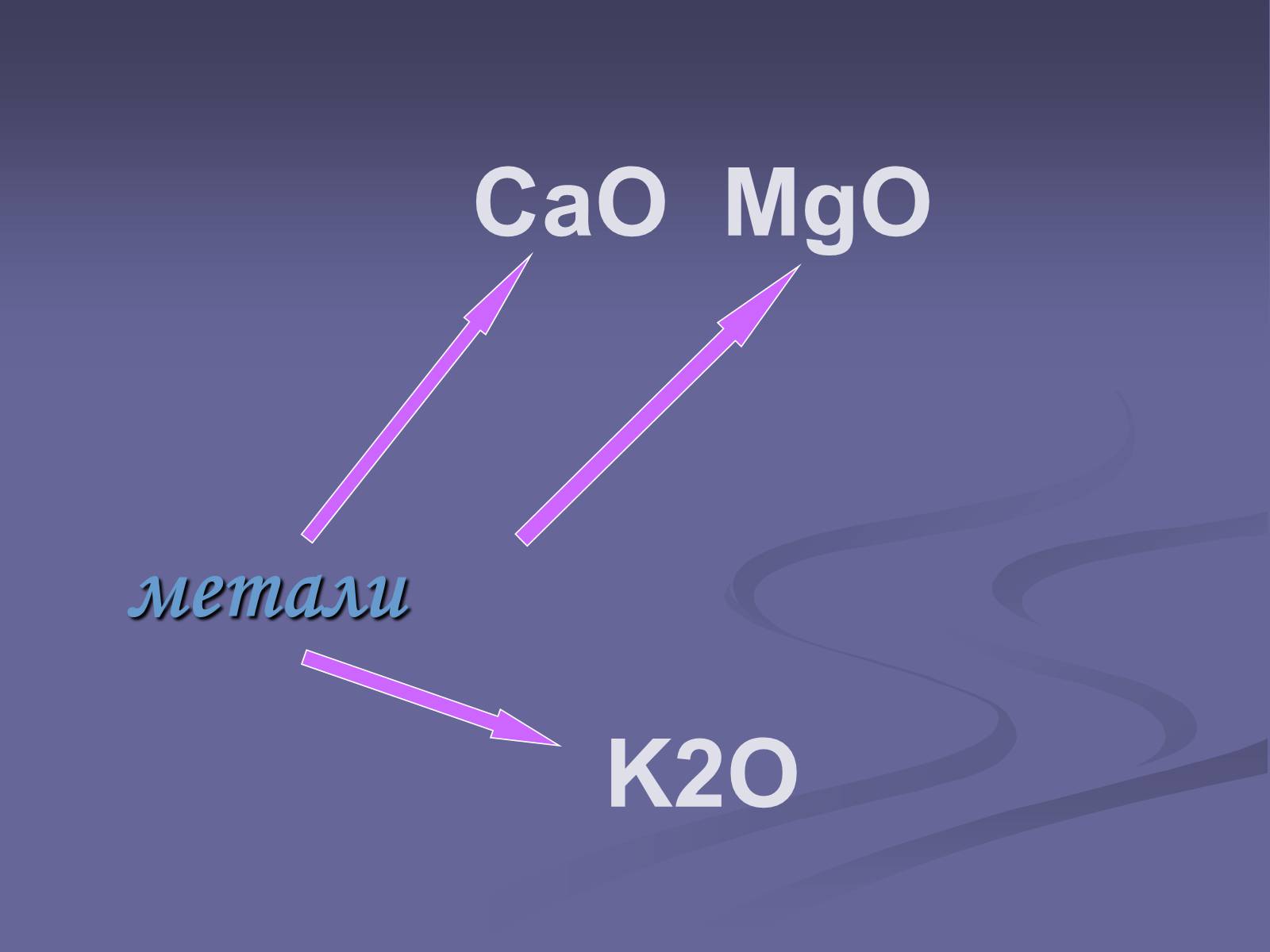
СаО MgO
K2O
метали

Амфотерність
Амфотерність –здатність елементів виявляти подвійні властивості.
Be Al Fe Zn
Примеры:
Al2O3 Fe2O3
ZnO

Утворення назви оксидів
Назва металу чи неметалу
+
Валентність елемента
+
Слово оксид

ВОДАtгідроген оксид

Вуглекислий газ Карбон (IV)оксид

Бурий газНітроген (IV) оксид

КварцСиліцій(IV)оксид

Природные соединения оксида алюминия:
боксит, корунд, рубин, обработанные сапфиры
Алюміній (ІІІ)оксид

Червоний та бурий залізнякФерум(ІІІ)оксид

Меркурій(ІІ) оксид

Купрум оксид

Купрум(ІІ)оксид

ПіролюзитМанган (IV)оксид

Хром(ІІІ)оксид

Хром (VI) оксид

Плюмбум(ІІ)оксид

СИЛІЦІЙ ОКСИД

Ай Плиний Старший, знаменитый естествоиспытатель и историк античного мира живший в I веке, описывает такой случай.
Однажды, в очень давние времена, Финикийские купцы везли по Средиземному морю груз добытой в Африке природной соды. По утру, разгребая золу, купцы обнаружили чудесный слиток, который был твёрд, как камень, горел огнём на солнце и был чист и прозрачен, как вода.
Это было стекло!
Г
химический
состав
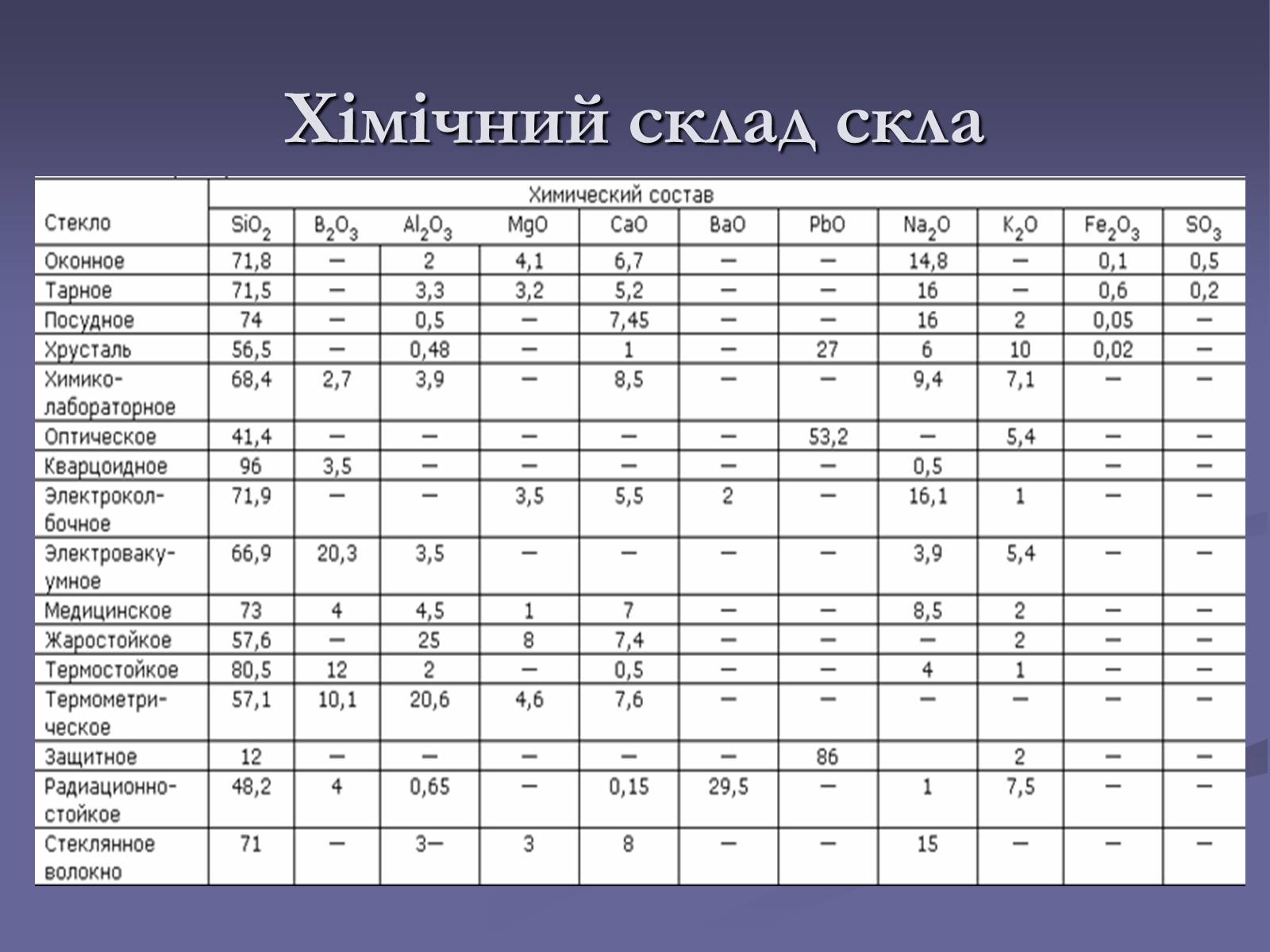
Хімічний склад скла

Для получения стекла составляют шихту- смесь соды Na2CO3 (иногда сульфата натрия с углем), известняка CaCO3, кварцевого песка, содержащего 97-99,8% SiO2,
и различных добавок. Шихту
помещают в специальные печи и сплавляют, постепенно повышая температуру до 1460-1500 градусов.

В процессе варки стекла происходят реакции:
Na2CO3+SiO2=Na2SiO3+CO2
CaCO3+SiO2=CaSiO3+CO2
Na2SiO3+CaSiO3+4SiO2=Na2O+CaO+6SiO2

Стекло имеет различные добавки. Роль добавок велика, они предают стеклу особые свойства. Так, MgO повышает химическую устойчивость и механическую прочность стекла; Al2O3 увеличивает термическую и химическую стойкость, твёрдость и прочность, улучшает однородность стекла, B2O3 увеличивает термостойкость стекла и улучшает его оптические свойства. Для получения специальных оптических стёкол в шихту диоксид германия GeO2 и диоксид титана TiO2. Специальные добавки обеспечивают окраску стекла: Mn2O3 придаёт стеклу фиолетовую окраску, CoO- синюю, Cr2O3 или Fe3O4- зелёную, CuO- голубую, CdS- жёлтую.

Стекло имеет различные добавки. Роль добавок велика, они предают стеклу особые свойства. Так, MgO повышает химическую устойчивость и механическую прочность стекла; Al2O3 увеличивает термическую и химическую стойкость, твёрдость и прочность, улучшает однородность стекла, B2O3 увеличивает термостойкость стекла и улучшает его оптические свойства. Для получения специальных оптических стёкол в шихту диоксид германия GeO2 и диоксид титана TiO2. Специальные добавки обеспечивают окраску стекла: Mn2O3 придаёт стеклу фиолетовую окраску, CoO- синюю, Cr2O3 или Fe3O4- зелёную, CuO- голубую, CdS- жёлтую.

РОЗМИНКА

«Первое начало и сущность всего – …»tФалес из Милета (VI в. до н.э.)
Вгадай що знаходиться в перші шкатулці,?

Вода
Вода – це найдивовижніша, найпоширеніша і найнеобхідніша речовина на нашій планеті.
Вода – джерело життя на Землі, сировина для промисловості, джерело енергії, чинник, що визначає погоду, клімат Землі. Три чверті земної поверхні вкрито водою, що утворює океани, моря, ріки та озера.

Вода в природі

Вода в природі

Складіть асоціативний ряд до слова «вода»

Акваріум

Акваторія

Акваланг

Акварель

Газ, необхідний
рослинам для
фотосинтеза
А що в ці шкатулці ?

Вуглекислий газ
До складу повітря входить карбон(IV) оксид СО2 (вуглекислий газ), об'ємна частка якого в повітрі становить 0,3 %.

«…На рукомойнике моем
позеленела медь,
Но так играет луч на нем,
что весело глядеть…»
А. Ахматова
А що в останій шкатулці ?

CuO