Презентація на тему «Маса та розміри атомів і молекул. Кількість речовини»

Маса та розміри атомів і молекул. Кількість речовини.

Атом. Молекула.

Атом. Молекула

Число молекул речовини в будь-якому тілі називається кількістю речовини і позначається ν.
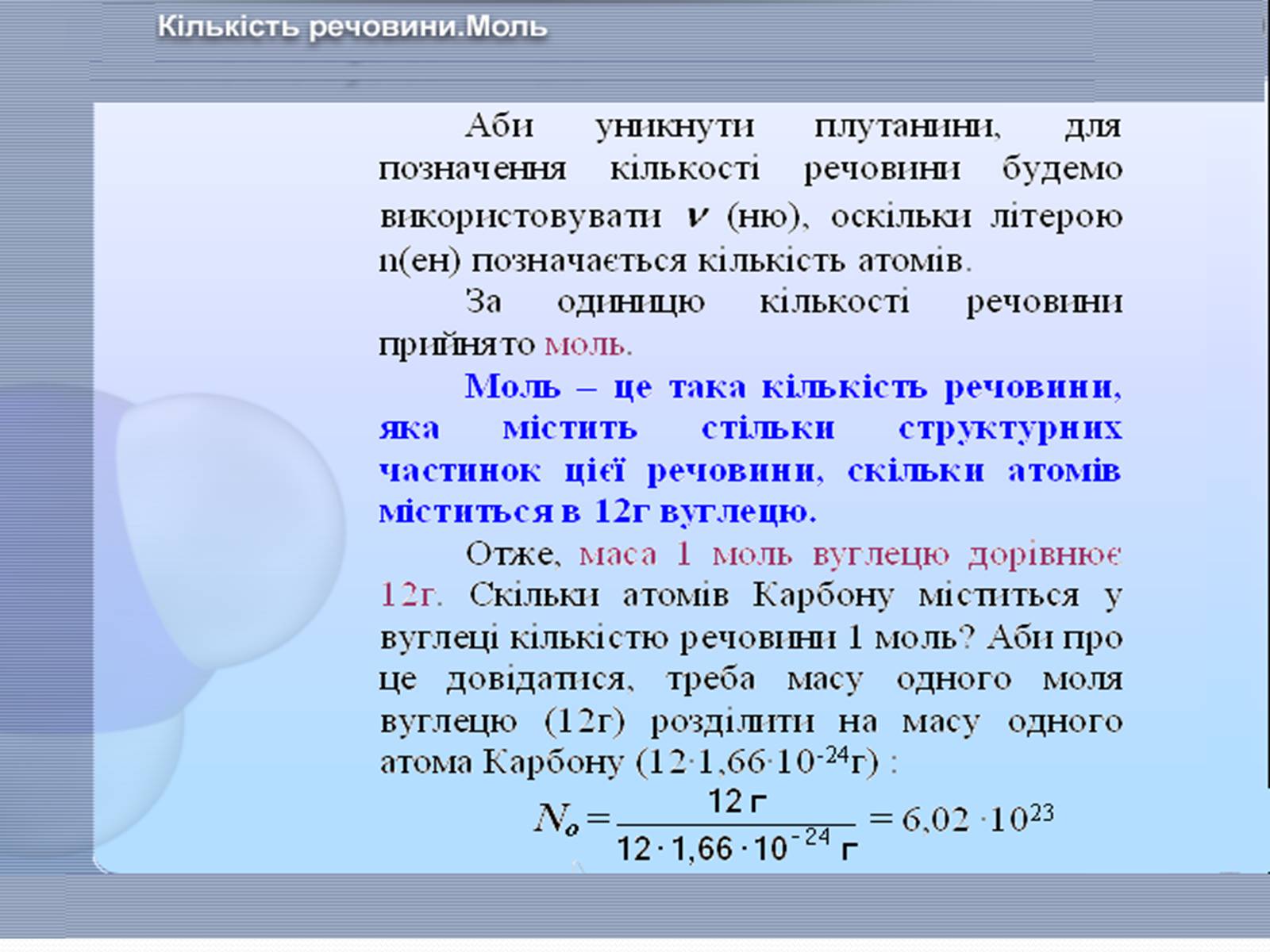
Кількість речовини

Моль довільної речовини містить однакову кількість молекул (атомів, іонів). Цю кількість називають числом Авогадро на честь італійського вченого ХІХ ст. Амадео Авогадро:
Число Авогадро

Амедео Авогадро
Амедео Авогадро (граф итал. Lorenzo Romano Amedeo Carlo Avogadro di Quaregna e Cerreto; 9 августа 1776, Турин— 9 июля 1856, там же) — італійський учений, фізик и хімік.
Імпульсом до активних експерементів в галузі хімії для Авогадро стало відкриття Гей-Люссаком газових законів.
Авогадро в своїх працях користувався поняттям молекула газу, яке, в тогочасній терминології, включало в себе одночасно поняття атом и молекула.[
Амедео Авогадро
Амедео Авогадро (граф итал. Lorenzo Romano Amedeo Carlo Avogadro di Quaregna e Cerreto; 9 августа 1776, Турин— 9 июля 1856, там же) — італійський учений, фізик и хімік.
Імпульсом до активних експерементів в галузі хімії для Авогадро стало відкриття Гей-Люссаком газових законів.
Авогадро в своїх працях користувався поняттям молекула газу, яке, в тогочасній терминології, включало в себе одночасно поняття атом и молекула.[

Амедео Авогадро
Амедео Авогадро (граф итал. Lorenzo Romano Amedeo Carlo Avogadro di Quaregna e Cerreto; 9 августа 1776, Турин— 9 июля 1856, там же) — італійський учений, фізик и хімік.
Імпульсом до активних експерементів в галузі хімії для Авогадро стало відкриття Гей-Люссаком газових законів.
Авогадро в своїх працях користувався поняттям молекула газу, яке, в тогочасній терминології, включало в себе одночасно поняття атом и молекула.[

Амедео Авогадро
Амедео Авогадро (граф итал. Lorenzo Romano Amedeo Carlo Avogadro di Quaregna e Cerreto; 9 августа 1776, Турин— 9 июля 1856, там же) — італійський учений, фізик и хімік.
Імпульсом до активних експерементів в галузі хімії для Авогадро стало відкриття Гей-Люссаком газових законів.
Авогадро в своїх працях користувався поняттям молекула газу, яке, в тогочасній терминології, включало в себе одночасно поняття атом и молекула.[

m - маса тіла , M – молярна маса
Кількість речовини обчислюємо за формулою:

Кількість молекул обчислюємо: