Презентація на тему «Корозія металів» (варіант 2)

Корозія металів

Корозія - це руйнування металів і сплавів під впливом хімічної чи електрохімічної взаємодії з оточуючим середовищем.

Корозію металів та їх сплавів викликають такі компоненти зовнішнього середовища , як вода, кисень, оксиди карбону і сульфуру , водні розчини солей.
Більш активний метал при електрохімічній корозії руйнується, переходячи в воду, тим самим захищає менш активний від руйнування.

Небезпека корозії
Може призвести до екологічних катастроф: потрапляння природного газу, нафти, небезпечних хімічних продуктів у навколишнє середовище.
Недопустима в авіаційному, нафтовому, атомному, хімічному машинобудуванні тощо.
Негативно впливає на здоров'я людини.

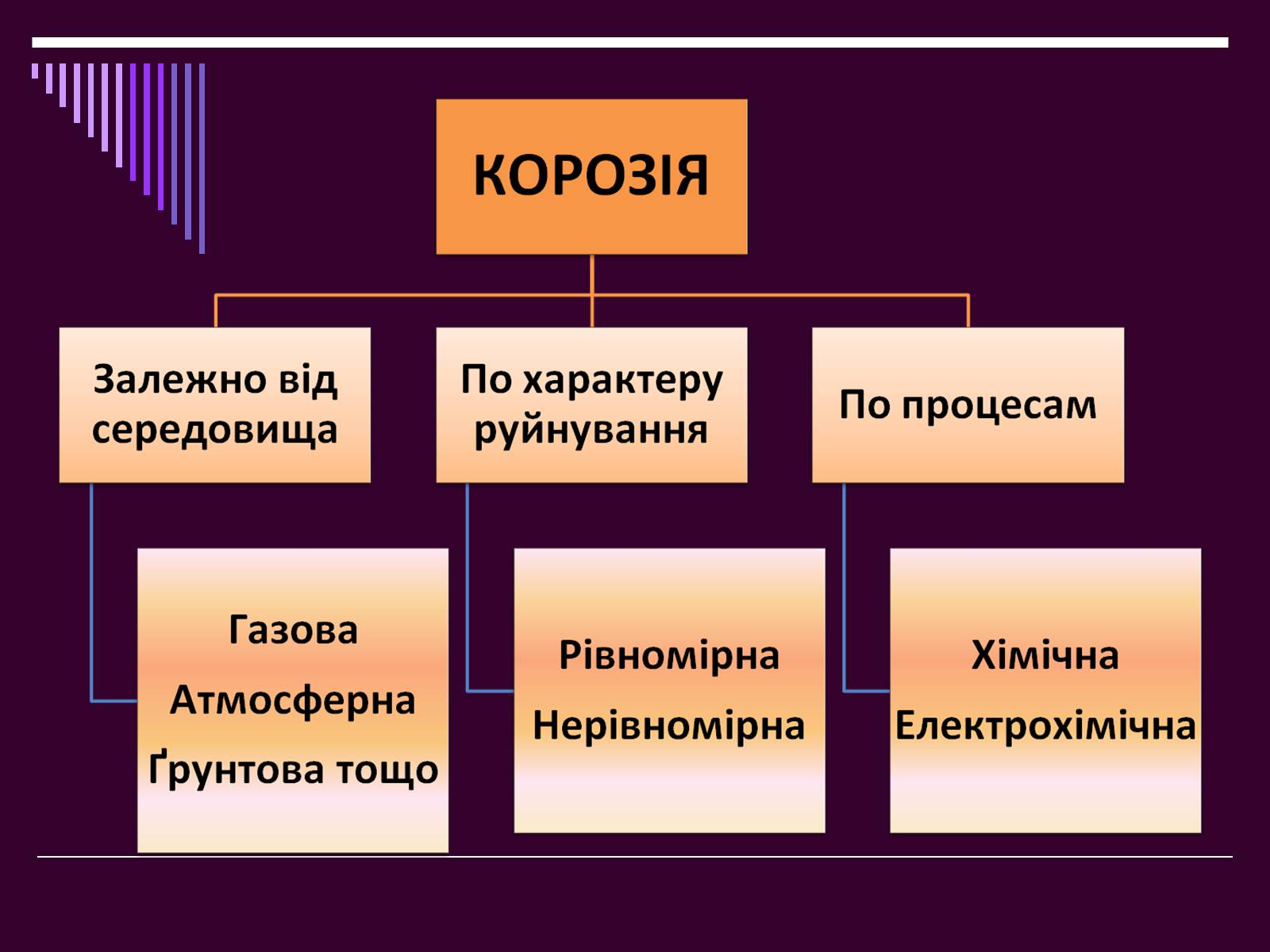
Корозія буває хімічна та електрохімічна
Хімічна корозіяХарактеризується хімічними процесами, які відбуваються між металом і агресивними речовинами оточуючого середовища.
Електрохімічна корозія
Руйнування металу супроводжується виникненням електричного струму у водному середовищі електроліта.

Що сприяє електрохімічній корозії:
Положення металів у ряду активності: чим далі один від одного вони розміщені, тим швидше відбувається корозія.
Чистота металу (домішки прискорюють корозію).
Нерівності поверхні, мікротріщини.
Висока температура і вологість.
Дія мікроорганізмів, грибів, лишайників.
Грунтові води, морська вода, розчини електролітів.

Усунути шкідливий вплив на металеві конструкції практично неможливо, тому корозія, на жаль, є вічним супутником металу. Швидкість «роз'їдання» залежить від умов, в яких виготовлено та експлуатується виріб. Але цьому процесу можна протистояти. Найбільш простий і доступний спосіб боротьби з корозією - застосування спеціальних фарб, що утворюють захисну плівку.
Шляхи захисту від корозії

Шляхи захисту від корозії
Покриття виробу іншими металами, стійкішими до корозії: позолота, хромування, цинкування тощо.
Створення нових антикорозійних сплавів.
Протекторний захист.

Для уповільнення корозії металевих виробів до електроліту вводять речовини, які інгібіторами, їх застосовують у тих випадках, коли метал необхідно захищати від роз'їдання кислотами. Вчені створили ряд інгібіторів, які при доданні до кислоти в сотні разів сповільнюють розчинення (корозію) металів.
Останнім часом розроблено леткі інгібітори. Ними просочують папір, яким обгортають металеві вироби.
Інгібітори широко застосовують при хімічному очищенні від накипу парових котлів, зніманні окалини з оброблених деталей, а також при зберіганні та перевезенні хлоридної кислоти у стальній тарі. До неорганічних інгібіторів належать нітрити, хромати, фосфати, силікати. Механізм дії інгібіторів є предметом дослідження багатьох науковців.