Презентація на тему «Карбон» (варіант 1)
Характеристика елемента та утворених ним сполук, кругообіг елемента в природі
Карбон

Періодична система хімічних елементів Д.І.Менделєєва
Періоди
1
2
3
4
5
6
7
Ряди
1
2
3
4
10
9
8
7
5
6
Групи елементів
I
II
VI
V
VII
III
IV
VIII
Характеристика
1.
Визнання Карбону хімічним елементом сталося у 1775 р., завдяки роботам А. Лавуазьє.
2.
У Періодичній системі знаходиться в 2 періоді, ІV група, головна підгрупа.
3.
У природі зустрічається як у вільному стані, так і у зв'язаному.
4.
Утворює кілька простих речовин: алмаз графіт, карбін, фулерени.
5.
Е=2,5; найнижчий ступінь окислення –4, найвищий ступінь окислення +4.
12
+6
C
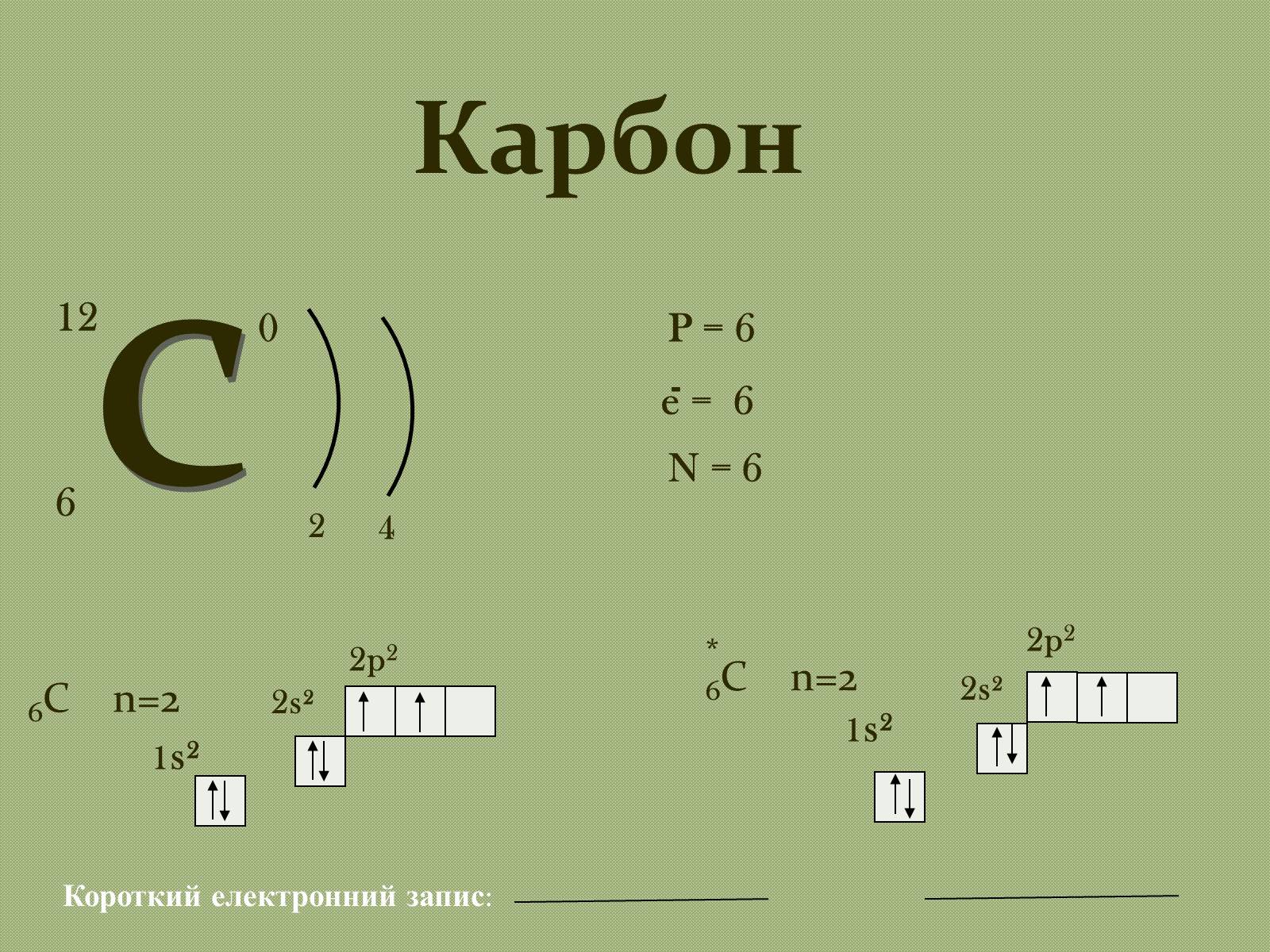
с
12
6
2
4
P = 6
e = 6
N = 6
-
Короткий електронний запис:
1s²
2p2
2s²
Карбон
6С n=2
1s²
2s²
2p2
6С n=2
*

Алотропні модифікації Карбону
Алмаз
Графіт
Фулерен

Хімічні властивості
Вуглець – найтугоплавкіша проста речовина. За звичайних умов вуглець малоактивний, при нагріванні вступає в реакції з металами і воднем, виявляючи окислювальні властивості, у реакціях з киснем, сіркою, оксидами металів та ін. – відновні властивості:
Ca+2C=CaC2 C+O2=CO2
4Al+3C=Al4C3 C+2S=CS2
2H2+C=CH4 C+PbO=Pb+CO

Карбон утворює два оксиди СО і СО2
СО (чадний газ) за звичайних умов поводить себе як несолетворний оксид, не реагує з водою, розчинами кислот і лугів. Однак при підвищеному тиску при нагріванні вступає в реакцію із лугами, утворюються солі мурашиної кислоти:
Со +NaOH HCOONa.
СО2 (вуглекислий газ), солетворний оксид, має властивості притаманні кислотним оксидам. Карбонатна (вугільна
кислота) нестійка, існує лише у
водному розчині, двохосновна.

Карбон утворює два оксиди СО і СО2
СО (чадний газ) за звичайних умов поводить себе як несолетворний оксид, не реагує з водою, розчинами кислот і лугів. Однак при підвищеному тиску при нагріванні вступає в реакцію із лугами, утворюються солі мурашиної кислоти:
Со +NaOH HCOONa.
СО2 (вуглекислий газ), солетворний оксид, має властивості притаманні кислотним оксидам. Карбонатна (вугільна
кислота) нестійка, існує лише у
водному розчині, двохосновна.

Карбон літосфери
В
А
П
Н
Я
К
Д
О
Л
О
М
І
Т
К
Р
Е
Й
Д
А
М
А
Р
М
У
Р
