Презентація на тему «Етери та естери»

Етери та естери

Етери або прості ефіри — органічні речовини, молекули яких складаються з двох вуглеводневих радикалів, сполучених між собою атомом кисню.
Прості ефіри – рухливі, легко закипаючі рідини, малорозчинні у воді, дуже легко займисті . Виявляють слабкі основні властивості.
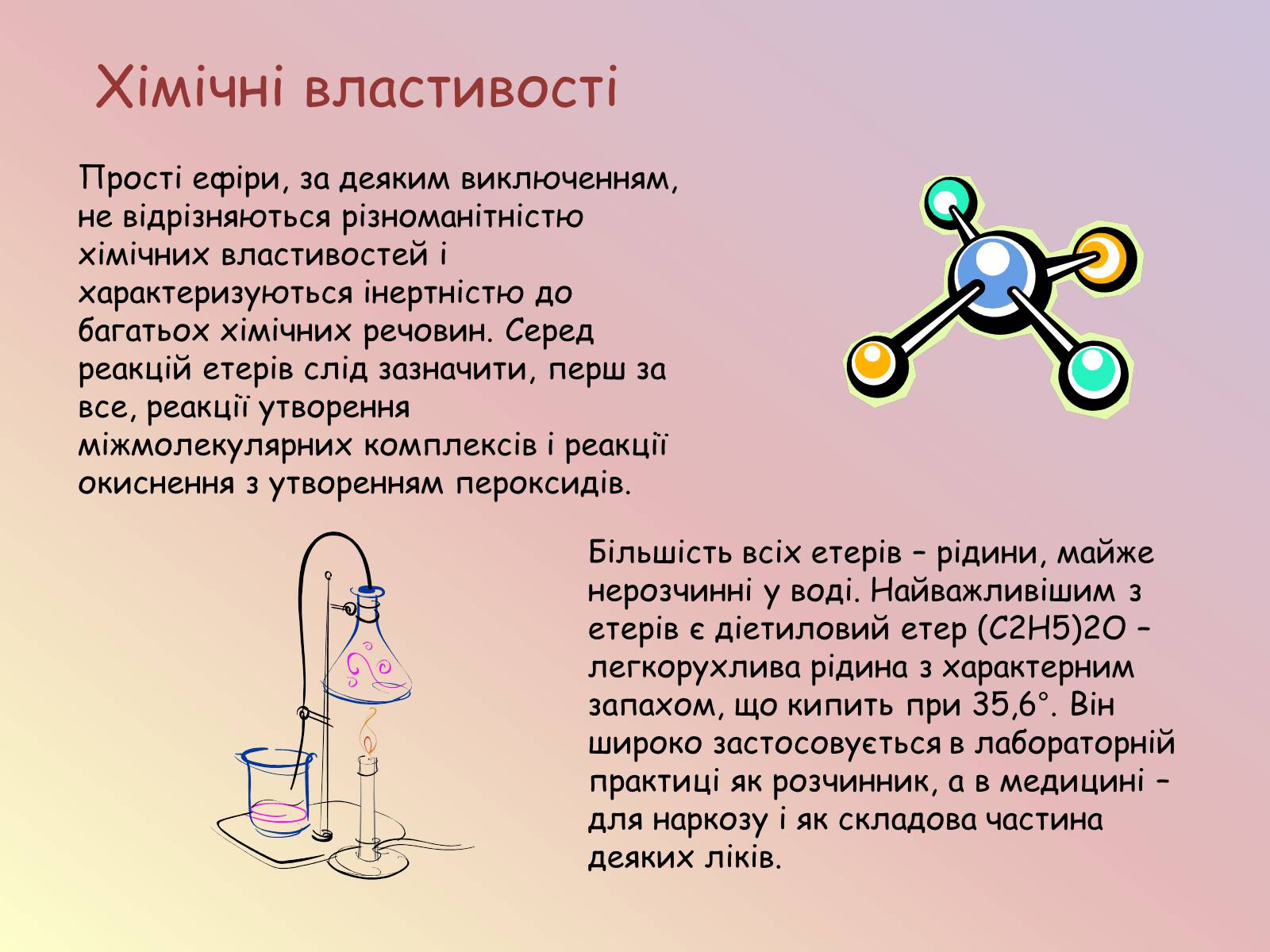
Більшість всіх етерів – рідини, майже нерозчинні у воді. Найважливішим з етерів є діетиловий етер (С2Н5)2О – легкорухлива рідина з характерним запахом, що кипить при 35,6°. Він широко застосовується в лабораторній практиці як розчинник, а в медицині – для наркозу і як складова частина деяких ліків.
Хімічні властивості
Прості ефіри, за деяким виключенням, не відрізняються різноманітністю хімічних властивостей і характеризуються інертністю до багатьох хімічних речовин. Серед реакцій етерів слід зазначити, перш за все, реакції утворення міжмолекулярних комплексів і реакції окиснення з утворенням пероксидів.
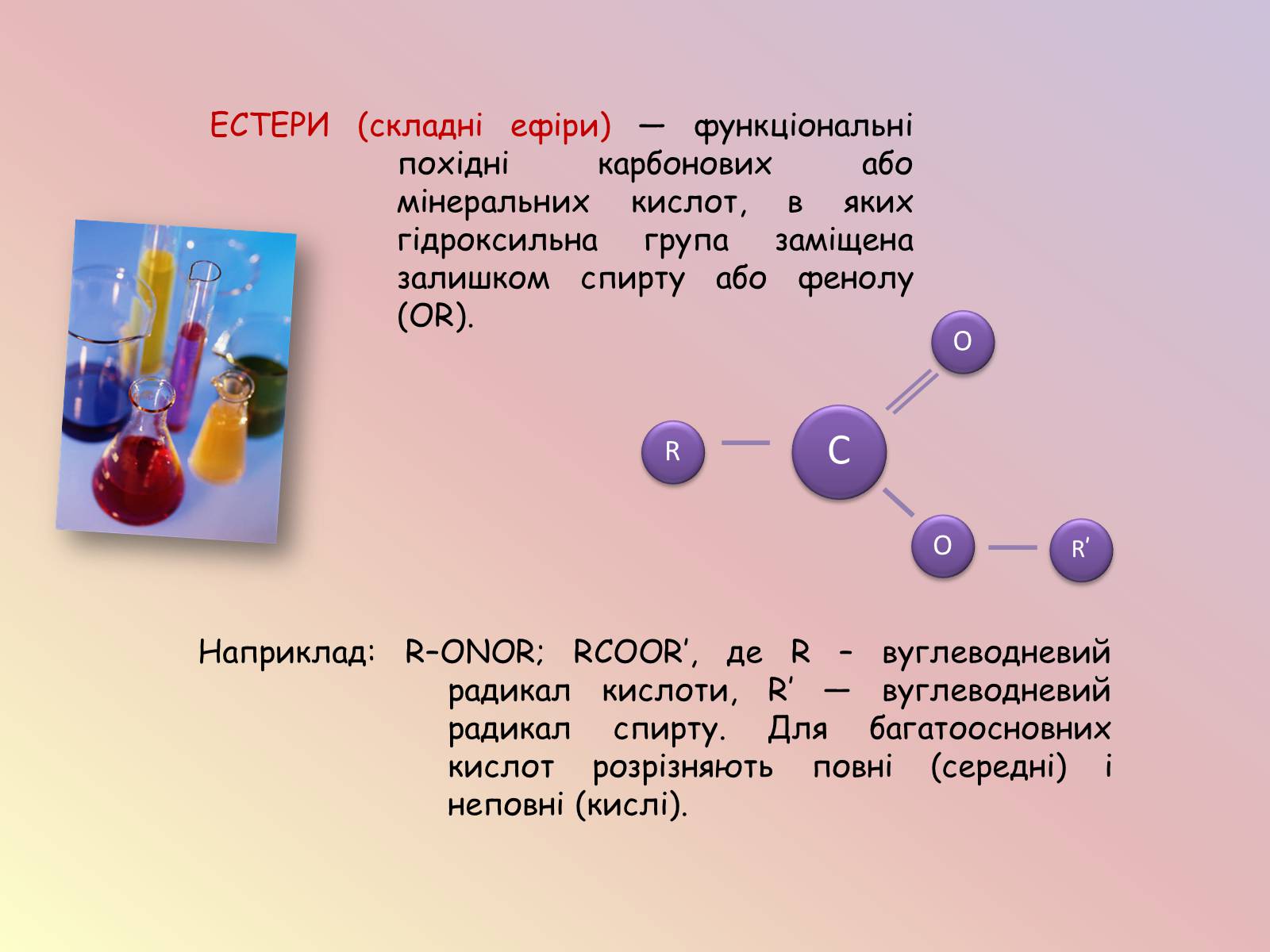
ЕСТЕРИ (складні ефіри) — функціональні похідні карбонових або мінеральних кислот, в яких гідроксильна група заміщена залишком спирту або фенолу (OR).
Наприклад: R–ONOR; RCOOR′, де R – вуглеводневий радикал кислоти, R′ — вуглеводневий радикал спирту. Для багатоосновних кислот розрізняють повні (середні) і неповні (кислі).
C
O
O
R′
R

Назви естерів утворюються від назв відповідних кислот і спиртів з додаванням слова естер.
Загальна формула естерів:
Наприклад:
етиловий естер оцтової кислоти,
за міжнародною систематичною номенклатурою — етилацетат (суфікс -ат).
де R1 — вуглеводневий радикал кислоти (у мурашиній кислоті це атом Гідрогену), R2 — вуглеводневий радикал спирту.

Естери нижчих карбонових кислот і спиртів:
леткі рідини, малорозчинні або нерозчинні у воді, добре розчинні у спирті та інших органічних розчинниках. Багато естерів мають приємний запах.
Естери вищих кислот і спиртів:
воскоподібні речовини, без запаху, нерозчинні у воді, добре розчинні в органічних розчинниках.
Фізичні властивості естерів

Реакція естерифікації
Реакції утворення естеру з кислоти і спирту називаються реакціями естерифікації. Ці реакції відбуваються з малою швидкістю, тому їх часто проводять за наявності сильних неорганічних кислот. При цьому йони Гідрогену діють як каталізатори.
Експериментально доведено, що під час реакції естерифікації від молекули карбонової кислоти відщеплюється гідроксильна група, а від молекули спирту – атом Гідрогену:

Хімічні властивості естерів
Взаємодія естеру з водою, що призводить до утворення вихідних спирту і кислоти, називається реакцією гідролізу, або омилення.
кислотний гідроліз (каталізатор - йони Гідрогену) оборотний:
лужний гідроліз (каталізатор - йони гідроксигрупи) необоротний, оскільки утворюється сіль карбонової кислоти:

Застосування естерів
Складні естери застосовуються:
як розчинники та розріджувачі для лаків і фарб
як ароматизатори в харчовій промисловості
у виробництві парфумів
при виготовленні штучних волокон (лавсан)
для виробництва СМЗ та вибухових речовин

У міру розвитку органічного синтезу дедалі більше речовин стало можливо добувати в лабораторії. Крім того чи мало отриманих запахів були абсолютно новими й у природі не зустрічалися. Це відкрило перед парфумерами всього світу необмежені можливості у винаході нових парфумів і ароматизаторів для косметичних засобів.
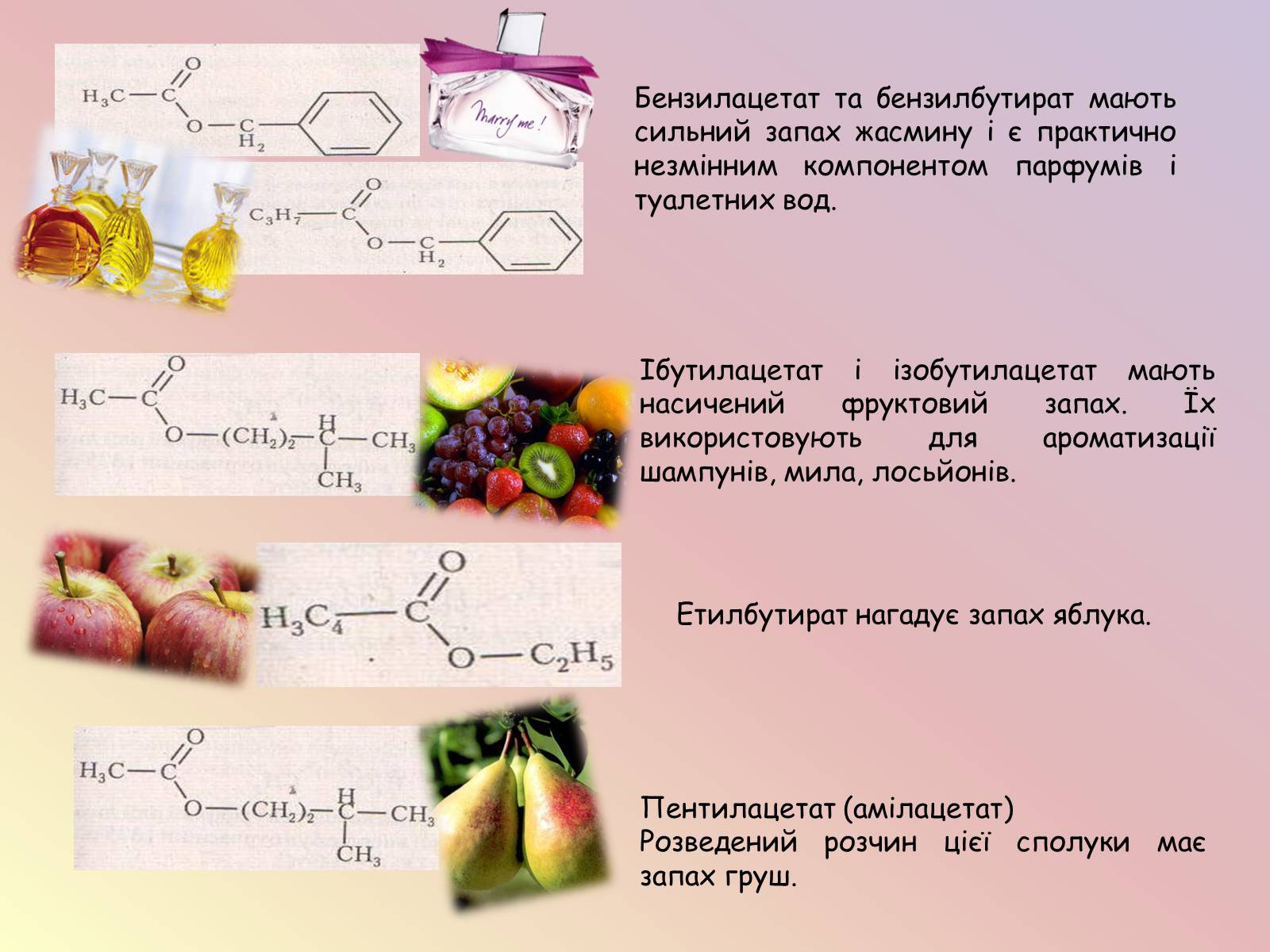
Бензилацетат та бензилбутират мають сильний запах жасмину і є практично незмінним компонентом парфумів і туалетних вод.
Етилбутират нагадує запах яблука.
Пентилацетат (амілацетат)
Розведений розчин цієї сполуки має запах груш.
Ібутилацетат і ізобутилацетат мають насичений фруктовий запах. Їх використовують для ароматизації шампунів, мила, лосьйонів.

Дякую за увагу!