Презентація на тему «Електричний струм у металах» (варіант 1)

Електричний струм у металах

Електричний струм - це упорядкований рух заряджених частинок.
Напрямок електричного струму співпадає з напрямком руху позитивних зарядів
Зарядженні частинки
Електрони
Протони
Іони
(катіони, аніони)

УМОВИ ІСНУВАННЯ ЕЛЕКТРИЧНОГО СТРУМУ:
Наявність вільних носіїв заряду;
Наявність різниці потенціалів (електричного поля);
Наявність сторонніх сил, які підтримують різницю потенціалів і переміщують заряд по замкненому контуру.

Речовини за здатністю проводити електричний струм поділяються на:
Діелек-трики
Провід-ники

Приклади: метали, грунт, розчини лугів і кислот у воді, графіт, тіло людини, тварини
Провідники – це речовини, що мають вільні заряди, тобто проводять електричний струм

Діелектрики – це речовини, що не мають вільних заряджених частинок, тобто не проводять електричний струм
Приклади: ебоніт, янтар, смола, порцеляна, гума, пластмаса, шовк, капрон та інші

Сила струму
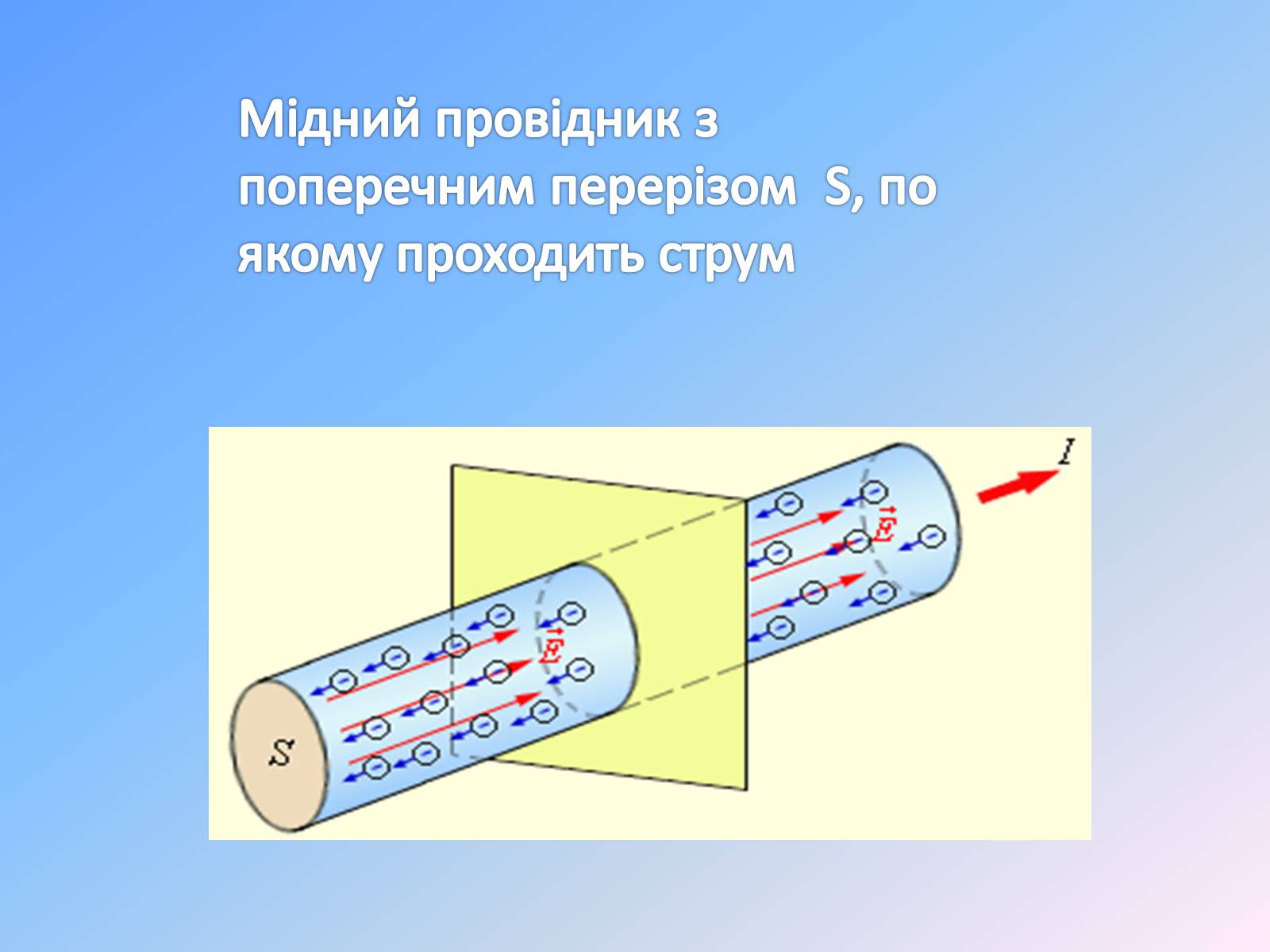
Мідний провідник з поперечним перерізом S, по якому проходить струм

Для металів характерний металічний тип зв'язку, суть якого полягає в тому, що атоми металів легко віддають зовнішні електрони, які переміщуються вільно по всій масі шматка металу. Атоми металів, що віддали електрони, стають позитивно зарядженими іонами. Останні притягують до себе електрони, що вільно рухаються. Одночасно інші атоми металу також віддають електрони. Отже, всередині шматка металу постійно циркулює “електронний газ”, який міцно зв'язує між собою всі атоми металу. Такий особливий тип хімічного зв'язку обумовлює фізичні та хімічні властивості металів. Іони розміщуються шарами у певному порядку один відносно одного, утворюючи певний тип кристалічної ґратки.
Властивості металів зумовлені насамперед особливостями будови кристалічних ґраток металів, міцністю зв'язку, будовою атомів.
Фізичні властивості металів
До таких властивостей металів належать:
Блиск
Твердість
Пласти-чність
Ковкість
Тепло- та електропровідність
Температура плавлення
Густина

Найважливішою фізичною характеристикою металічного стану є електрична провідність. Вона зумовлена наявністю рухливих електронів у кристалічній ґратці металів. Тому метали відносять до провідників І роду. За звичайних умов найкращу електропровідність має срібло, на другому місці – мідь, далі – алюміній. Метали з високою електропровідністю мають і високу теплопровідність, яка також пояснюється можливістю переміщення електронів.

Дослідне підтвердження електропровідності металів
У 1899 р. К. Рікке на трамвайній підстанції у Штутгарті вмикав у головний провід, яким подавалося живлення трамвайним лініям, послідовно три металевих циліндри, тісно притиснутих один до одного торцями: два крайніх — мідних, а середній — алюмінієвий. Через ці циліндри понад рік проходив електричний струм. У результаті точного зважування виявилося, що дифузія вметалах не відбулася: в мідних циліндрах не було атомів алюмінію і навпаки.Таким чином, К. Рікке довів, що під час проходження провідником електричного струму йони не переміщуються, а в різних металах переміщуються лише електрони. Отже, електричний струм у металевих провідниках створюється впорядкованим рухом електронів.
Отже, заряд в металах переноситься не іонами.

Дякую за увагу Виконала Скакалова Олександра 11-А