Презентація на тему «Білки» (варіант 9)

Білки
Розмаїтого Дмитра, 9-Б клас

Білки — складні високомолекулярні природні органічні речовини, що складаються з амінокислот, сполучених пептидними зв'язками.
Стрічкова молекулярна модель білка — ядерного антигену проліферуючих клітин (PCNA) людини.
Зазвичай білки є лінійними полімерами — поліпептидами, хоча інколи мають складнішу структуру. Невеликі білкові молекули, тобто олігомери поліпептидів, називаються пептидами. Послідовність амінокислот у конкретному білку визначається відповідним геном і зашифрована генетичним кодом.
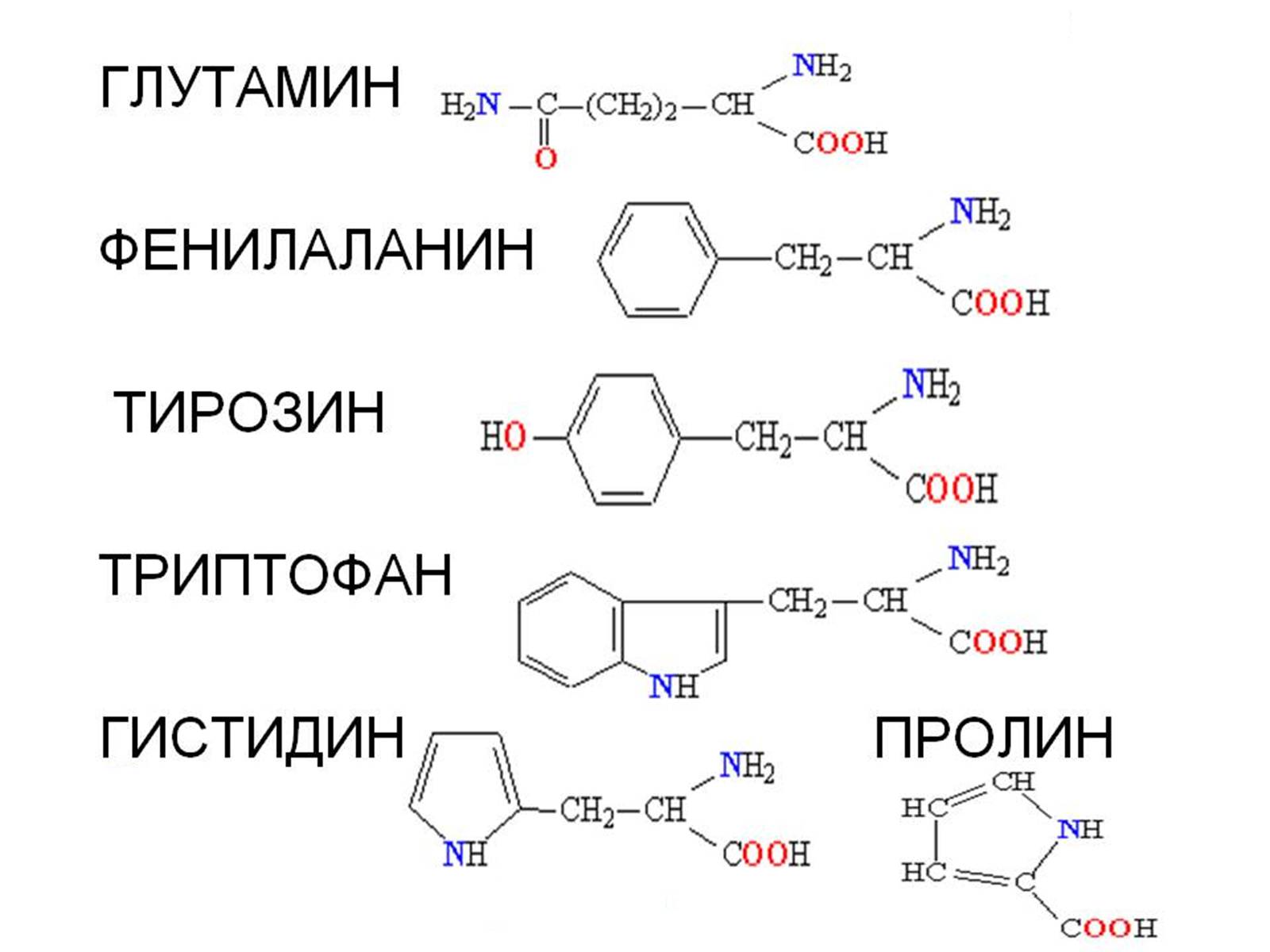
Хоча генетичний код більшості організмів визначає лише 20 «стандартних» амінокислот, їхнє комбінування уможливлює створення великого різноманіття білків із різними властивостями. Крім того, амінокислоти у складі білка часто піддаютьсяпосттрансляційним модифікаціям, які можуть виникати і до того, як білок починає виконувати свою функцію, і під час його «роботи» в клітині. Для досягнення певної функції білки можуть діяти спільно, і часто зв'язуються, формуючи великі стабілізовані комплекси (наприклад, фотосинтетичний комплекс).
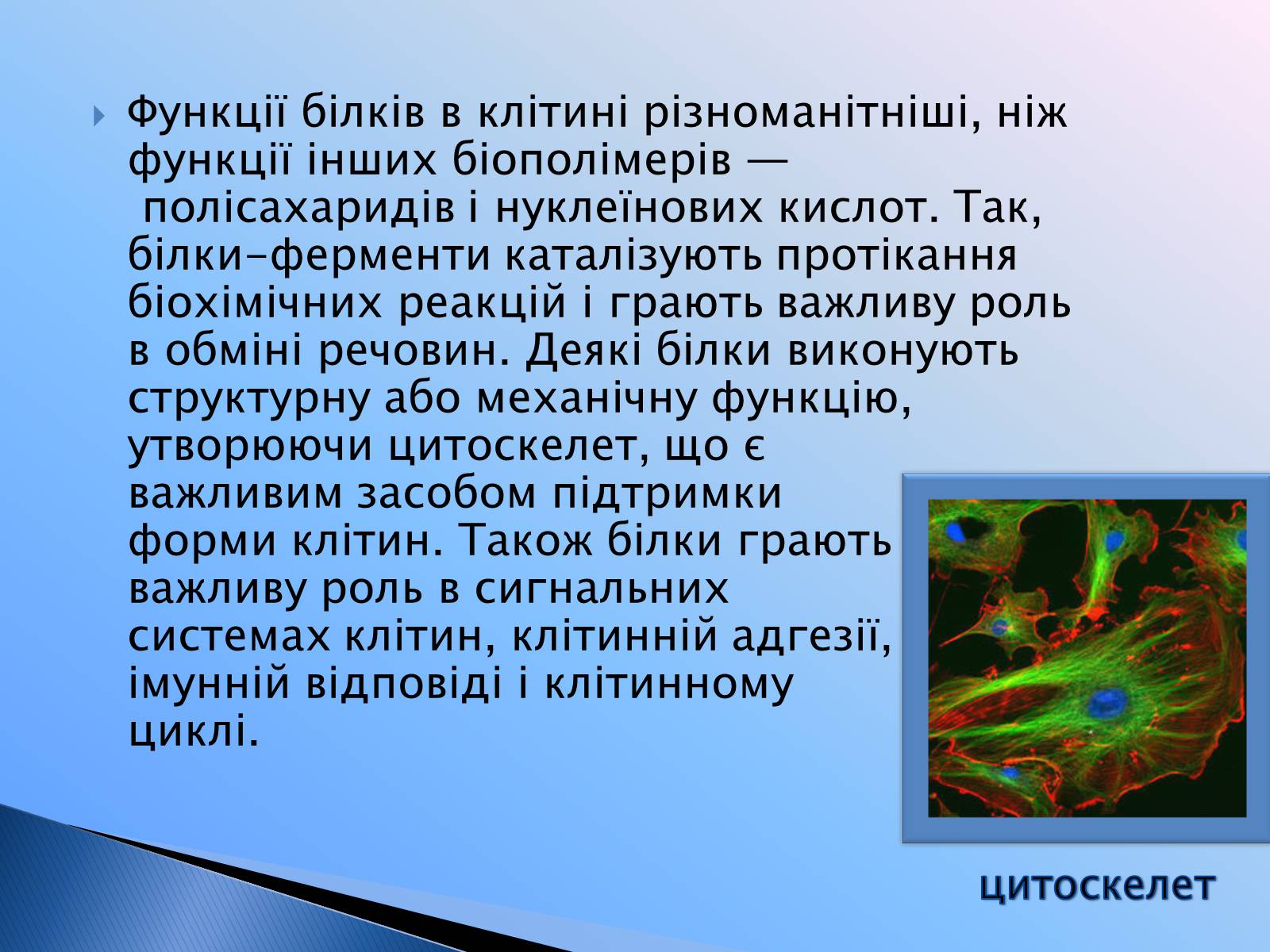
Функції білків в клітині різноманітніші, ніж функції інших біополімерів — полісахаридів і нуклеїнових кислот. Так, білки-ферменти каталізують протікання біохімічних реакцій і грають важливу роль в обміні речовин. Деякі білки виконують структурну або механічну функцію, утворюючи цитоскелет, що є важливим засобом підтримки форми клітин. Також білки грають важливу роль в сигнальних системах клітин, клітинній адгезії, імунній відповіді і клітинному циклі.
цитоскелет

Білки — важлива частина харчування тварин і людини, оскільки ці організми не можуть синтезувати повний набір амінокислот і повинні отримувати частину з них із білковою їжею. У процесі травлення протелітичні ферменти руйнують спожиті білки, розкладаючи їх до рівня амінокислот, які використовуються при біосинтезі білків організму або піддаються подальшому розпаду для отримання енергії.

Білки були вперше описані шведським хіміком Єнсом Якобом Берцеліусом в 1838 році, який і дав їм назву протеїни, від грец. πρώτα — «першорядної важливості». Проте, їхня центральна роль в життєдіяльності всіх живих організмів була виявлена лише у 1926 році, коли Джеймс Самнер показав, що фермент уреаза також є білком.

Секвенування першого білка — інсуліну, тобто визначення його амінокислотної послідовності, принесло Фредерику Сенгеру Нобелівську премію з хімії 1958 року. Перші тривимірні структури білків гемоглобіну і міоглобіну були отримані за допомогою рентгеноструктурного аналізу, за що автори методу, Макс Перуц і Джон Кендрю, отримали Нобелівську премію з хімії 1962 року.

Історія дослідження

Білки були виділені в окремий клас біологічних молекул у 18 столітті в результаті робіт французького хіміка Антуана де Фуркруа та інших учених, в яких було відмічено властивість білків коагулювати під час нагрівання або під дією кислот. У той час були досліджені такі білки, як альбумін з яєчних білків, фібрин з крові і глютен із зерна пшениці.

Голландський хімік Герріт Мульдер провів аналіз складу білків і виявив, що практично всі білки мають однакову емпіричну формулу. Мульдер також визначив продукти руйнування білків — амінокислоти — і для однієї з них (лейцину) майже точно визначив молекулярну масу — 131 дальтон.

Мульдеру, зокрема, належить перша модель хімічної будови білків, запропонована ним у 1836 році. Виходячи з теорії радикалів, він сформулював поняття про мінімальну структурну одиницю у складі білків. Саме ця одиниця зі складом C16H24N405 отримала пізніше назву «протеїну» (Pr), а концепція — теорії протеїну.

Сам термін «протеїн», що в сучасному розумінні означає білок більшістю європейських мов, був запропонований у 1838 році співробітником Мульдера Якобом Берцеліусом. Перевірка цієї моделі привернула увагу відомих хіміків свого часу, таких як Юстус Лібіх і Жан-Батист Дюма. Під впливом нових даних теорія протеїну декілька разів корегувалася, але все ж до кінця 1850-х років від неї довелося повністю відмовитися.

До кінця 19 століття вже було досліджено більшість амінокислот, що входять до складу білків. У 1894 році німецький фізіолог Альбрехт Коссель висунув теорію, що амінокислоти є головними структурними елементами білків. На початку 20-го століття німецький хімік Еміль Фішер експериментально доказав, що білки збудовані з залишків амінокислот, сполучених пептидними зв'язками.
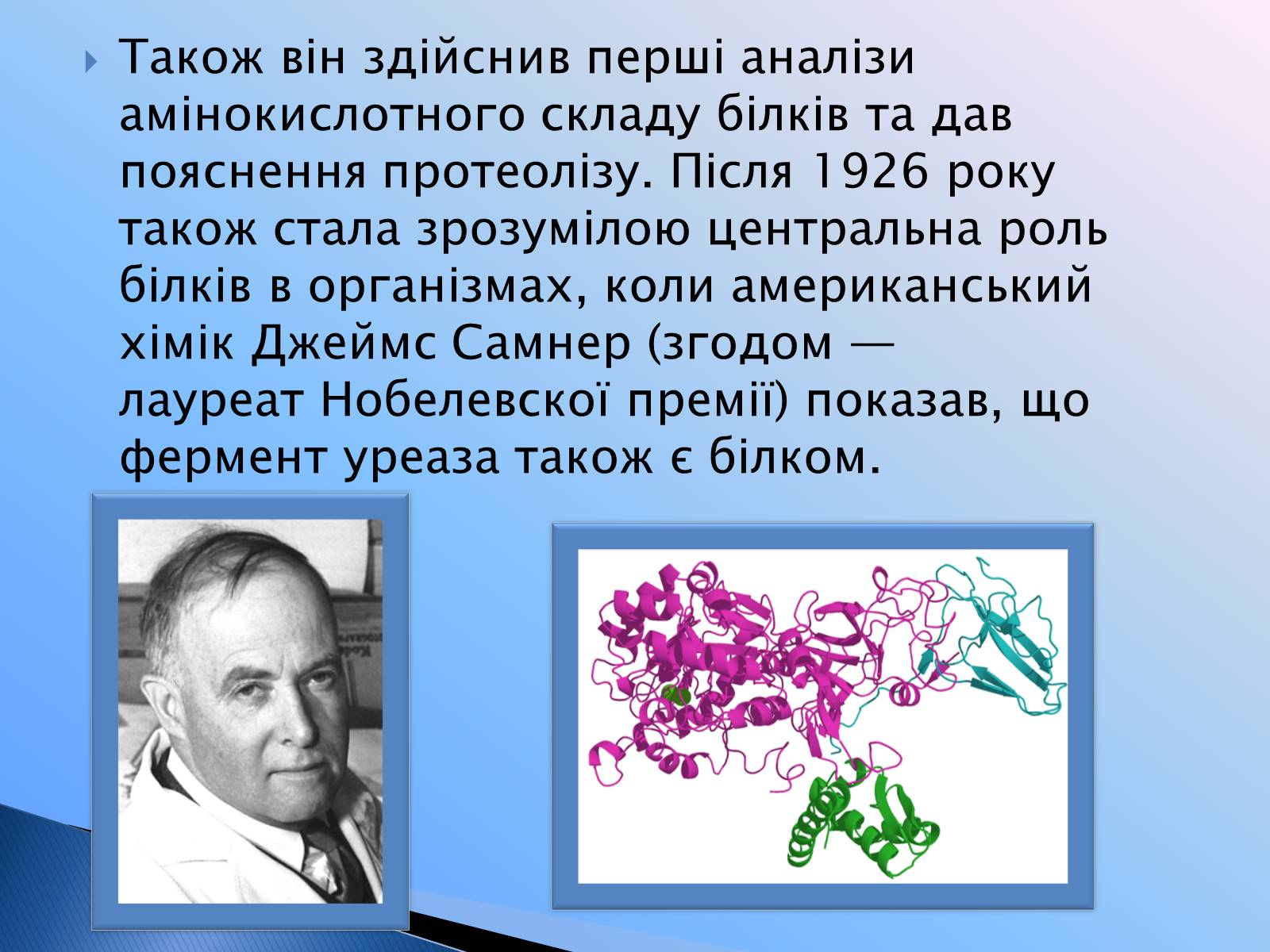
Також він здійснив перші аналізи амінокислотного складу білків та дав пояснення протеолізу. Після 1926 року також стала зрозумілою центральна роль білків в організмах, коли американський хімік Джеймс Самнер (згодом — лауреат Нобелевскої премії) показав, що фермент уреаза також є білком.

Вивченню білків перешкоджала складність їхнього виділення. Тому перші дослідження білків проводилися з використанням тих поліпептидів, які могли бути очищені у великій кількості, тобто білків крові, курячих яєць, різних токсинів і травних/метаболічних ферментів, які можна було виділити в місцях забою худоби. У кінці 1950-х років компанія Armour Hot Dog Co. змогла очистити кілограм бичачої панкреатичної рибонуклеази А, яка стала експериментальним об'єктом для багатьох учених.

Лайнус Полінг
Ідея про те, що вторинна структура білків утворюється в результаті формування водневих зв'язків між амінокислотами, була висловлена Вільямом Астбері в 1933 році, але Лайнус Полінг вважається першим ученим, який зміг успішно передбачити вторинну структуру білків.

Фред Сенгер
Пізніше Волтер Каузман, спираючись на роботи Кая Ліндерстрем-Ланга, зробив вагомий внесок до розуміння законів утворення третинної структури білків і ролі в цьому процесі гідрофобних взаємодій. У 1949 році Фред Сенгер визначив амінокислотну послідовність інсуліну, продемонструвавши таким способом, що білки — це лінійні полімери амінокислот, а не розгалужені (як у деякихцукрів) ланцюжки, колоїди або циклоли.

Перші структури білків, що ґрунтуються на методах рентгеноструктурного аналізу на рівні окремих атомів, були отримані в 1960-х роках, а за допомогою ЯМР-спектроскопії — в 1980-х роках. У 2006 році Банк даних білків (Protein Data Bank) містив приблизно 40 000 структур білків. У наш час кріоелектрона мікроскопіявеликих білкових комплексів за роздільною здатністю наближається до атомного рівня.

Протеом, ідентифікований при застосування гелевого електрофорезу в 2D гелі
Особливістю досліджень білків початку 21-го століття є одночасне отримання даних про білковий склад цілих клітин, тканин або організмів — протеоміка. У результаті необхідності аналізу цих даних та росту можливостей обчислювальних технологій активно розвиваються методи біоінформатики аналізу та порівняння білкових структур та обчислювальні методи передбачення структури білків, наприклад, методи молекулярної динаміки, призначені замінити в майбутньому експериментальне визначення білкових структур.

Будова

Молекули білків є лінійними полімерами, що складаються з α-L-амінокислот (які є мономерами цих полімерів) і, в деяких випадках, з модифікованих основних амінокислот (щоправда модифікаціївідбуваються вже після синтезу білка на рибосомі). Для позначення амінокислот в науковій літературі використовуються одно- або трьохбуквені скорочення.
Склад

Хоча на перший погляд може здатися, що використання «всього» 20 основних типів амінокислот обмежує різноманітність білкових структур, насправді кількість варіантів важко переоцінити: для ланцюжка всього з 5 амінокислот воно становить вже більше 3 мільйонів, а ланцюжок з 100 амінокислот (невеликий білок) може бути представлений більш ніж у 10130 варіантах (для порівняння — кількість атомів у Всесвіті оцінюється приблизно у 1080).

Поліпептидні ланцюжки завдовжки від двох до кількох десятків амінокислотних залишків зазвичай називають пептидами, при більшому ступені полімеризації — власне білками або протеїнами, хоча цей поділ вельми умовний.
Схематичне зображення утворення пептидного зв'язку. Подібна реакція відбувається на рибосомі — молекулярній машині для складання білків.

При утворенні білка в результаті взаємодії α-аміногрупи (-NH2) однієї амінокислоти з α-карбоксильною групою (-СООН) іншої амінокислоти утворюються пептидні зв'язки. Кінці білка називають С- і N- кінцями (залежно від того, яка з груп кінцевої амінокислоти вільна: -COOH чи -NH2, відповідно).
При природному синтезі білка на рибосомі, нові амінокислоти приєднуються до C-кінця, тому назва пептиду або білка дається шляхом перерахування амінокислотних залишків починаючи з N-кінця.

Послідовність амінокислот у білку відповідає інформації, що міститься в гені даного білка. Ця інформація представлена у вигляді нуклеотидної послідовності, причому одній амінокислоті відповідає одна або декілька послідовностей з трьох нуклеотидів — так званих кодонів. Те, яка амінокислота відповідає даному кодону в ДНК та мРНК(проміжній ланці біосинтезу білків), визначається генетичним кодом, який може дещо відрізнятися у різних організмів.
ДНК

Окрім послідовності амінокислот поліпептиду (первинної структури), для функціонування білків украй важлива тривимірна структура, яка формується в процесі згортання білків . Ця структура утримується в результаті взаємодії структур нижчих рівнів. Тривимірна структура білків за нормальних природних умов називається нативним станом білка. Хоча чимало білків здатні згортатися та приймати нативний стан самостійно, завдяки властивостям свого поліпептидного ланцюжка, інші вимагають допомоги інших білків, молекулярних шаперонів.
Рівні структури білків
До
Після

Виділяють чотири рівні структури білків:
Первинна
Вторинна
Третинна
Четвертинна

— пептидна або амінокислотна послідовність, тобто послідовність амінокислотних залишків у пептидному ланцюжку. Саме первинна структура кодується відповідним геном і найбільшою мірою визначає властивості сформованого білка.
Первинна структура
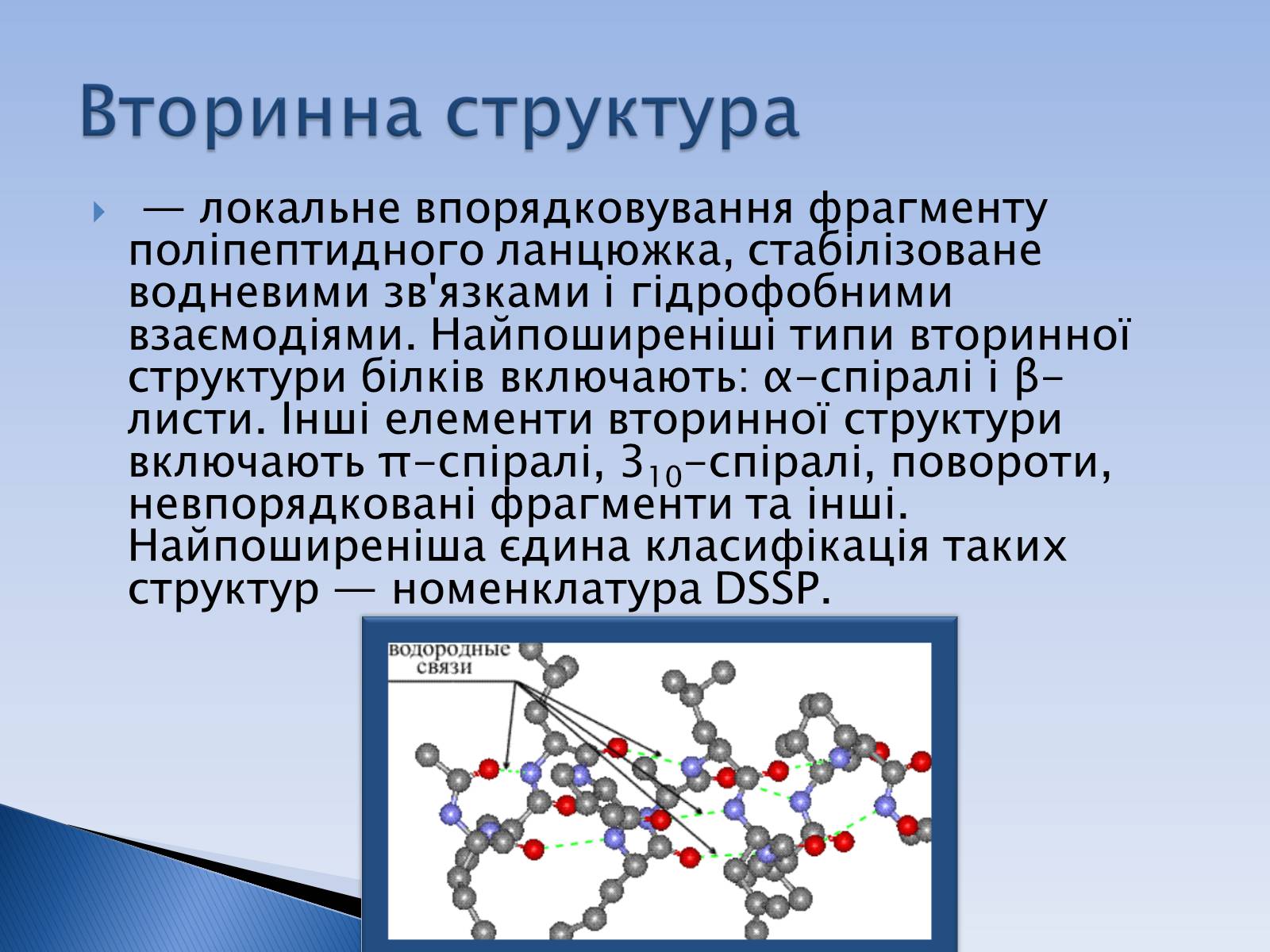
— локальне впорядковування фрагменту поліпептидного ланцюжка, стабілізоване водневими зв'язками і гідрофобними взаємодіями. Найпоширеніші типи вторинної структури білків включають: α-спіралі і β-листи. Інші елементи вторинної структури включають π-спіралі, 310-спіралі, повороти, невпорядковані фрагменти та інші. Найпоширеніша єдина класифікація таких структур — номенклатура DSSP.
Вторинна структура
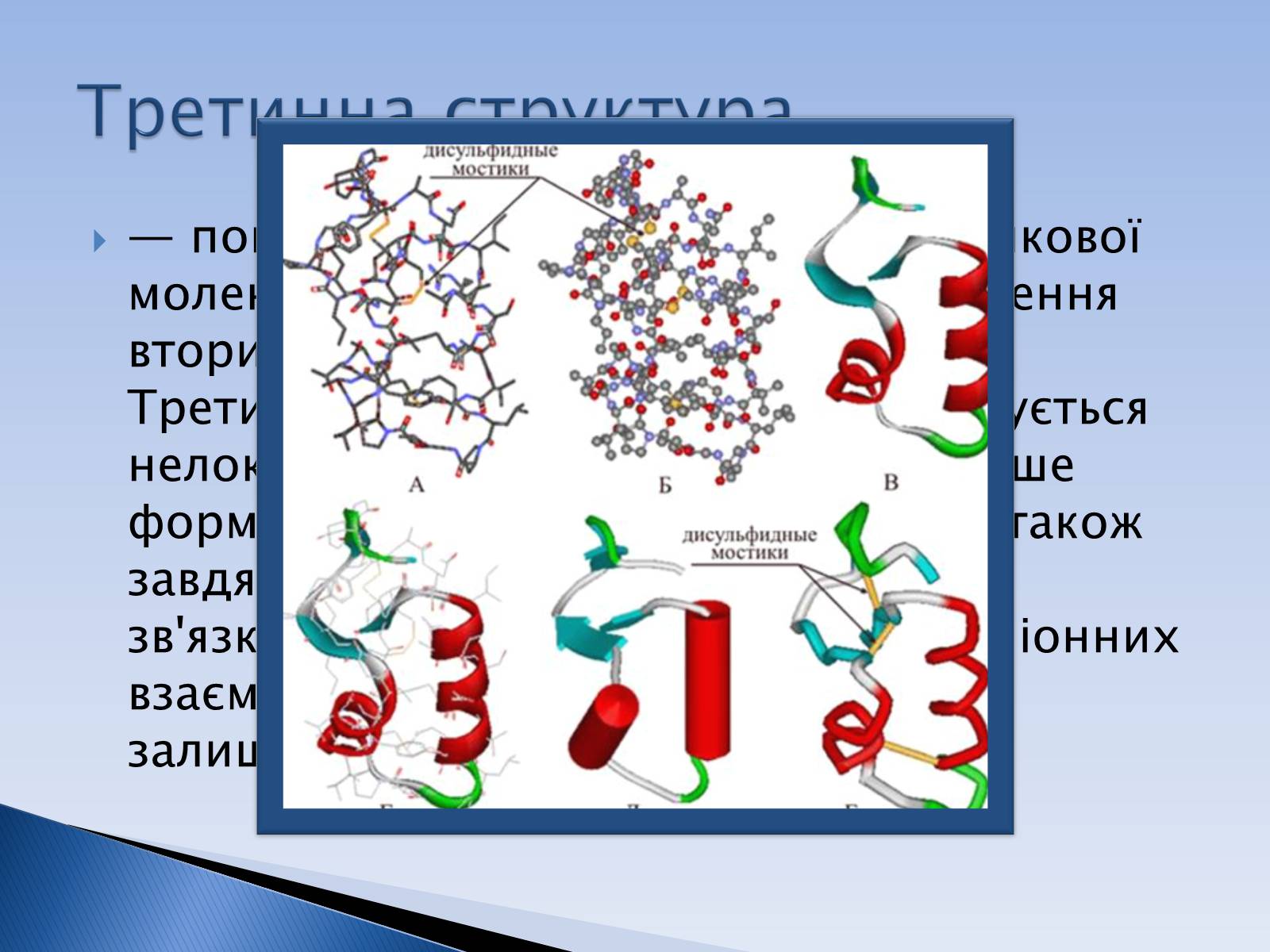
— повна просторова будова цілої білкової молекули, просторове взаємовідношення вторинних структур одна до одної. Третинна структура загалом стабілізується нелокальними взаємодіями, найчастіше формуванням гідрофобного ядра, а також завдяки утворенню водневих зв'язків, солевих містків, інших типів іонних взаємодій, дисульфідних зв'язків між залишками цистеїну.
Третинна структура
До третинної структури зазвичай відносять і проміжні рівні між основними елементами вторинної структури та повною структурою білка — «надвторинну» структуру, що складається із структурних мотивів та доменів. Структурні мотиви — невеликі усталені поєднання кількох елементів вторинної структури, що мають схожу структуру, важливу для виконання білком певних функцій. Схожі структурні мотиви зазвичай виконують схожі функції, завдяки чому за ними можна передбачити функцію невідомого білка.

— структура, що виникає в результаті взаємодії кількох білкових молекул, які в даному контексті називають субодиницями. Повна структура кількох поєднаних субодиниць, що разом виконують спільну функцію, називається білковим комплексом.
Четвертинна структура

Розмір білка може вимірюватися за числом амінокислот або в одиницях молекулярної маси —дальтонах — Да. Найбільшим відомим одиничним білком є тітін, що містить понад 29 тис. амінокислот і має молекулярну масу 3 МДа, а найбільший внутрішньоклітинний білковий комплекс —комплекс ядерної пори хребетних тварин — має масу біля 125 МДа.
Розміри
Порівняльні розміри білків та пептидів. Зліва направо: Антитіло(IGG), гемоглобін, інсулін (гормон), аденілаткіназа (фермент) і глютамінсинтетаза (фермент).

Як правило, білки протягом досить довгого часу зберігають структуру і, отже, фізико-хімічні властивості, наприклад, розчинність, в умовах (таких як pH, температура), до яких пристосований даний організм або які підтримуються в його межах в результаті збереження гомеостазу. Різка зміна цих умов, наприклад, внаслідок нагрівання або обробки білка кислотою чи лугом, приводить до втрати четвертинної, третинної і вторинної структур білка, цей процес називається денатурацією. Відомий випадок денатурації білка в побуті — приготування курячого яйця, коли під впливом високої температури розчинний у воді прозорий білок овальбумін стає щільним, нерозчинним і непрозорим.
Денатурація білків
Необоротна денатурація білка курячого яйця під впливом високої температури.

Як правило, білки протягом досить довгого часу зберігають структуру і, отже, фізико-хімічні властивості, наприклад, розчинність, в умовах (таких як pH, температура), до яких пристосований даний організм або які підтримуються в його межах в результаті збереження гомеостазу. Різка зміна цих умов, наприклад, внаслідок нагрівання або обробки білка кислотою чи лугом, приводить до втрати четвертинної, третинної і вторинної структур білка, цей процес називається денатурацією. Відомий випадок денатурації білка в побуті — приготування курячого яйця, коли під впливом високої температури розчинний у воді прозорий білок овальбумін стає щільним, нерозчинним і непрозорим.
Денатурація білків
Необоротна денатурація білка курячого яйця під впливом високої температури.

Використання людиною

Харчування
Борщ — джерело різноманітних денатурованих рослинних і тваринних білків.
Білки надходять в організм разом з їжею й служать основним джерелом амінокислот. Обов'язкове використання білків у їжі обумовлене потребою в незамінних амінокислотах, які не можуть синтезуватися людиною з інших речовин. Травленняпочинається з кислотної денатурації білків у шлунку — необхідної стадії для кулінарно неопрацьованої їжі. Денатуровані білки стають субстратом для протеаз, спочатку в шлунку, а потім у слаболужньому середовищі тонкого кишечнику.

Значна кількість досліджень у медицині направлена на використання білків в якості терапевтичних препаратів та засобів діагностикизахворювань. Фармацевтичне застосування білків почалося з природних білків отриманих з різноманітних живих організмів. Нові препарати створюються штучно, рекомбінантними методами або за допомогою проектування білків.
Білкові лікувальні препарати
Суміш для нарощування м'язів (США) містить білки молочної сироватки.

Дякую за увагу!
І за терпіння…