Презентація на тему «Білки» (варіант 13)

Білки

Білки́ — складні високомолекулярні природні органічні речовини, що складаються з амінокислот, сполучених пептидними зв'язками.
Білки — важлива частина харчування тварин і людини, оскільки ці організми не можуть синтезувати повний набір амінокислот і повинні отримувати частину з них із білковою їжею.

Білки були вперше описані шведським хіміком Єнсом Якобом Берцеліусом в 1838 році, який і дав їм назву протеїни. Проте, їхня центральна роль в життєдіяльності всіх живих організмів була виявлена лише у 1926 році, коли Джеймс Самнер показав, що фермент уреаза також є білком. Секвенування першого білка — інсуліну, тобто визначення його амінокислотної послідовності, принесло Фредерику Сенгеру Нобелівську премію з хімії 1958 року. Перші тривимірні структури білків гемоглобіну і міоглобіну були отримані за допомогою рентгеноструктурного аналізу, за що автори методу, Макс Перуц і Джон Кендрю, отримали Нобелівську премію з хімії 1962 року.
Історія дослідження білків
Єнс Якоб Берцеліус

Джеймс Бетчеллер Самнер
Фредерік Сенгер
Макс Фердинанд Перуц
Джон Коудери Кендрю

Склад
Молекули білків є лінійними полімерами, що складаються з амінокислот (які є мономерами цих полімерів) і, в деяких випадках, з модифікованих основних амінокислот (щоправда модифікації відбуваються вже після синтезу білка на рибосомі).
Будова
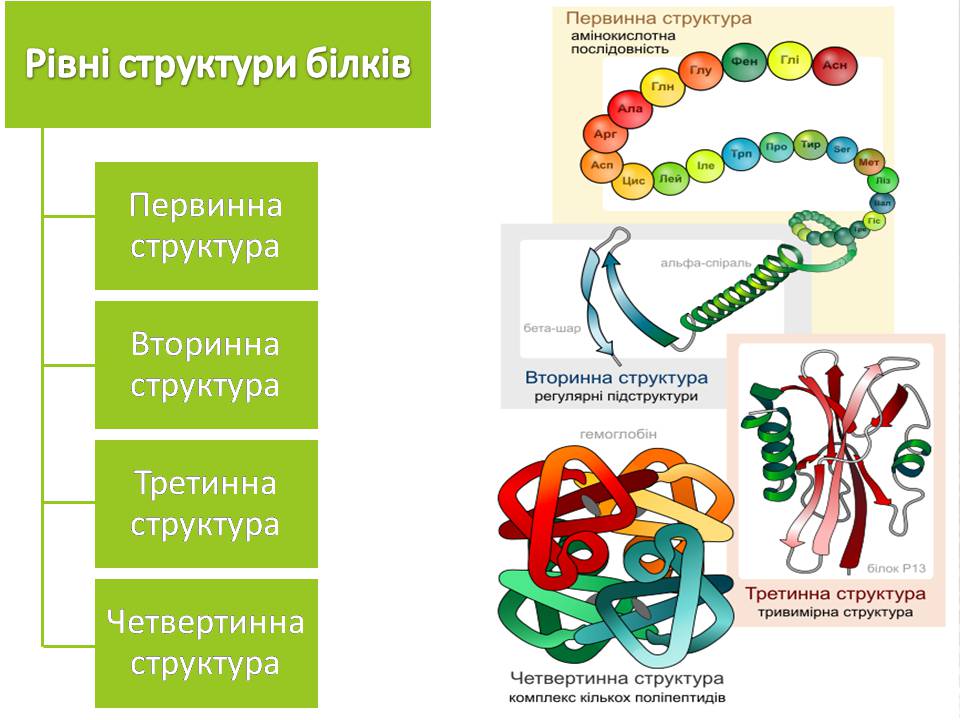
Рівні структури білків
Четвертинна структура
Третинна структура
Вторинна структура
Первинна структура
На відміну від них складні білки мають також неамінокислотні групи. Ці додаткові групи у складі складних білків називаються простетичними групами.
Білки
Прості
Складні
Прості білки містять тільки амінокислоти, зв'язані в ланцюжки.

Білки дуже відрізняються між собою за властивостями. Це
залежить від наявності в їхньому складі амінокислот із
різними функціональними групами, здатними вступати в
характерні для них реакції.
Денатурація - це руйнування четвертинної, третинної, вторинної структури білка під дією високої температури, радіації, хімічних реагентів;
Гідроліз – під час нього білок розщеплюється на окремі амінокислоти, з яких побудований;
Кольорові реакції білків – використовують для їх аналітичного визначення.
Хімічні властивості білків:

Білки - амфотерні електроліти. При певному значенні pH
середовища кількість позитивних і негативних зарядів у
молекулі білка однакова.
Білки мають різноманітну будову.
- Є білки нерозчинні у воді, є білки легко розчинні у воді;
- Є білки малоактивні у хімічному відношенні;
- Є білки вкрай нестійкі;
- Є білки, що досягають у довжину сотень нанометрів;
Є білки, що мають форму кульок діаметром усього
5-7 нм.Вони мають велику молекулярну масу (104-107).
Фізичні властивості білків:

Харчування
При споживанні білка (білків) в складі їжі, молекули білка руйнуються в травній системі у процесі травлення під дією кислого (у шлунку) та лужного (в стравоході та кишечнику) середовища та протеолітичними ферментами (протеазами) на пептиди та амінокислоти, що всмоктуються клітинами кишечника та використовуються організмом. Білок в харчуванні перш за все важливий як джерело незамінних амінокислот, які тваринний організм не може безпосередньо синтезувати. Крім того, білок їжі є важливим джерелом азоту. Білки, подібно вуглеводам, містять 4 ккал на грам (тоді як жири містять 9 ккал, а спирти 7 ккал на грам). Білки можуть бути перетворені на вуглеводи або жири в результаті метаболічних процесів організму.
Використання людиною

Харчування
При споживанні білка (білків) в складі їжі, молекули білка руйнуються в травній системі у процесі травлення під дією кислого (у шлунку) та лужного (в стравоході та кишечнику) середовища та протеолітичними ферментами (протеазами) на пептиди та амінокислоти, що всмоктуються клітинами кишечника та використовуються організмом. Білок в харчуванні перш за все важливий як джерело незамінних амінокислот, які тваринний організм не може безпосередньо синтезувати. Крім того, білок їжі є важливим джерелом азоту. Білки, подібно вуглеводам, містять 4 ккал на грам (тоді як жири містять 9 ккал, а спирти 7 ккал на грам). Білки можуть бути перетворені на вуглеводи або жири в результаті метаболічних процесів організму.
Використання людиною

Значна кількість досліджень у медицині направлена на використання білків в якості терапевтичних препаратів та засобів діагностики захворювань. Біофармацевтичні препарати, що знаходять широке використання, включають білки крові (наприклад, для лікування гемофілії), тромболітичні ферменти, гормони, цитокіни та фактори росту, білки імунної системи (інтерферони і антитіла, що використовуються для лікування інфекційних захворювань та деяких видів раку) і вакцини.
Білкові лікувальні препарати
Суміш для нарощування м'язів

Серед всіх білків в харчовій промисловості активно використовуються численні ферменти. Так, у пекарській промисловості використовуються альфа-амілаза і протеази; у пивоварінні використовуються численні ферменти ячменю (амілаза, глюканази, протеази); целюлази і пектинази використовуються для освітлення соків; хімозин, ліпаза і лактаза використовуються для виготовлення кисломолочних продуктів; а папаїн застосовується для пом'якшення м'ясних продуктів. Для виготовлення крохмалю використовують амілазу і глюкоамілазу, а для виготовлення паперу — целюлази і ксиланазу. Також протео- і ліполітичні ферменти часто додаються до миючих засобів.
Іншим використанням білків є використання фібрилярних білків для виготовлення волокон, що використовуються, зокрема, в текстильній промисловості.
Використання в промисловості