Презентація на тему «Амінокислоти» (варіант 1)

Амінокислоти
Корєшкова А. В.

Амінокислота
Органічна сполука, молекули якої одночасно містять аміно- (-NH2) та карбоксильну (-COOH) групи;
Є мономерними одиницями білків, у складі яких залишки амінокислот з'єднані пептидними зв'язками;
Більшість побудовані із комбінації 19 “первинних” амінокислот, тобто таких, що містять первинну аміногрупу, і однієї “вторинної” амінокислоти аба імінокислоти проліну, що кодуються генетичним кодом.
номенклатура
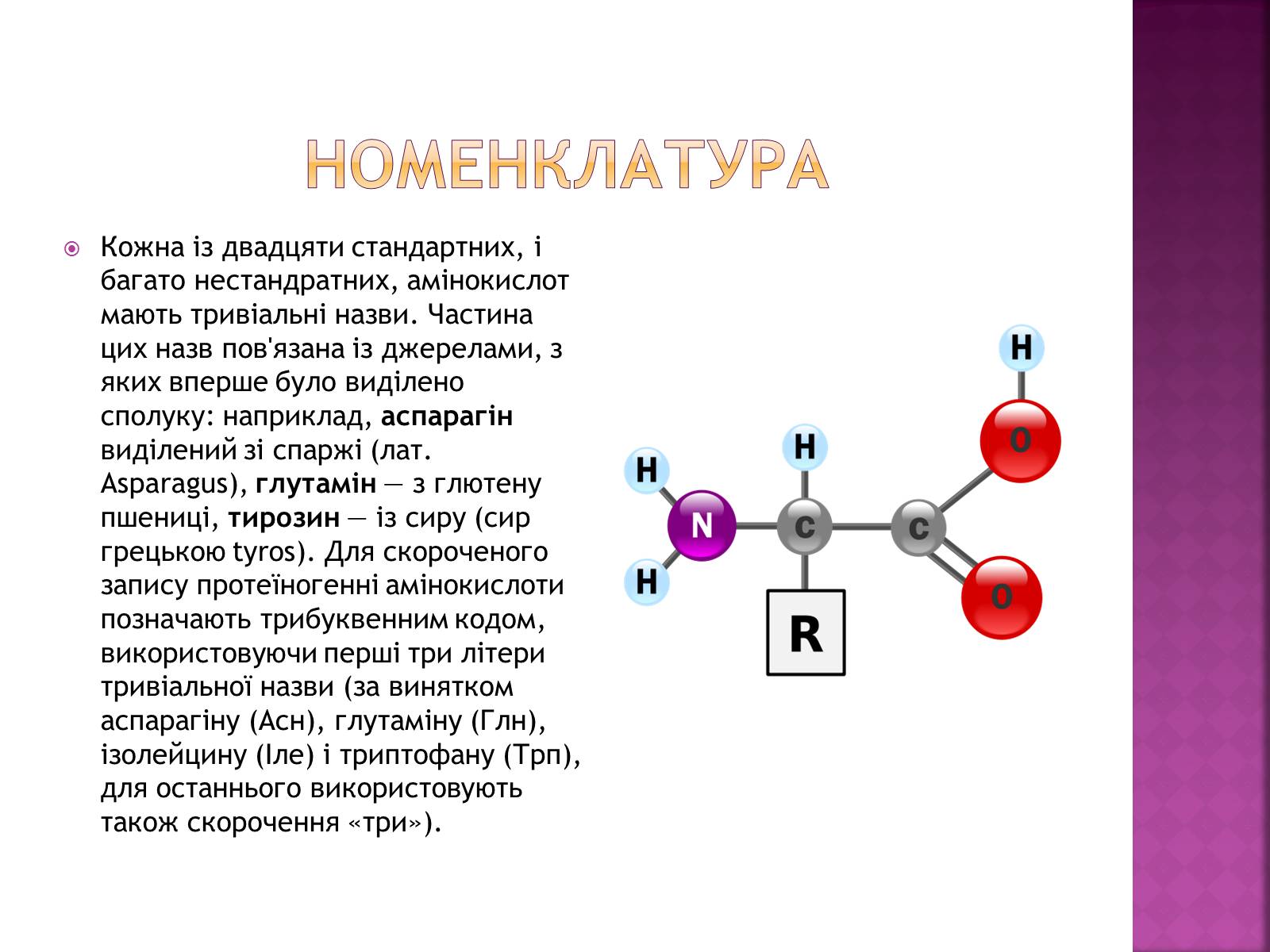
Кожна із двадцяти стандартних, і багато нестандратних, амінокислот мають тривіальні назви. Частина цих назв пов'язана із джерелами, з яких вперше було виділено сполуку: наприклад, аспарагін виділений зі спаржі (лат. Asparagus), глутамін — з глютену пшениці, тирозин — із сиру (сир грецькою tyros). Для скороченого запису протеїногенні амінокислоти позначають трибуквенним кодом, використовуючи перші три літери тривіальної назви (за винятком аспарагіну (Асн), глутаміну (Глн), ізолейцину (Іле) і триптофану (Трп), для останнього використовують також скорочення «три»).

Абревіатури амінокислот
Для позначення шести амінокислот використані їх початкові літери (в англійській мові), оскільки вони є унікальними (CHIMSV). Ще у п'яти (AGLPT) перші букви не є унікальними, але позначають більш розповсюджені амінокислоти (наприклад, літера L позначає лейцин, оскільки він зустрічається частіше ніж лізин).

Хімічна будова
Усі амінокислоти містять карбоксильну й аміногрупи. В α-амінокислот вони приєднані до одного і того ж атома карбону. Решту молекули називають бічним ланцюгом або R-групою. Ці групи відрізняються за розміром, формою, гідрофільністю, електричним зарядом, схильністю формувати водневі зв'язки і загальною реакційною здатністю надаючи кожній амінокислоті унікальних властивостей. У найменшої амінокислоти — гліцину — бічного ланцюга немає, біля α-атома карбону крім карбоксильної і аміногрупи розташовані два атоми водню.
“нестандартні амінокислоти”
Крім 20 «стандартних» амінокислот, що кодуються генетичним кодом, у живих організмах також трапляється велика кількість так званих нестандартних амінокислот.
У складі готових поліпептидних ланцюгів деякі залишки амінокислот можуть модифікуватись. Таким чином, наприклад, утворюються нестандарнті амінокислоти 5-гідроксилізин і 4-гідроксипролін. Обидві входять до складу білка сполучної тканини колагену, а гідроксипролін знайдений також у клітинних стінках рослин.

“нестандартні” амінокислоти
6-N-метиллізин є складовою скоротливого білка міозину. Деякі білки, які зв'язують іони кальцію, наприклад, протромбін, містять γ-карбоксиглутамат. Десмозин — складна амінокислота, що утворюється із чотирьох залишків лізину — знайдена у фібрилярному білку еластині. Багато залишків амінокислот можуть бути посттрансляційно модифіковані тимчасово з метою регуляції функції білків. До таких модифікацій належить приєднання фосфтаних, метильних, ацетильних, аденільних, АДФ-рибозильних та інших груп.

“нестандартні” аміноксилоти
Всього у живих клітинах зустрічається близько 700 різних амінокислот, багато із яких виконують самостійні функції. Наприклад, орнітин і цитрулін є ключовими метаболітами у циклі сечовини і шляху біосинтезу аргініну, гомоцистеїн — проміжний продукт метаболізму деяких амінокислот, S-аденозилметіонін – відіграє роль метилюючого агенту.
Деякі з амінокислот також знайдені і в метеоритах, особливо в карбонових хондритах.
Функції амінокислот
На додаток до синтезу білків, стандартні і нестандартні амінокислоти в тваринному організмі виконують багато інших важливих біологічних функцій. Гліцин та глутамат (аніон глутамінової кислоти) використовуються як нейромедіатори при нервовій передачі через хімічні синапси, нейромедіаторами також є нестандартна амінокислота гамма-аміномасляна кислота, що є продуктом декарбоксилювання глутамату, дофамін — похідне тирозину, і серотонін, який утворюється із триптофану. Гістидин є попередником гістаміну – локального медіатора запальних і алергічних реакцій. Йодовмісний гормон щитоподібної залози тироксин утворюється із тирозину. Гліцин є одним із метаболічних попередників порфіринів (таких як дихальний пігмент гем)

Функції амінокислот
Деякі з 20-ти протеїногенних амінокислот називаються «незамінними» — це такі, що не виробляються в організмі і повинні надходити з їжею. Для людини це лізин, лейцин, ізолейцин, метіонін, фенілаланін, треонін, триптофан, валін, а для дітей також гістидин та аргінін.
Кислотно-основні властивості
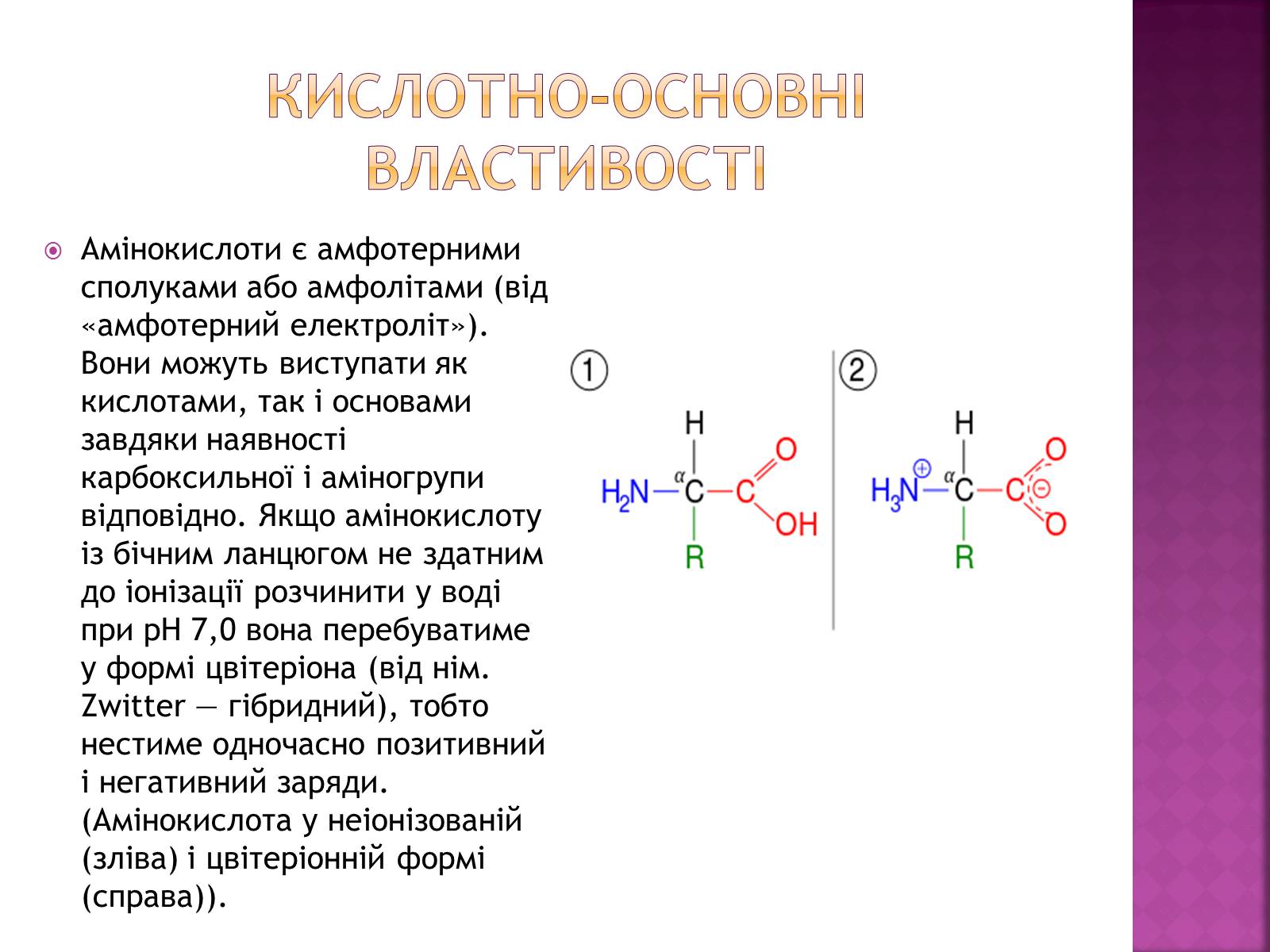
Амінокислоти є амфотерними сполуками або амфолітами (від «амфотерний електроліт»). Вони можуть виступати як кислотами, так і основами завдяки наявності карбоксильної і аміногрупи відповідно. Якщо амінокислоту із бічним ланцюгом не здатним до іонізації розчинити у воді при pH 7,0 вона перебуватиме у формі цвітеріона (від нім. Zwitter — гібридний), тобто нестиме одночасно позитивний і негативний заряди. (Амінокислота у неіонізованій (зліва) і цвітеріонній формі (справа)).