Презентація на тему «Атоми, Молекули. Йони»

Атоми,молекули, йони,
хімічні елементи,
їхні назви й символи

Мета
Поглибити знання учнів про атоми і молекули як складні структурні частинки речовини.
Дати поняття про йони як заряджені частинки речовини.
На основі будови атома дати поняття про хімічний елемент як певний тип атомів.
Познайомити учнів із сучасною науковою українською номенклатурою. Дати уявлення про поширення хімічних елементів у природі

Властивості речовин залежать від того, які частинки входять до їх складу і як вони між собою з'єднуються.
Відомо, що багато які речовини складаються з молекул.
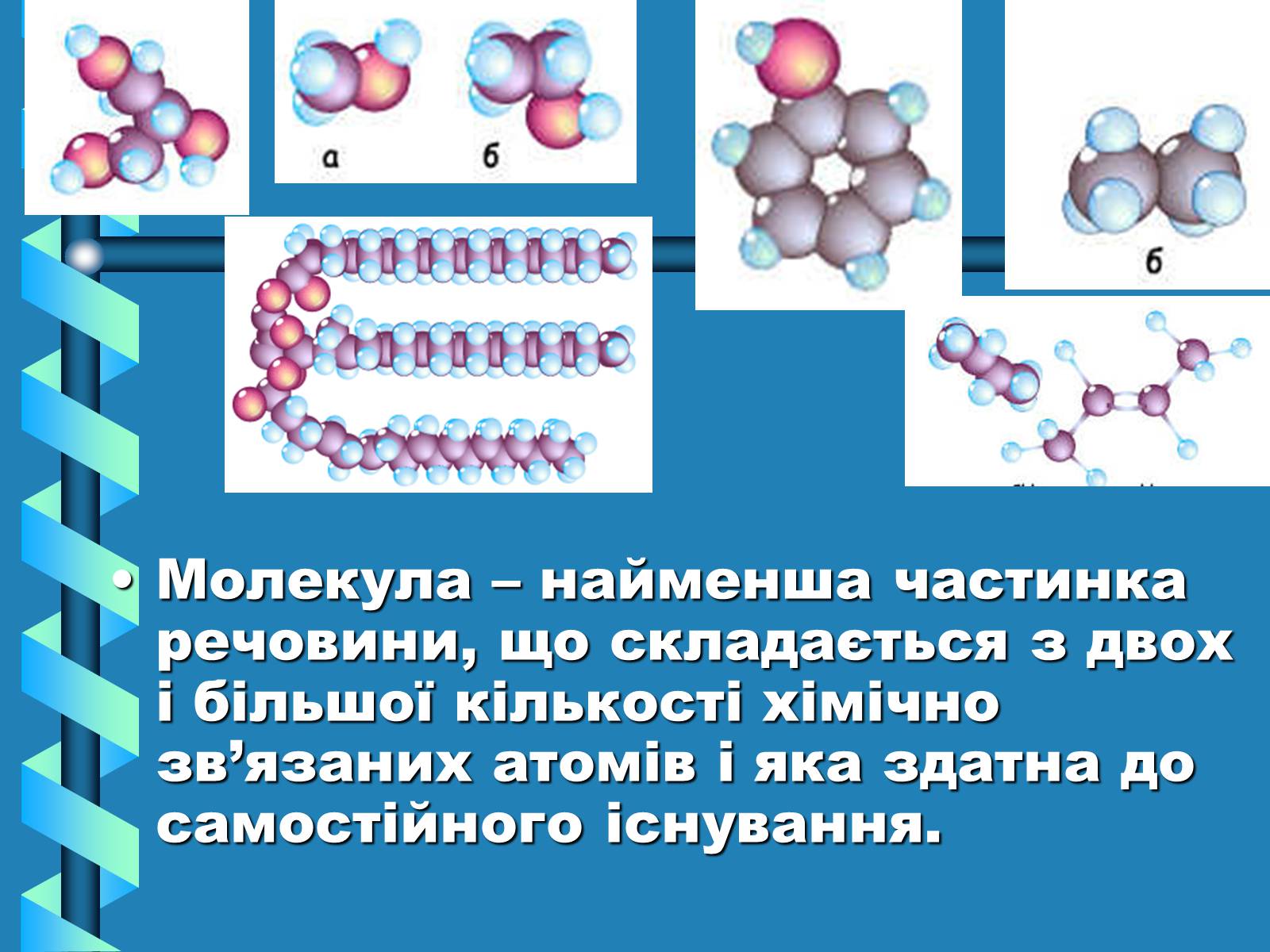
Молекула – найменша частинка речовини, що складається з двох і більшої кількості хімічно зв'язаних атомів і яка здатна до самостійного існування.
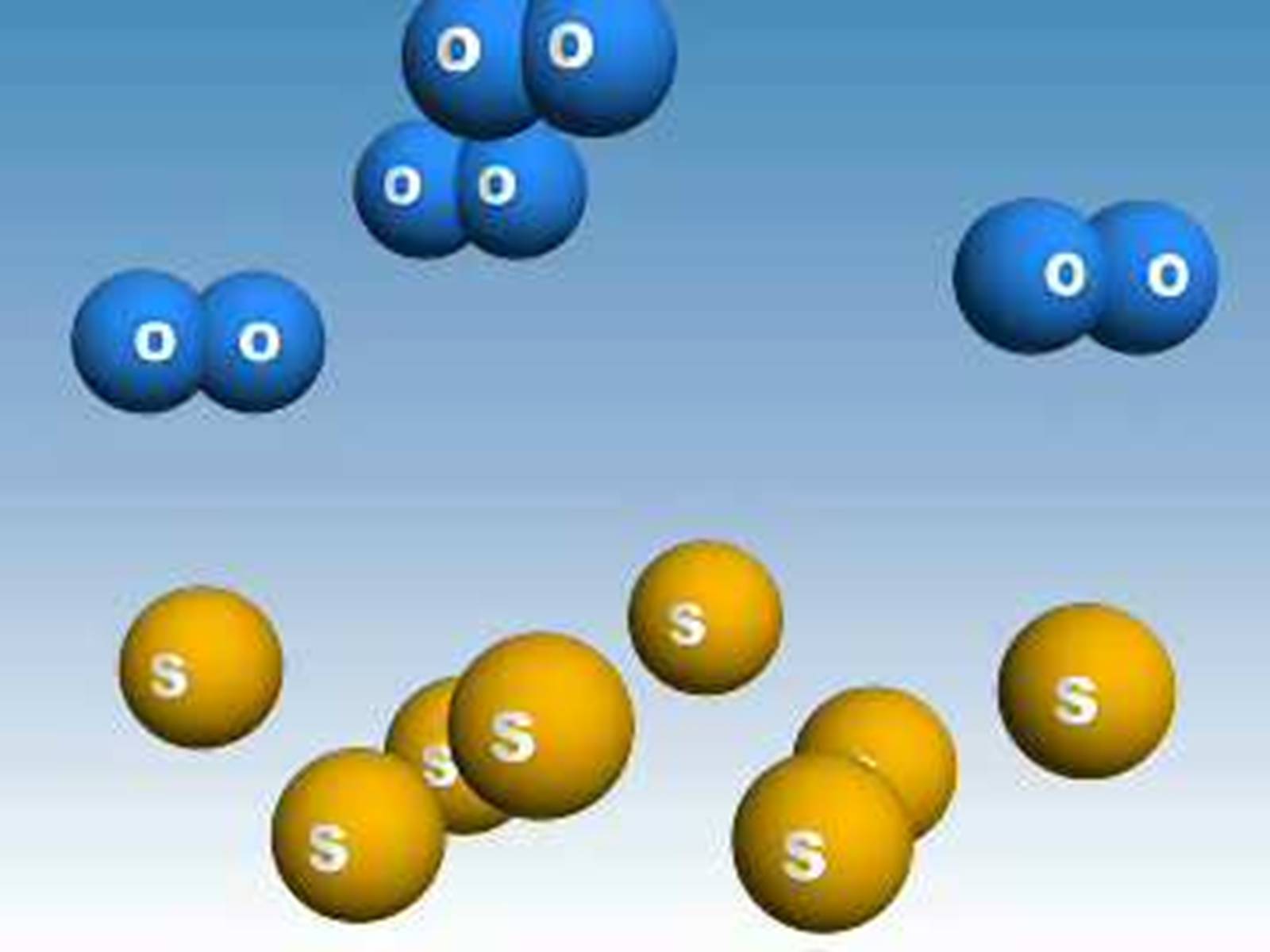
Молекула – найменша частинка речовини, що складається з двох і більшої кількості хімічно зв'язаних атомів і яка здатна до самостійного існування.
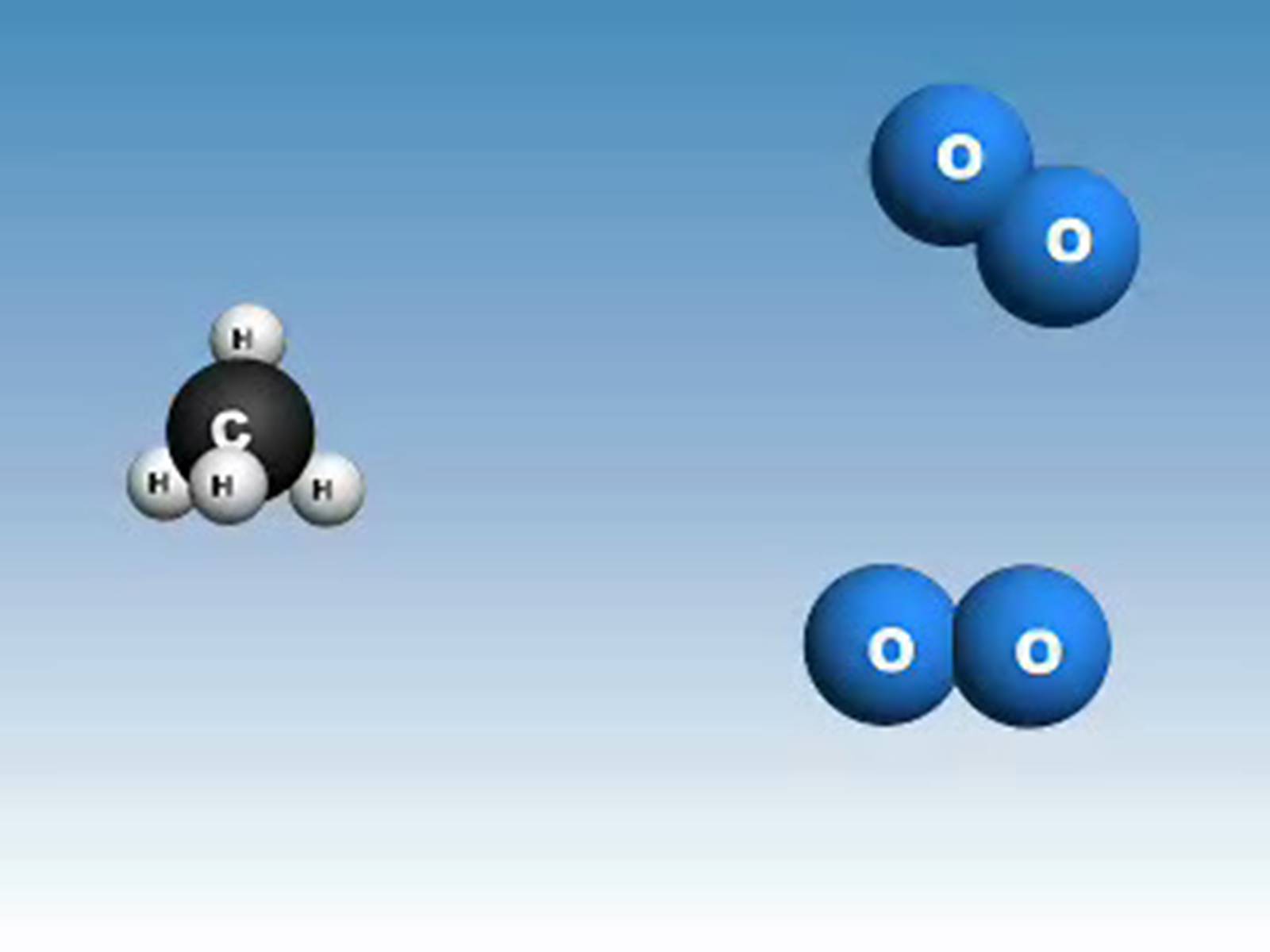
Молекула – найменша частинка речовини, що складається з двох і більшої кількості хімічно зв'язаних атомів і яка здатна до самостійного існування.

Так, вода, вуглекислий газ, кисень, озон, спирт, крохмаль – речовини молекулярної будови.
Молекули – це їхні структурні частинки.

Інші речовини, наприклад алмаз, графіт, кремнезем (річковий пісок), усі метали, складаються з атомів.
Атоми – це їхні структурні частинки.

Атом – найдрібніша частинка речовини, що складається з позитивно зарядженого ядра і негативно заряджених електронів.

Ядро атома містить елементарні частинки – протони та нетрони.
Протони мають заряд +, тому ядро завжди позитивно заряджене.
Заряд електрона становить –.
В атомі сумарний заряд протонів дорівнює сумарному заряду електронів, тому атом електронейтральний.
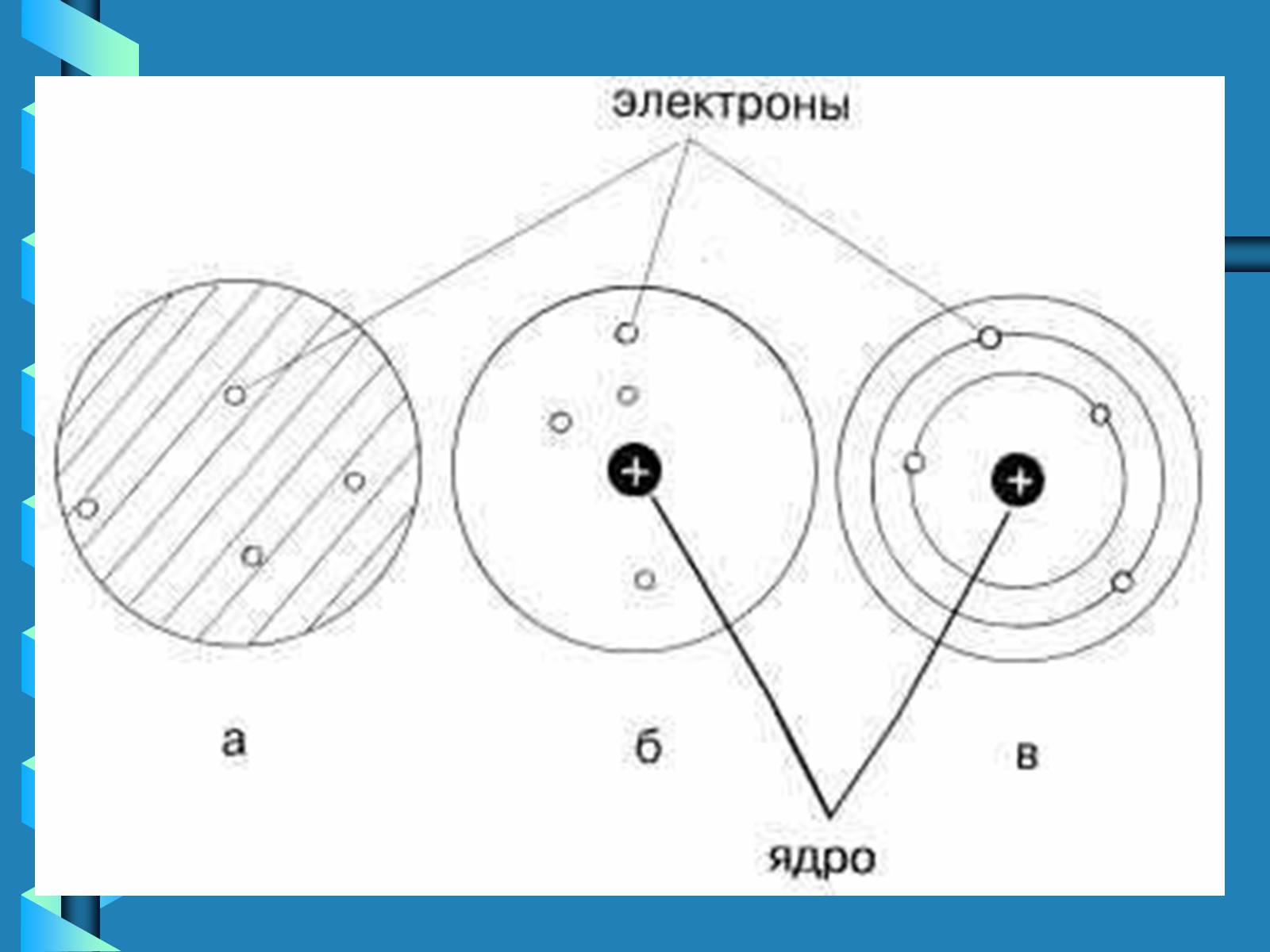
Ядро атома містить елементарні частинки – протони та нетрони.
Протони мають заряд +, тому ядро завжди позитивно заряджене.
Заряд електрона становить –.
В атомі сумарний заряд протонів дорівнює сумарному заряду електронів, тому атом електронейтральний.

Але в навколишньому світі електронейтральних атомів дуже мало,
це, наприклад, атоми Гелію, Неону, Аргону тощо.
Схематичне зображення атома гелію з електронною хмарою навколо і складним за будовою ядром

Частіше атоми або втрачають, або приєднують електрони і стають зарядженими частинками – йонами.
Наприклад, натрій хлорид (кухонна сіль) складається з йонів Натрію і йонів Хлору.

Частіше атоми або втрачають, або приєднують електрони і стають зарядженими частинками – йонами.
Наприклад, натрій хлорид (кухонна сіль) складається з йонів Натрію і йонів Хлору.

Основні положення Атомно-молекулярного вчення
1. Існують речовини з молекулярною і немолекулярное будовою.
2. Між молекулами є проміжки, розміри яких залежать від агрегатного стану речовини. Найбільші відстані між молекулами газів, найменші в твердих речовинах.
3. Атоми одного елемента відрізняються від атомів інших елементів масою, розмірами і властивостями.
4. Молекули і складаються з них атоми знаходяться в безперервному русі. Підтвердженням цього положення можуть служити процеси розповсюдження запахів (дифузія), випаровування рідин.
5. При фізичних явищах молекули зберігаються, а при хімічних руйнуються, атоми перегруповуються і утворюють нові молекули.

Нині відомо понад 110 видів різних атомів, з них 90 зустрічаються в природі і 20 – добуті штучно.
Вид атомів з певним зарядом ядра називають хімічним елементом.

Усі відомі нині речовини, а їх вже понад 15 000 000, утворені з'єднанням атомів різних хімічних елементів.
У цій безлічі речовин неможливо було б орієнтуватися, якби не було прекрасного винаходу, що нагадує азбуку.
За пропозицією шведського хіміка Й. Берцеліуса хімічні елементи почали позначати однією або двома літерами їх латинської назви.
Наприклад, Оксиген позначається літерою О від Oxygenium (Оксігеніум), Сульфур S від Sulfur, Ферум – Fe від Ferrum тощо.

Назви елементів мають різне походження:
за властивостями елементів (водень - породжує воду);
на честь планет (селен - місяць);
з міфології (Тантал, Титан);
від географічних назв (рутеній - латинська назва Росії);
на честь учених (Менделєвій - Менделєєв).

Такою хімічною символікою користуються з 1814 р. й досі.
Твоє завдання полягає в тім, щоб поступово запам'ятати символи найважливіших хімічних елементів, навчитися їх писати, вимовляти й розуміти, що вони позначають.
Зверни увагу: назви хімічних елементів пишуться з великої літери.

Усі хімічні елементи за властивостями поділяють на метали й неметали.
До елементів - металів належать Алюміній Al, Натрій Na, Магній Mg тощо,
до елементів-неметалів – Оксиген О, Хлор Сl, Фосфор Р тощо.
Така класифікація дещо умовна, оскільки між елементами-металами і елементами-неметалами не можна провести чіткої межі, проте вона широко використовується.

Поширення хімічних елементів у природі
Всі хімічні елементи утворилися внаслідок складних процесів ядерного синтезу в зірках і в космічному просторі.
Є багато теорій, що пояснюють походження хімічних елементів та особливості їх розповсюдження на Землі і в Космосі (ми їх не розглядаємо).

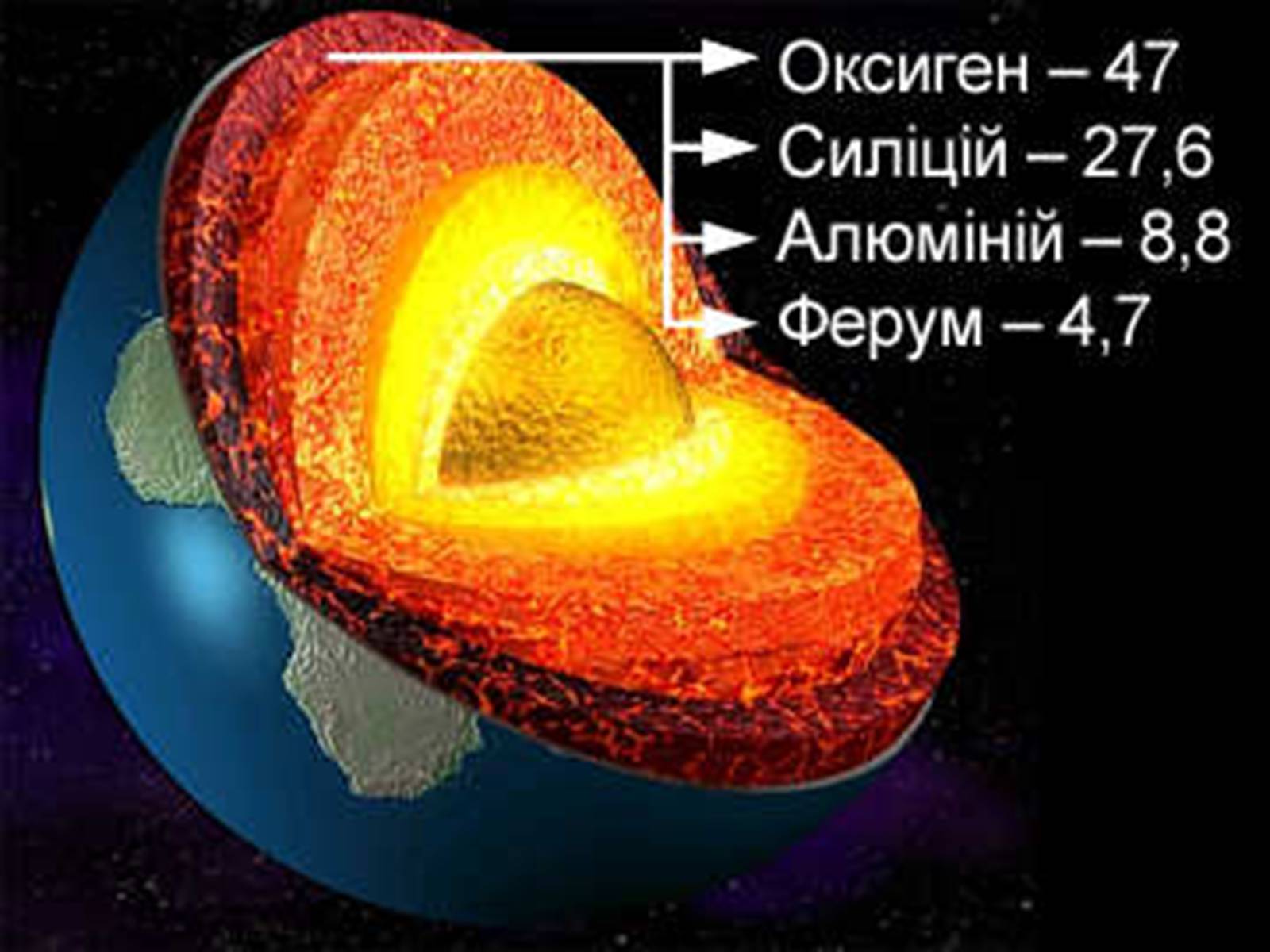
На Землі найпоширенішим є Оксиген О (47% від маси земної кори),
за ним ідуть Силіцій Si (27,6%),
Алюміній Al (8,8%),
Ферум Fe (4,65%).
Ці елементи разом із Кальцієм Са, Натрієм Na, Калієм К і Магнієм Mg складають понад 99% маси земної кори .
На Землі найпоширенішим є Оксиген О (47% від маси земної кори),
за ним ідуть Силіцій Si (27,6%),
Алюміній Al (8,8%),
Ферум Fe (4,65%).
Ці елементи разом із Кальцієм Са, Натрієм Na, Калієм К і Магнієм Mg складають понад 99% маси земної кори .

Висновки
Речовини бувають молекулярної і немолекулярної – атомної або йонної – будови.
Атоми певного виду з однаковим зарядом ядра і є хімічним елементом.
Уся різноманітність речовин утворилася внаслідок комбінації хімічних елементів.
