Презентація на тему «Будова електронних оболонок атомів»

Будова електронних оболонок атомів. Енергетичні рівні й підрівні
1

Цілі уроку
Розширити уявлення про будову атомів;
Навчити складати електронні формули, схеми розподілу електронів по квантових комірках для елементів І-ІІІ періодів;
Формувати вміння визначати електронну будову атома за його положенням у періодичній системі.
2

Хімічний бліц-турнір
Як визначити кількість елекронів у атомі?
Чому атоми електронейтральні?
Що таке орбіталь?
Які форми може мати електронна хмарина?
Яка максимальна кількість електронів може перебувати на s-орбіталі, p-орбіталі, d-орбіталі, f-орбіталі?
Яка кількість енергетичних рівнів може бути в атомі?
Як визначити кількість енергетичних рівнів у атомі?
Як визначити кількість електронів на зовнішньому енергетичному рівні?
Як розподіляються електрони по енергетичним рівням?
3
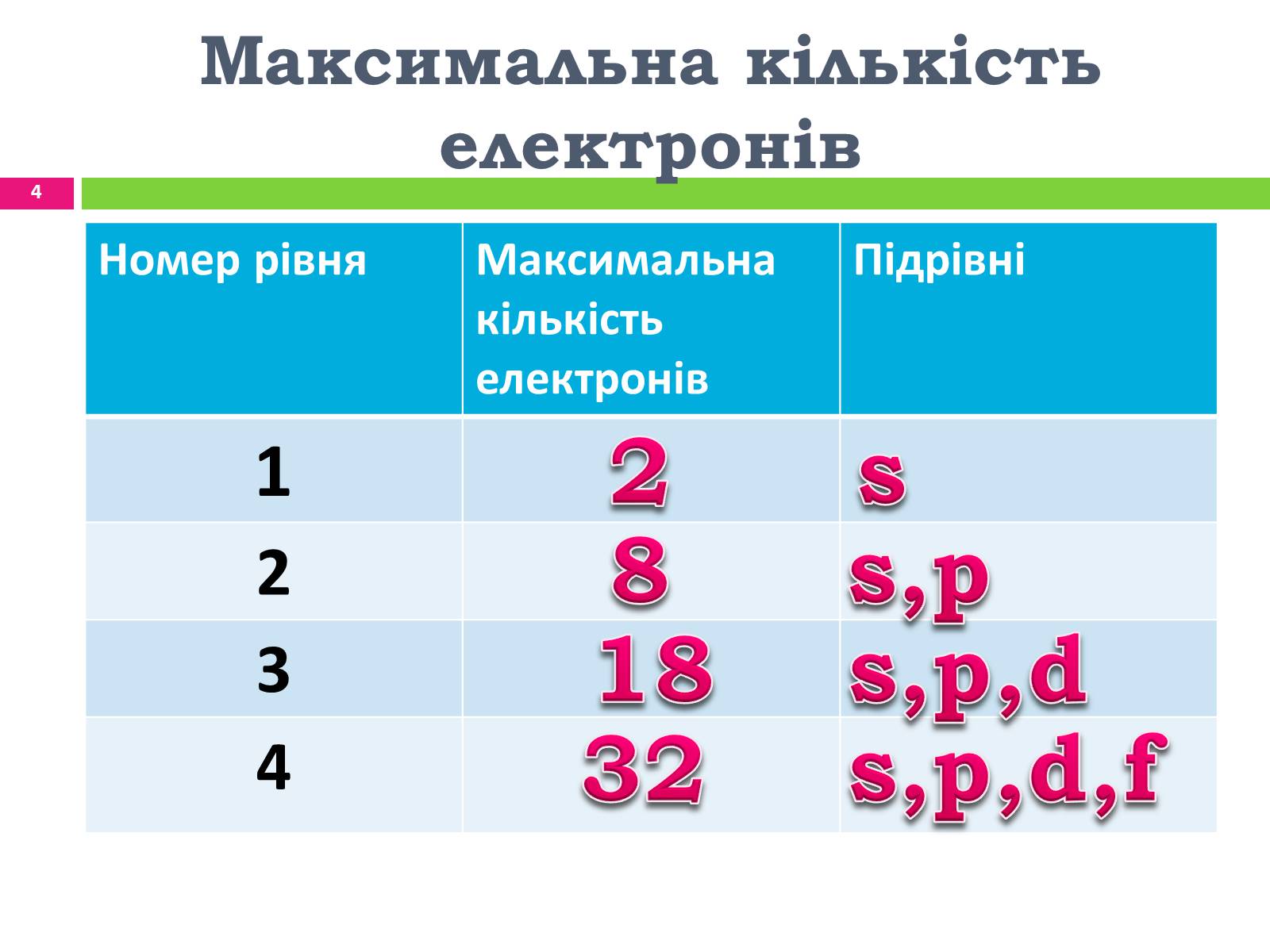
Максимальна кількість електронів
Номер рівня
Максимальна кількість електронів
Підрівні
1
2
3
4
2
8
18
32
s
s,p
s,p,d
s,p,d,f
4

Практика
Побудуймо схему будови атома Гідрогену Н, запишіть електронну формулу, розподіл електронів по квантових комірках
Н +1)1 1s
Побудуйте схему будови атома Гелію Не, запишіть електронну формулу, розподіл електронів по квантових комірках
He +2)2 1s
1
1
1
4
2
2
5

Ключові моменти
Загальне число електронів у атомі дорівнює номеру елемента в періодичній системі хімічних елементів;
Число енергетичних рівнів у атомі дорівнює номеру періоду, в якому знаходиться елемент;
Число електронів на зовнішньому енергетичному рівні дорівнює номеру групи, в якому знаходиться хімічний елемент;
В атомі не можу бути двох однакових електронів.
6

Керована практика
Побудувати схему будови атомів, електронну формулу та розподіл електронів по квантових комірках для таких елементів
Літію, Берилію, Бору, Карбону
Нітрогену, Оксигену, Флуору, Неону.
7