Презентація на тему «Тепловий ефект реакції. Екзотермічні та ендотермічні реакції»

Презентація з хімії
.
На тему : « Тепловий ефект реакції. Екзотермічні та ендотермічні реакції » .
Підготували : Лисенко А.
Гунько А.
Медина В.

Пригадаємо!
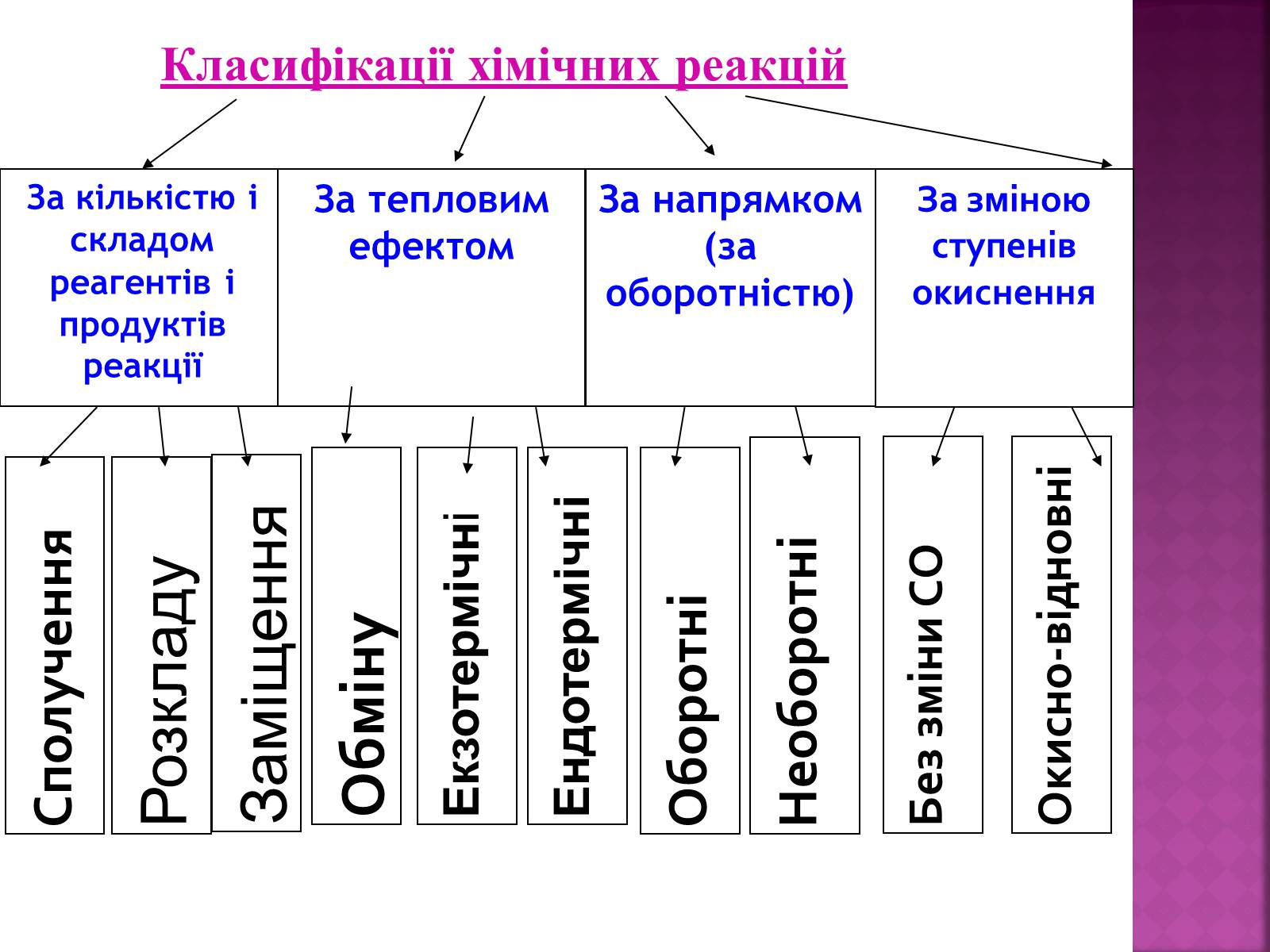
За кількістю і складом реагентів і продуктів реакції
За тепловим ефектом
За напрямком
(за оборотністю)
За зміною ступенів окиснення
Розкладу
Заміщення
Обміну
Сполучення
Екзотермічні
Ендотермічні
Оборотні
Необоротні
Без зміни СО
Окисно-відновні
Класифікації хімічних реакцій

Мета уроку:
• познайомитися з класифікацією реакцій за тепловим ефектом: з екзотермічними і ендотермічними реакціями; • знати визначення тепловому ефекту, екзо- і ендотермічним реакціям; • розрізняти екзо- і ендотермічні реакції;

Тепловий ефект реакції – кількість теплоти, що виділяється чи поглинається під час хімічних реакції.
Тепловий ефект позначається:
а) Q – показує скільки теплоти (в кДж) виділилося або поглинулося під час реакції;
б) ∆ Н – показує різницю між вмістом енергії у вихідних речовинах і кінцевих продуктах
(ентальпія)
∆ Н = - Q
Тепловий ефект вимірюється в Дж або в кДж

Екзотермічна реакція - хімічна реакція, яка супроводжується виділенням тепла (наприклад, горіння).
Приклад :

Ендотермічна реакція-хімічна реакція, що супроводиться поглинанням теплоти.
Приклад :

Закріпи свої знання!

1). Що таке екзотермічна реакція ?
2). Що таке ендотермічна реакція?
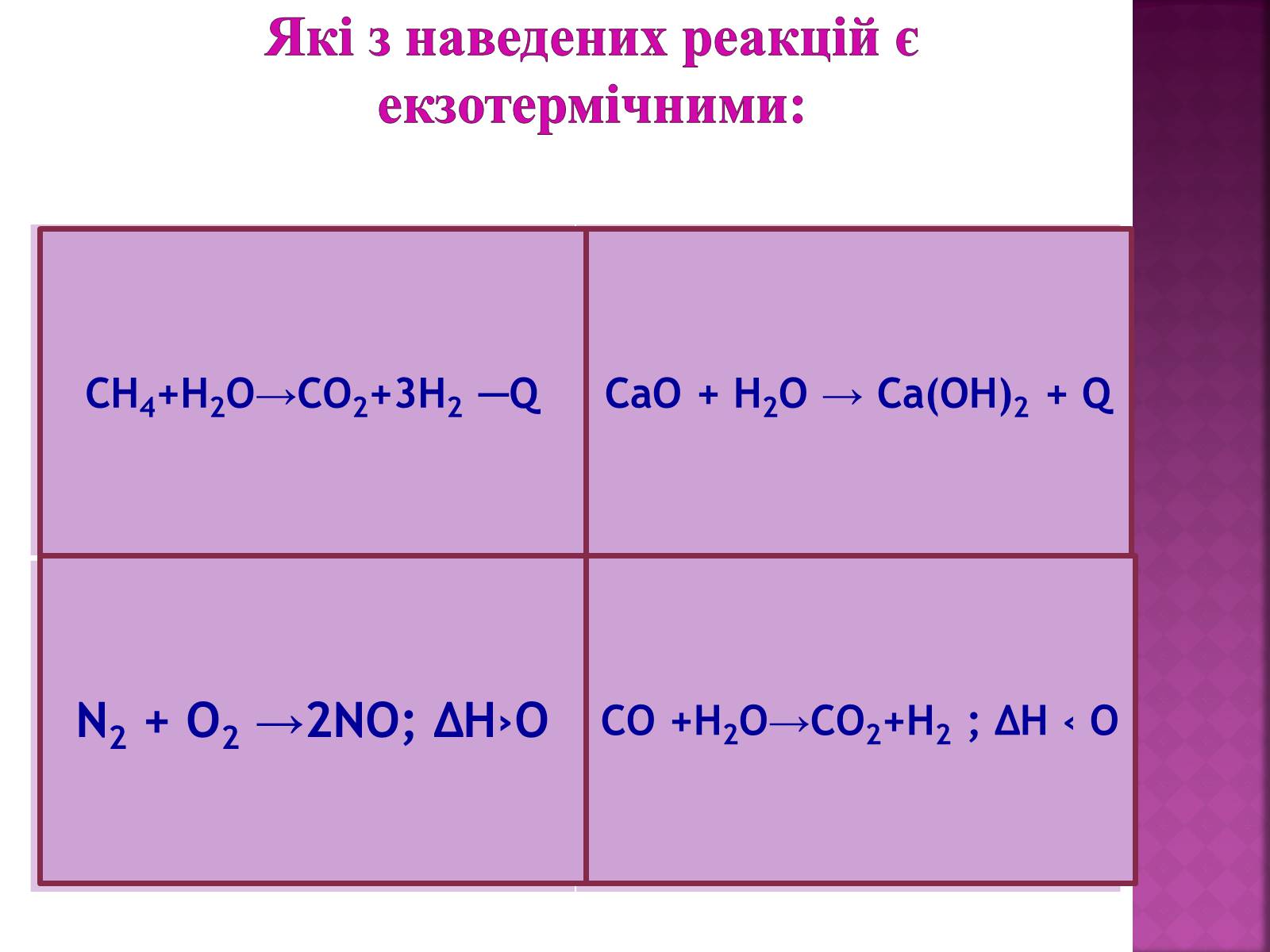
Які з наведених реакцій є екзотермічними:
Невірно!
Молодець!
Невірно!
Молодець!
СН4+Н2О→СО2+3Н2 ─Q
N2 + O2 →2NO; ∆Н›О
СаО + Н2О → Са(ОН)2 + Q
СО +Н2О→СО2+Н2 ; ∆Н ‹ О

До ендотермічних реакцій належать :
А )
Б )

Дякуємо за увагу!