Презентація на тему «Хімічні властивості алканів»

Яке явище небезпечне для життя?

Хімічні властивості алканів
Урок в 9 класі
КЗ Верхівцевського НВК
Учитель Кукса Н.М.

Тест – есе
Закінчіть речення.
Сполуки Карбону з Гідрогеном називаються…
Вуглеводні, що мають у своєму складі прості одинарні зв'язки, називаються…
Сполуки, які різняться на групу СН2 і мають подібну будову і подібні властивості, називаються…
Сполуки, які мають однаковий склад, але відрізняються за будовою та властивостями, називаються…
Відстань між атомами Карбону в молекулах алканів становить…
Алкани мають такі фізичні властивості :…

1.Ознайомитися з хімічними властивостями метану;
2.Навчитися складати рівняння реакцій;
3.Дізнатися про значення метану в промисловості,та знаходженні його в природі.
4.Для чого метан потрібен у побуті.
Цілі уроку:

Хімічні властивості алканів
За н.у. алкани досить інертні:
не реагують з лугами і кислотами;
не окиснюються перманганатом калію (KMnO4)
не знебарвлюють бромну воду (Вr2)
У ХІХ ст. алкани називали «хімічними мерцями»

2. Горіння – повне окиснення
СН4 + 2О2 →СО2 + 2Н2О; ∆Н = 890 кДж/моль
Суміш СН4 і О2 дуже вибухонебезпечна. Спричинює аварії в шахтах, може статися вибух в приміщенні.
Запишіть рівняння горіння етану .

За допомогою реакції горіння парафіну, можна визначити якісний склад алканів
Парафін
Безводний купрум(ІІ) сульфат СuSO4
Вапняна вода Ca(OH)2
1
2
3

3. Термічний розклад
t›1000°C
а) СН4 → С + 2Н2
t=400°C
б) 2СН4 → С2Н2 + 3Н2
Запишіть рівняння повного термічного розкладу етану .
Н2 – для добування НСl , NH3
С – для добування гуми і фарб
NH3
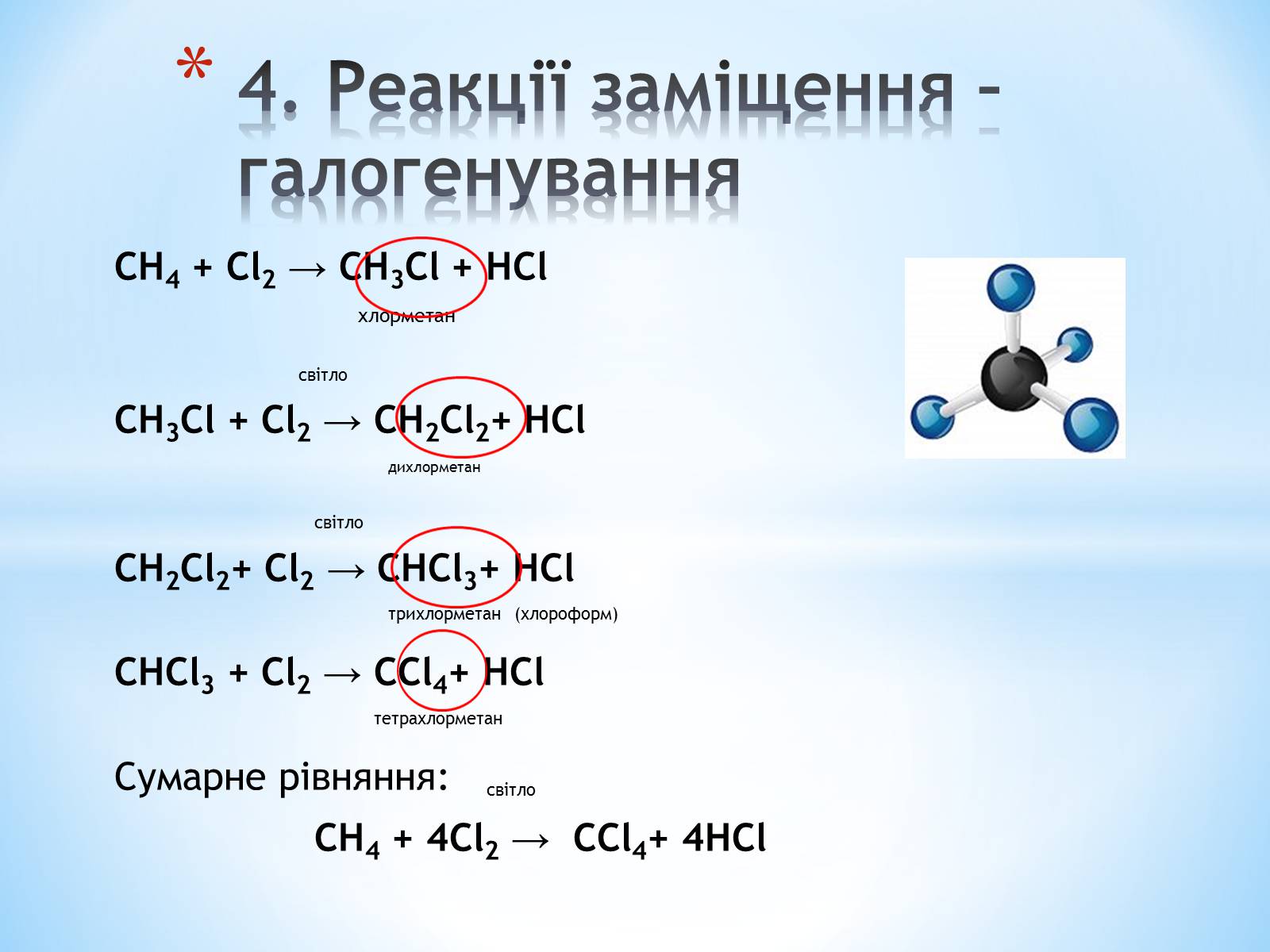
СН4 + Cl2 → CH3Cl + HCl
хлорметан
світло
CH3Cl + Cl2 → CH2Cl2+ HCl
дихлорметан
світло
CH2Cl2+ Cl2 → CHCl3+ HCl
трихлорметан (хлороформ)
CHCl3 + Cl2 → CCl4+ HCl
тетрахлорметан
Сумарне рівняння: світло
СН4 + 4Cl2 → CCl4+ 4HCl
4. Реакції заміщення – галогенування

Це цікаво!
CH3Cl
Використовують в холодильних установках, в медицині для місцевої анестезії, в органічному синтезі
CH2Cl2
розчинник
CHCl3
розчинник, анестезуюча дія, раніше
використовували в медицині для знеболювання
CCl4
розчинник, протипожежний засіб, але не в закритих приміщення. Оскільки утворюється отруйний фосген СОСl2

Запишіть рівняння галогенування етану
C2H5Cl – застосовують в медицині для швидкого охолодження шкіри і м'язів при вивихах і розтягненнях
Усі продукти хлорування алканів токсичні й руйнують озоновий шар.
C2H6 + Cl2 =C2H5Cl + HCl

До складу феромонів тварин входять деякі вищі алкани. Запах феромонів приваблює комах або їх відлякує.
Насичені вуглеводні, які виробляють квітки орхідеї, виконують функцію приваблювання комах.
Феромон тривоги в мурашок-древоточців містить насичений вуглеводень декан.

На поверхні фруктів воскоподібна плівка містить гомологи метану.

Застосування
Парафін
(С18 – С35) – використовує- ться в медицині (парафінотерапія)

Вазелінова олія
(до С25) - використовують у медицині, парфумерії, косметології

Спрей-заморозку «Doc Sprt» використовують для швидкого охолодження шкіри і м'язів при вивихах і розтягненнях. Містить зріджені пропан і бутан

Подумай і дай відповідь

Виберіть реакції, характерні для алканів:
Повне окиснення;
Каталітичне приєднання водню;
Приєднання брому;
Окиснення розчином калій перманганату;
Заміщення за участю хлору;
Термічний розклад.
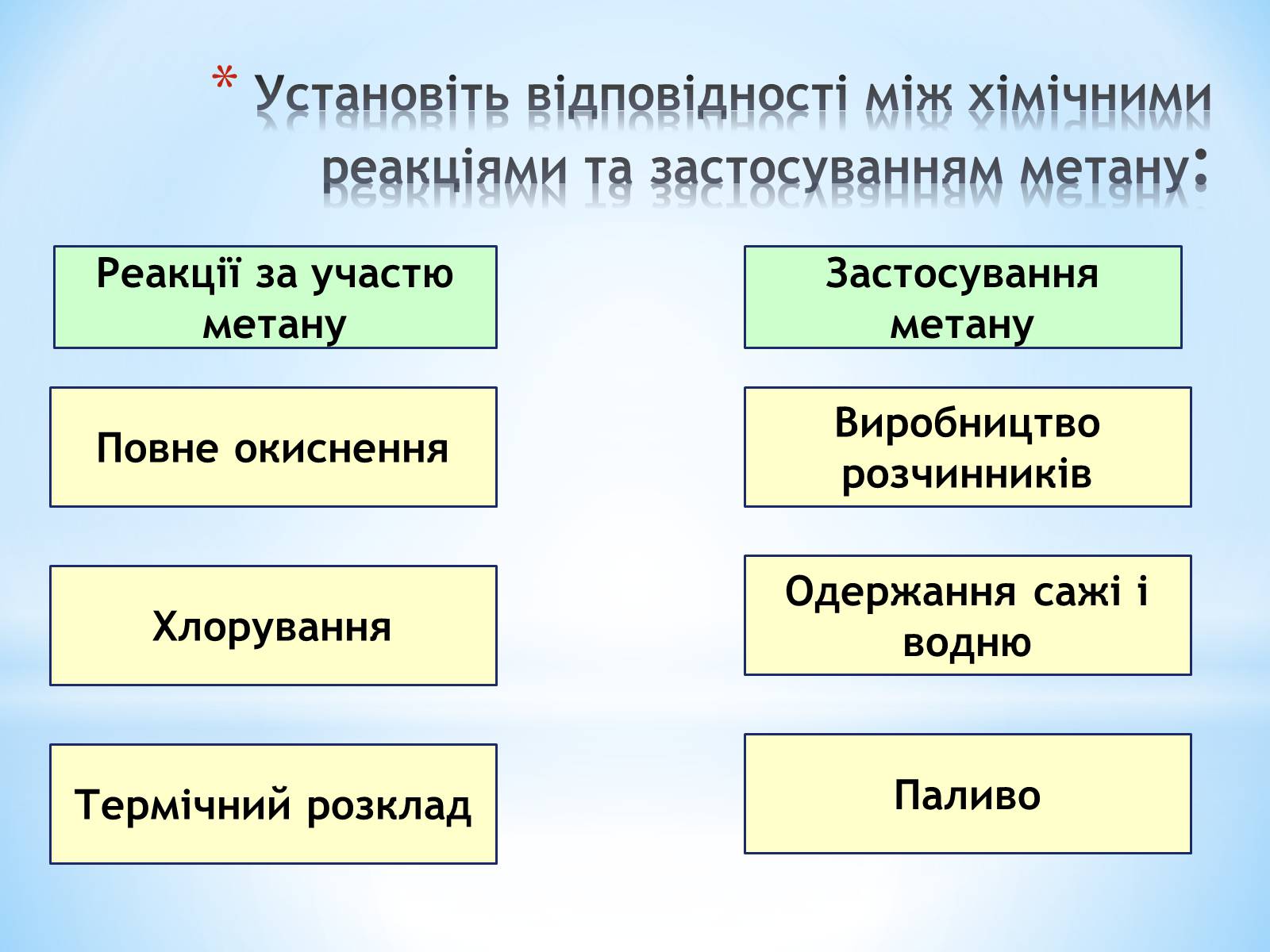
Установіть відповідності між хімічними реакціями та застосуванням метану:
Повне окиснення
Застосування метану
Реакції за участю метану
Термічний розклад
Паливо
Одержання сажі і водню
Виробництво розчинників
Хлорування
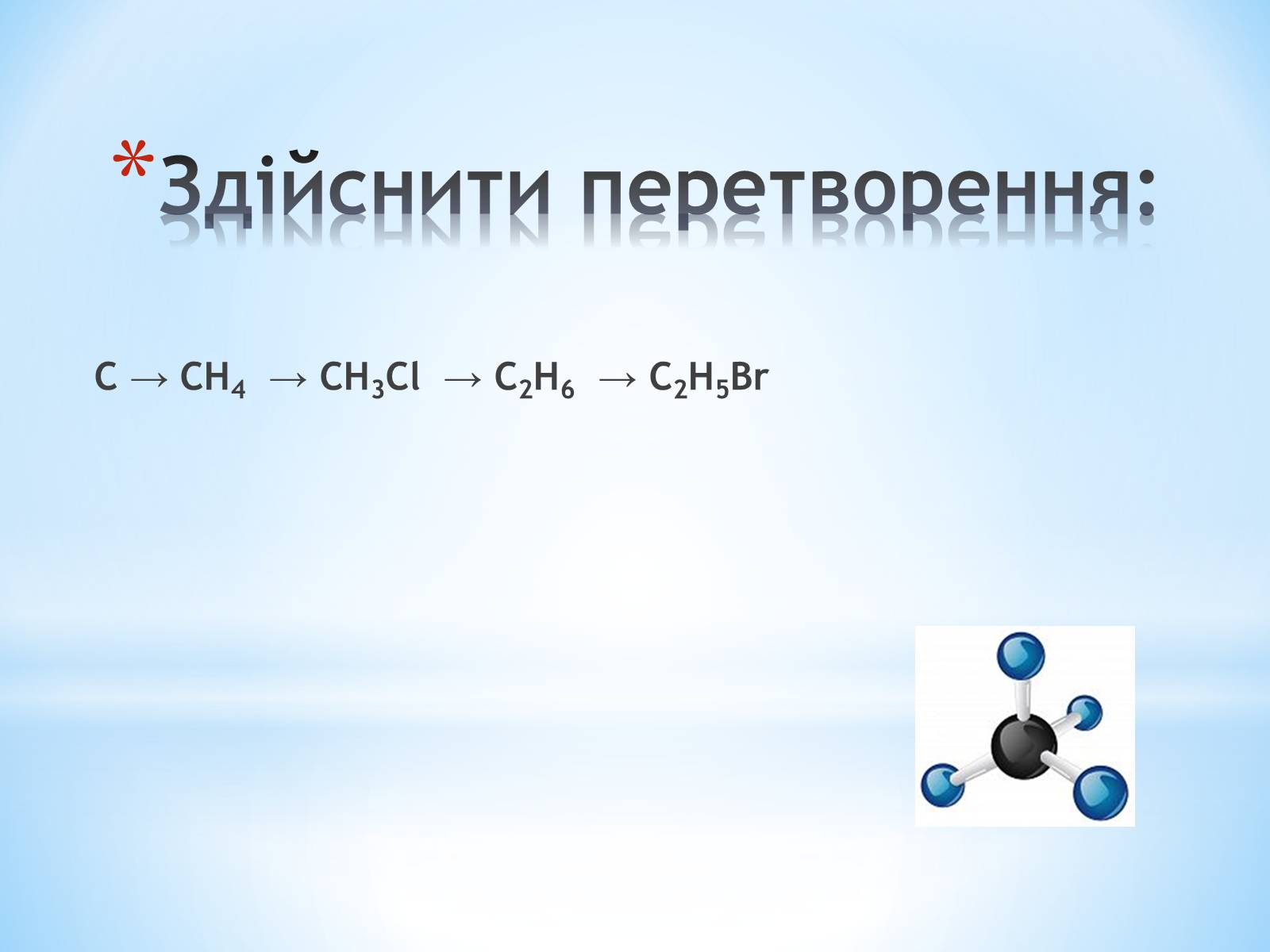
Здійснити перетворення:
С → СН4 → СН3Cl → C2H6 → C2H5Br

Задача.
Обчисліть, який об'єм карбон (ІV) оксиду утвориться внаслідок згоряння пропану об'ємом 15л.

Продовжіть ланцюжок:
Я знаю …..
Я вмію …..
Я використовую ……
Мені це буде необхідно для …..
Я навчився ……
Я набув вміння …….

Домашнє завдання
§20,
Впр. 7,10,додадково 13