Презентація на тему «Використання правильних многогранників в структурі речовин»

Використання правильних многогранників в структурі речовин
Презентацію підготувала
учениця 11-А класу
Трачук Олеся

Молекули більшості хімічних речовин мають закономірну геометричну структуру. Як правило, ці молекули можна зобразити так, що атоми розташовуються у вершинах або в центрі гранних геометричних тіл. Наприклад, структуру метану СН4 можна зобразити, використовуючи тетраедр. Атоми водню розташовують у вершинах, а атом вуглецю - в центрі тетраедра.
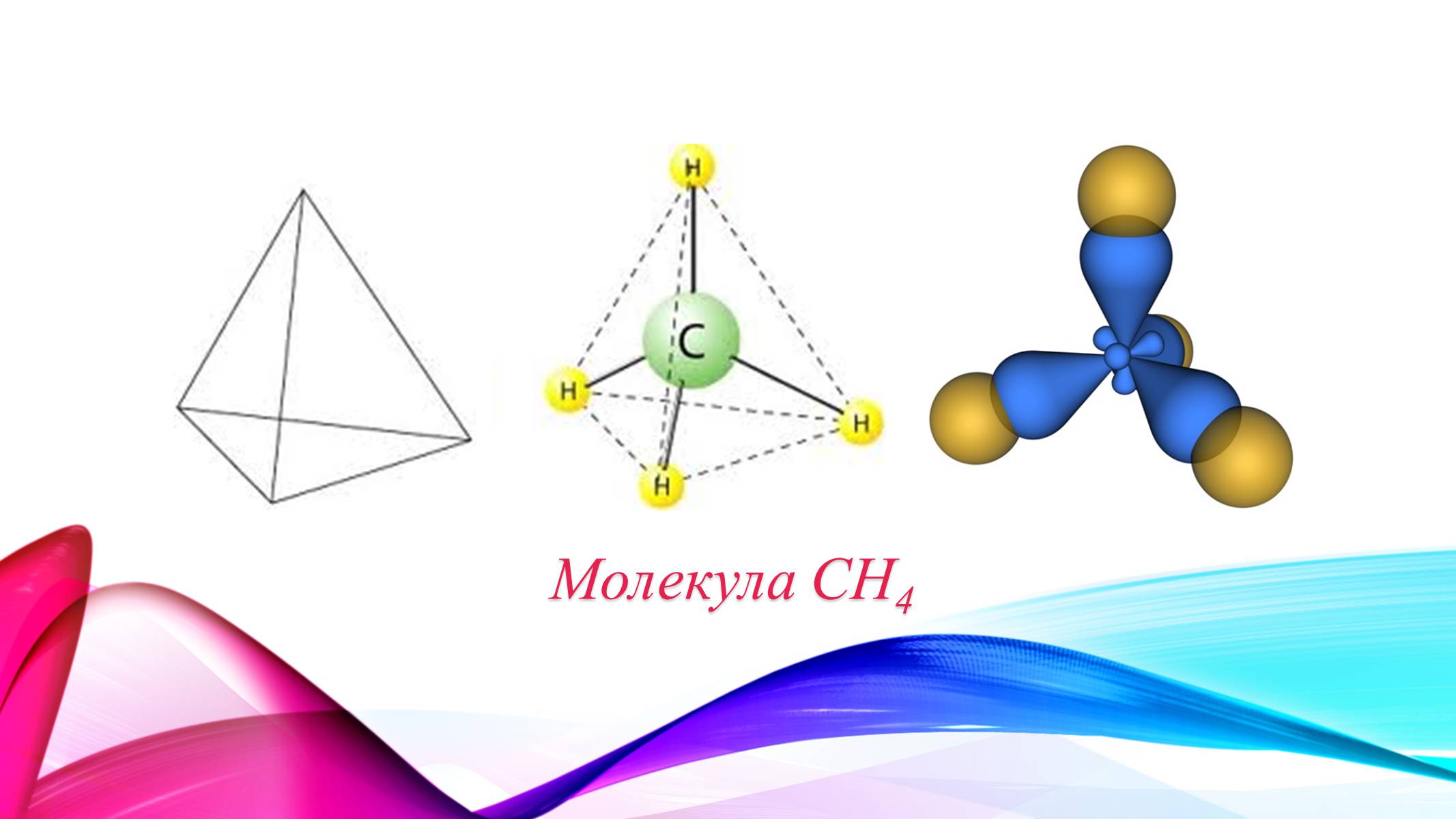
Молекула CH4

Структура етану C2H6 зображується за допомогою іншого геометричного тіла - прізматоїда. Прізматоїд являє собою гранне геометричне тіло, всі грані якого трикутники. Причому, основи прізматоїда є рівносторонніми трикутниками. Останні повернені один відносно одного так, що є обернено симетричними. Бічні грані - рівнобедренні трикутники. Атоми водню розташовують у вершинах прізматоїда.
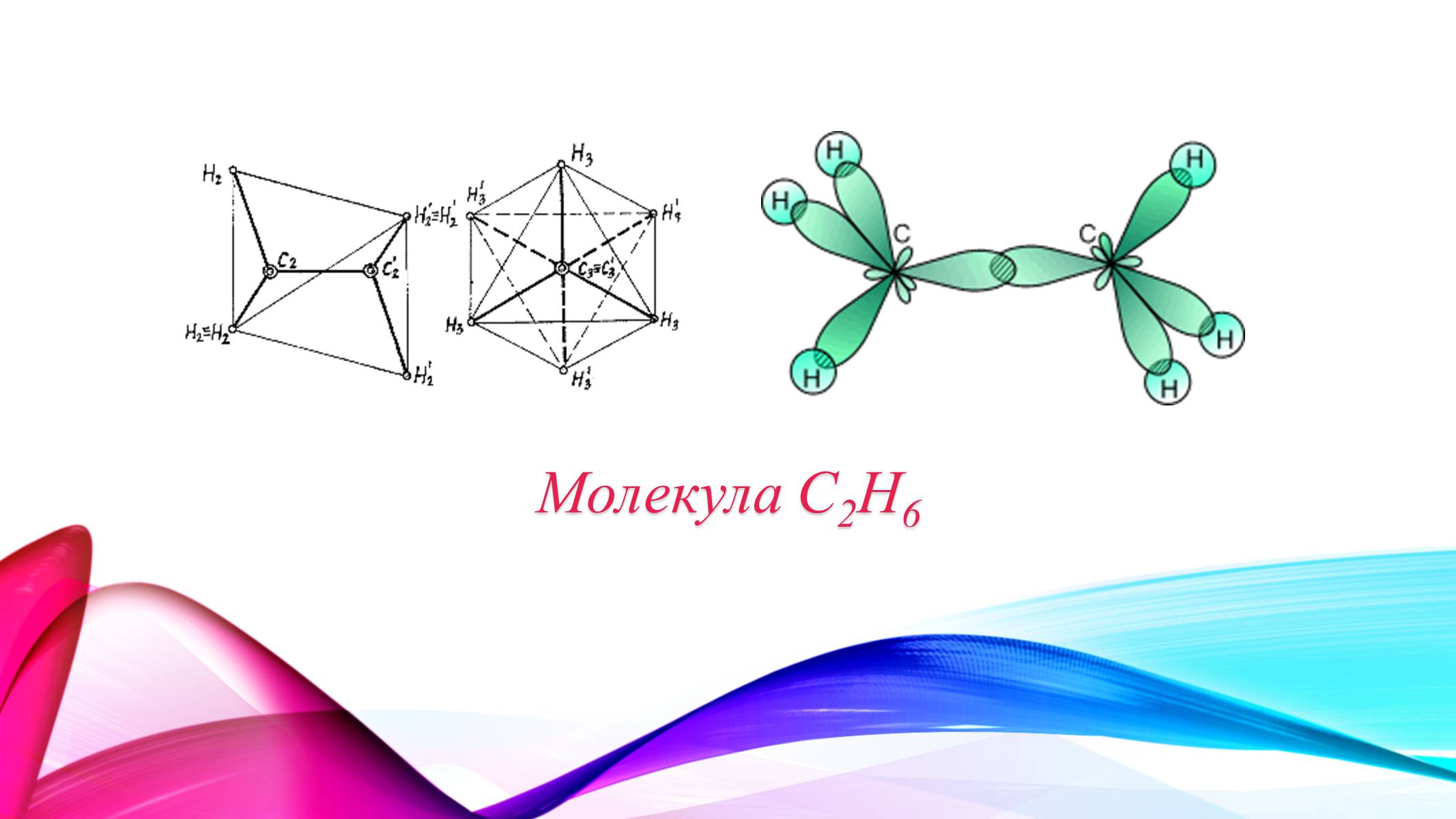
Молекула C2H6

Багато комплексних сполук можна зобразити графічно за допомогою правильних багатогранників. У Fе(СN)6. Іони CN розташовані в вершинах, а іон заліза - в центрі октаедра. Деякі кристалічні речовини мають гексагональну структуру.
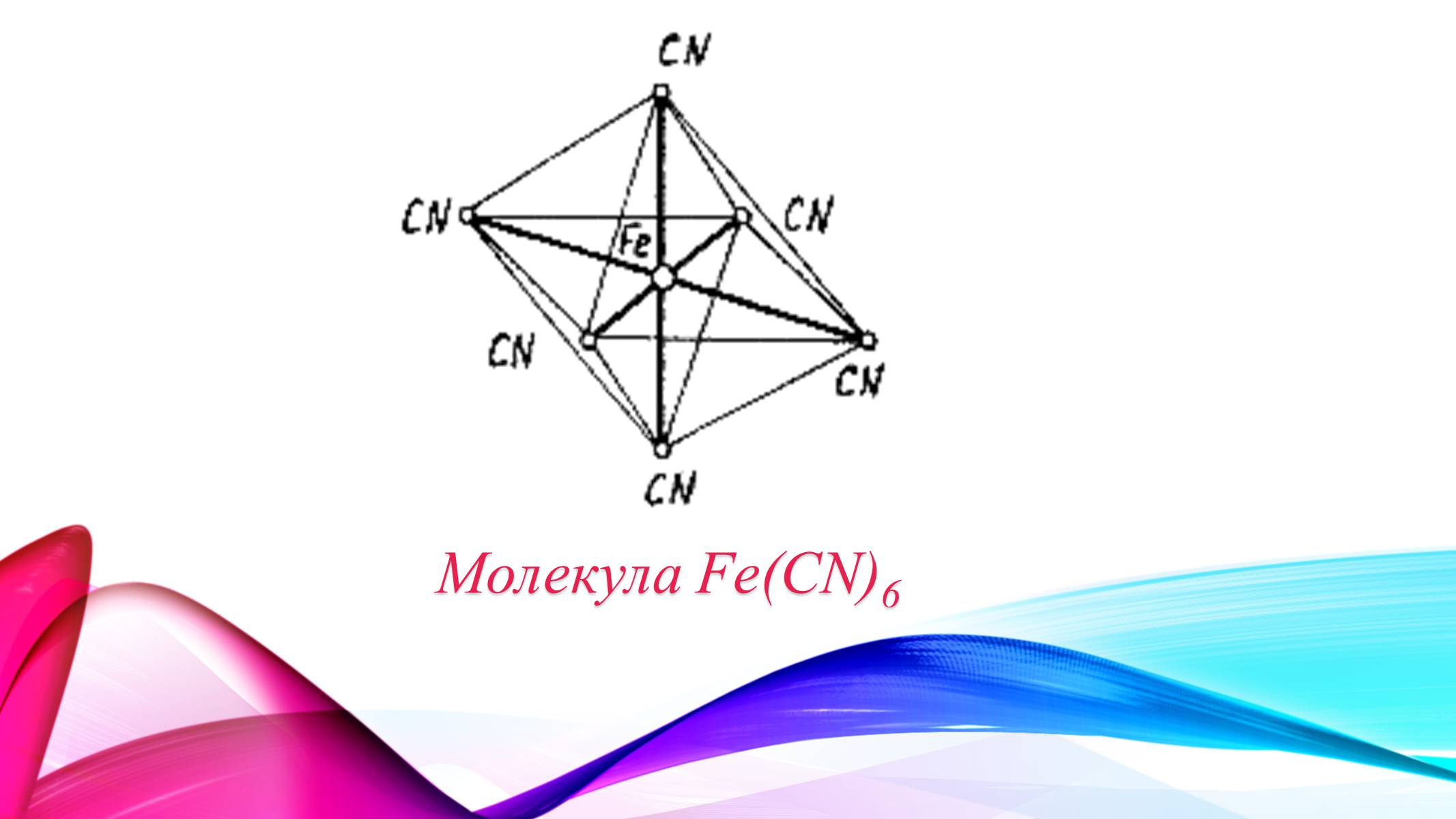
Молекула Fe(CN)6
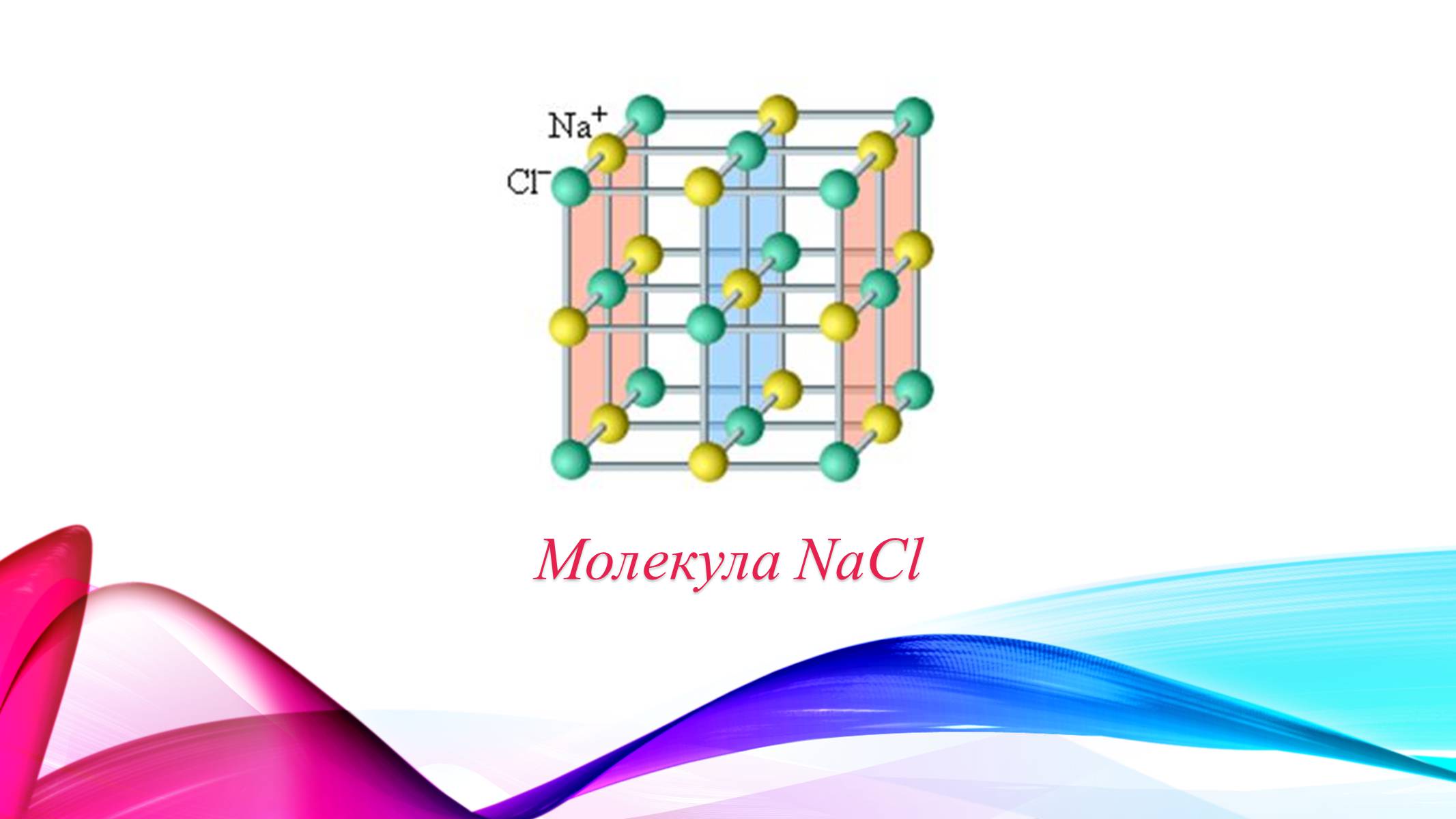
Молекула NaCl
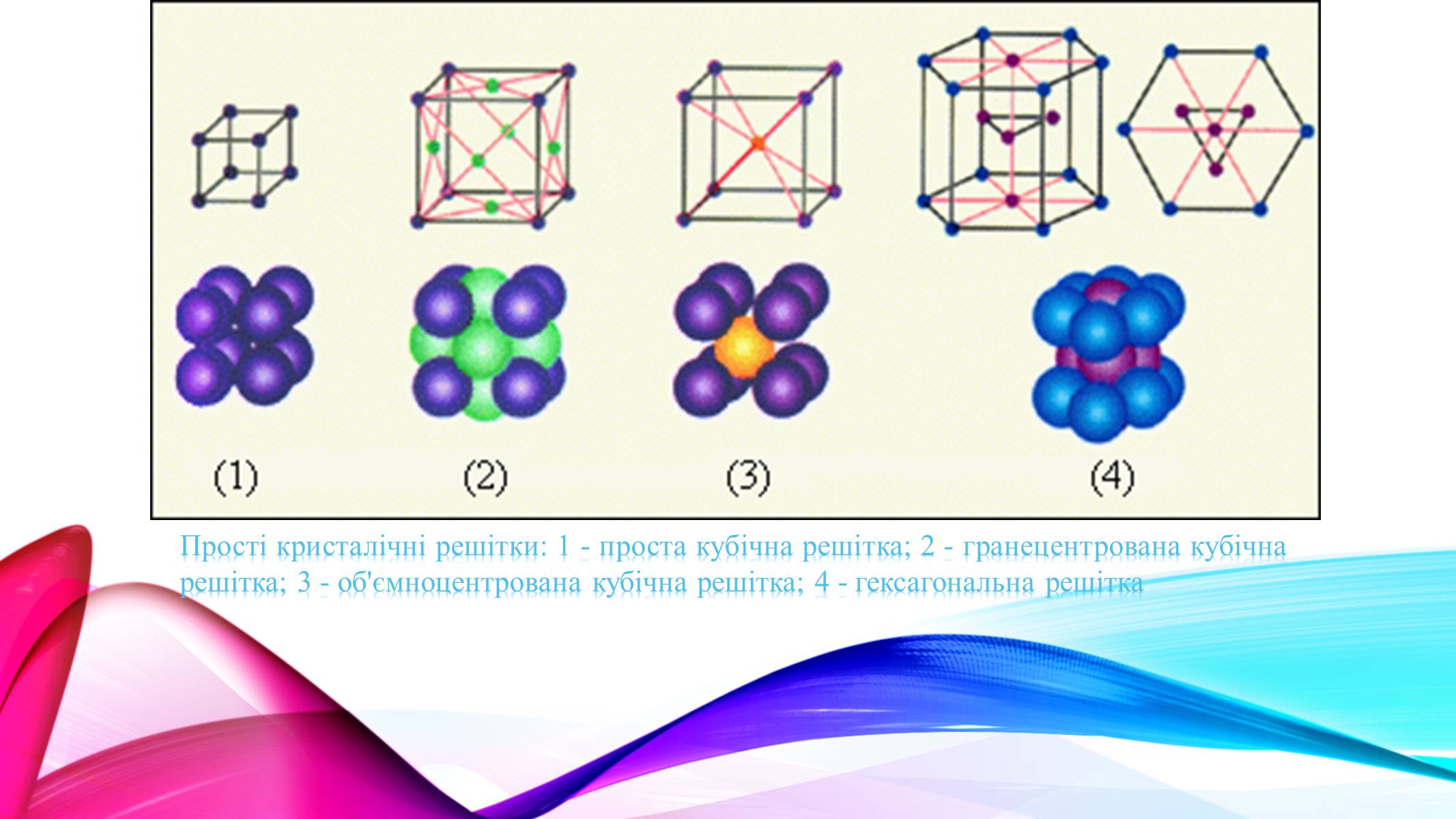
Прості кристалічні решітки: 1 - проста кубічна решітка; 2 - гранецентрована кубічна решітка; 3 - об'ємноцентрована кубічна решітка; 4 - гексагональна решітка

Дякую за увагу!