Презентація на тему «Фосфор» (варіант 1)

Фосфор
Характеристика елемента та утворених ним сполук, кругообіг елемента в природі

Періодична система хімічних елементів Д.І.Менделєєва
Періоди
1
2
3
4
5
6
7
Ряди
1
2
3
4
10
9
8
7
5
6
Групи елементів
I
II
VI
V
VII
III
IV
VIII
Характеристика
1.
Відкрито у 1669 році Хеннінгом Брандтом.
2.
У Періодичній системі знаходиться в 3 періоді, V група, головна підгрупа.
3.
У природі зустрічається тільки у зв'язаному стані.
4.
Утворює кілька простих речовин, які помітно різняться за властивостями: білий, червоний, чорний фосфор.
5.
Е=2,1; найнижчий ступінь окислення –3, найвищий ступінь окислення +5.
31
+15
P

Фосфор
p
31
+15
2
8
5
P = 15
e = 15
N = 16
−
Короткий електронний запис:
1s²
2p⁶
3p
3
2s²
3s²
3d

Хімічні властивості
Для фосфору характерні відновні властивості, які він виявляє у реакціях з неметалами:
4P+3O2 (нестача) 2P2O3
4P+5O2 (надлишок) 2P2O5
2P+5Cl2 (надлишок) 2PCl5
В реакціях з активними металами фосфор виступає в ролі окисника:
3Mg+2P Mg3P.
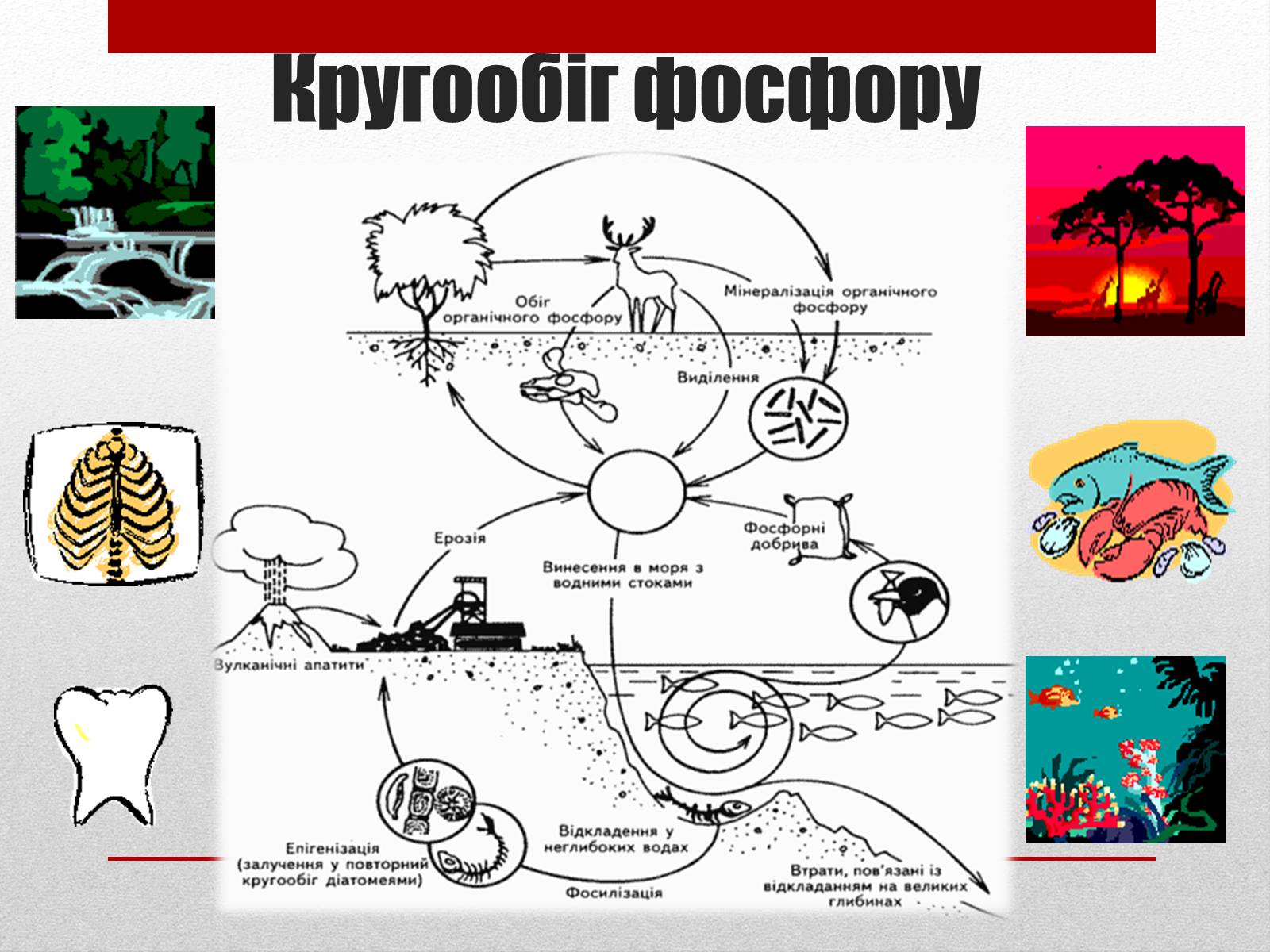
Кругообіг фосфору

Природні сполуки фосфору
фосфати
Ф
О
С
Ф
О
Р
И
Т
и

Діяльність людини порушила
природний кругообіг Фосфору.
Сполуки Фосфору використовуються
для виробництва добрив
та мийних засобів.
Це призводить до забруднення
водойм сполуками Фосфору.
Діяльність людини порушила
природний кругообіг Фосфору.
Сполуки Фосфору використовуються
для виробництва добрив та мийних засобів.
Це призводить до забруднення
водойм сполуками Фосфору.