Презентація на тему «Щелочноземельные металлы»

Вторая группа главная подгруппа наряду с семейством щелочноземельных металлов включает и два типических элемента –бериллий и магний
Щелочноземельные металлы
Be
Mg
Ca
Sr
Ba
Ra
Общая характеристика
Радиус атома
Металлические свойства
n S2
Максимальная степень окисления
+2
Щелочноземельные металлы
Металлы химически активные
Взаимодействуют с водой, кроме бериллия.
Взаимодействуют с водородом с образованием гидридов

Бериллий сходствует с алюминием и магнием…Получил своё название потому, что находится в минерале берилле. Металл называют также глицием от греческого слова «сладкий», потому что соли его имеют сладковатый вкус. Д.И.Менделеев
Бериллий

Распространение в природе
Берилл
3Be * Al2O3 *6SiO2
Хризоберилл
BeAl2O4
Изумруд
Аквамарин
Александрит
аквамарин
александрит
изумруд
Кажется, что если вглядеться в аквамарин, то увидишь тихое море с водой цвета звёзд
К.Г.Паустовский
Такой цвет ему придаёт небольшая примесь двухвалентного железа
«Изумруд капризный, как женщина
Встречается совсем не там, где его ищут»
Благодаря насыщенному зелёному цвету и твёрдости очень популярен у ювелиров, чудесная окраска вызвана наличием ионов хрома или ванадия. Зелёный минерал образует кристаллы в форме шестигранных призм
Александрит впервые найденный на Урале в 1830 году в день совершеннолетия царевича Александра II был назван его именем
Александрит редкий камень. Его производят и искусственным путём, однако идёт он не на продажу, а на использование в аэрокосмической отрасли

В виде простого вещества бериллий получили в 1828году немецкий учёный Фридрих Вёлер и французский химик Антуан Бюсси. Они действовали калием на безводный хлорид бериллия
BeCl2+2K=Be+2KCl
Получение

BeF2+Mg=Be+MgF2 В настоящее время бериллий получают, восстанавливая его фторид магнием, либо электролизом расплава смеси хлоридов бериллия и натрия.
Be
Металл светло-серого цвета, покрытый тончайшей оксидной плёнкой
Тугоплав-
кий металл
t = 1287 C
Уникальное сочетание лёгкости с высокой твёрдостью
Чистый пластичен , но незначительные примеси делают его хрупким
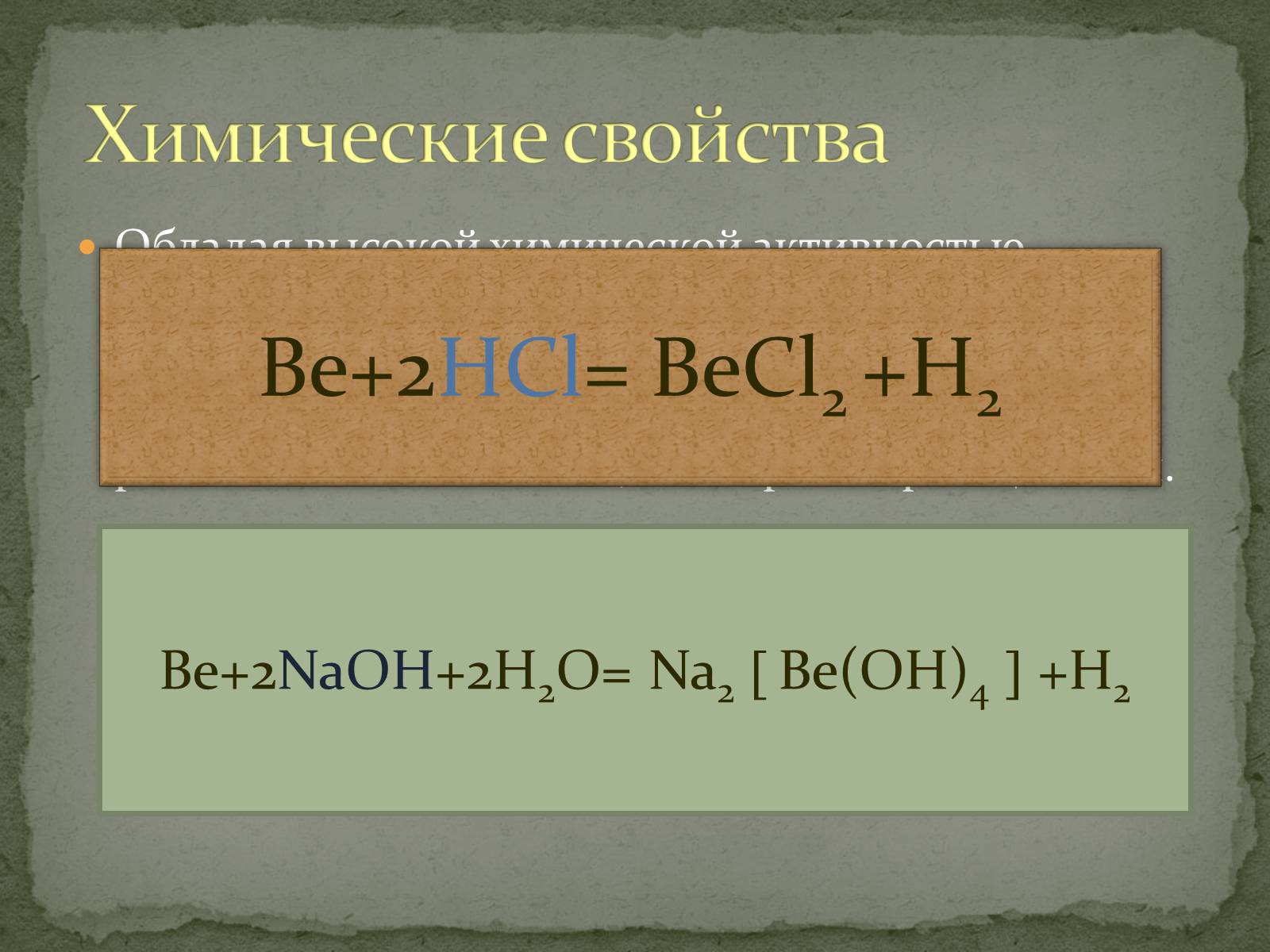
Обладая высокой химической активностью бериллий вступает в реакции с галогенами, серой и азотом. Вода на него не действует, зато подобно алюминию он легко растворяется как в разбавленных кислотах , так в растворах щелочей.
Химические свойства
Be+2HCl= BeCl2 +H2
Be+2NaOH+2H2O= Na2 Be(OH)4 +H2

Магний был открыт при анализе воды из минерального источника вблизи города Эпсом в Англии. Горькая на вкус она привлекла внимание исследователей, при упаривании такой воды на стенках сосуда образовывалась белая корка вещества, соль MgSO4 7H2O
Магний

Впервые магний был получен в 1808г Гемфри Деви при электролизе влажной магнезии . По его предложению элемент назвали Magnium
Поучение

Физические свойства
Мягкий и пластичный
При комнатной температуре покрыт тончайшей оксидной плёнкой
Температура плавления 650 С
Mg

Распространение в природе
Входит в состав минералов
магнезит MgCO3
Доломит MgCO3 CaCO3
Магний входит в состав активного центра зелёного пигмента растений -хлорофилла

Горение на воздухе 2Mg+ O2=2MgO
При комнатной температуре не взаимодействует с водой, лишь при кипячении Mg+2H2O=Mg(OH)2 +H2
Магний легко взаимодействует с разбавленными кислотами
Химические свойства
Химически активен
Сильный восстанови-
тель

Применение
Mg
Твёрдые и прочные сплавы с алюминием магналий- 30 Mg
Электрон –включает цинк, марганец, медь
Автомобильная , авиационная и ракетная промышленность
В медицине
Оксид магния -для понижения кислотности желудка
Сульфат магния - слабительное
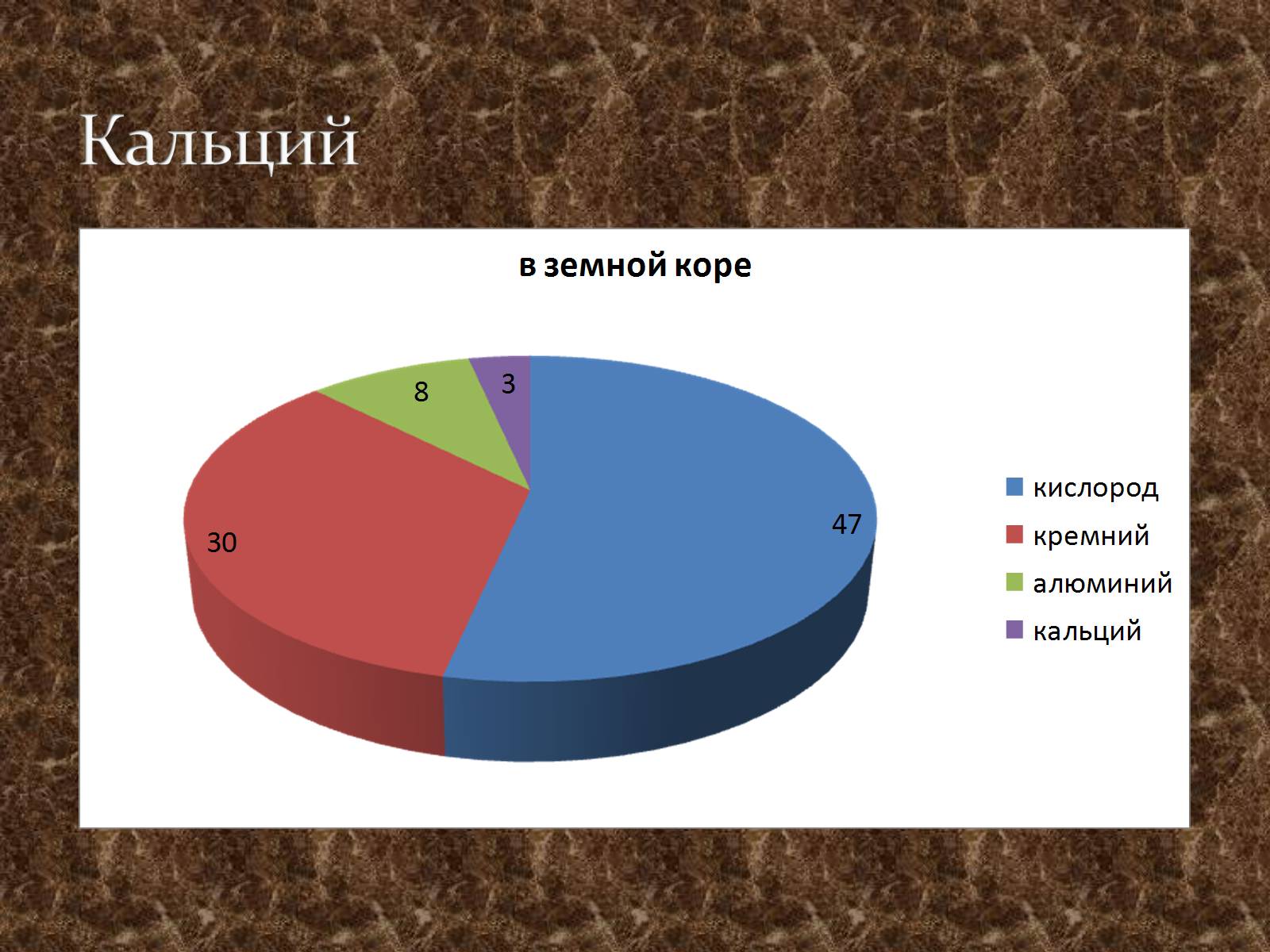
Кальций

Распространение в природе
Гипс CaSO4 2H2O
Флюорит CaF2
апатит Ca5(PO4)3(OH)
мел, мрамор, известняк CaCO3

Получение
Металлический кальций был получен в 1808 году при электролизе смеси влажной гашёной извести с оксидом ртути
Электролиз расплавов солей CaCl2 =Ca+Cl2
Алюмотермия CaO +Al=CaAlO+Ca
Физические свойства
Ca
Лёгкий, беловато-серый,
Пластичный металл
Из –за достаточной твёрдости невозможно резать ножом, как щелочные металлы
Температура плавления С

С простыми веществами
Ca+H2=CaH2
Ca+Cl2=CaCl2
Ca+N2=Ca3N
Химические свойства
Кирпично-красное пламя
Ca+O2=CaO

Со сложными веществами
Ca+NH3=Ca(NH2)2 +H2
Ca+H2O=Ca(OH)2+H2
Ca+HCl=CaCl2+H2 любая кислота кроме азотной
Химические свойства
Стронций и барий
Стронций встречается в природе в виде минерала целестина-сульфата стронция образующего красивые розово-красные или бледно-голубые кристаллы
Барий встречается в виде барита (тяжёлого шпата)
BaSO4
Стронций получил своё название от шотландской деревни Стронциан, близь которой был найден редкий минерал стронцианит
Впервые барий был обнаружен шведским химиком Карлом Вильгельмом Шееле и его учеником в тяжёлом шпате и получил название «барис» тяжёлый.
В виде простых веществ барий и стронций были выделены Г.Деви в 1808 году

Соединения кальция, стронция и бария применяют в разных отраслях промышленности и строительстве.
Соединения стронция(нитрат, карбонат ,хлорид, оксалат) используют в производстве осветительных ракет, химического и термически устойчивого стекла. Оксид стронция входит в состав эмалей для защиты металлических предметов.
Применение
BaSO4
Используют в производстве белой краски литопон, обладающей высокой кроющей способностью
Добавка в производстве бумаги дорогих сортов- денежных знаков и документов
Изготовление защитных материалов для рентгеновских установок, в медицине

Презентацию выполнила учитель химии Тихомирова И.Ю. МОУ лицей № 20 г.Кострома
Спасибо за внимание