Презентація на тему «Алюміній» (варіант 14)

10 клас
Алюміній

Назва “алюміній” походить від лат. Alumen (aluminis) – “галуни” у зв'язку із застосуванням останніх як протиотрути під час фарбування тканин і як засобу для припинення кровотечі; алюмокалієві галуни - перші сполуки Алюмінію, що знайшли практичне застосування.
Історична довідка

Періодична система хімічних елементів Д.І.Менделєєва
Періоди
1
2
3
4
5
6
7
Ряди
1
2
3
4
10
9
8
7
5
6
Групи елементів
I
II
VI
V
VII
III
IV
VIII
Характеристика
1.
Вперше добуто в 1825 році Гансом Ерстедом.
2.
У Періодичній системі знаходиться в 3 періоді, III група, головна підгрупа.
3.
У природі зустрічається тільки у вигляді сполук.
4.
Сріблясто-білий, легкий метал. Має високі тепло - та електропровідність.
5.
Валентність: III.
Ступінь окиснення: +3.
27
+13
Al

Алюміній
Al
27
+13
2
8
3
P = 13
e = 13
N = 14
−
Короткий електронний запис:
1s²
2p⁶
3p
1
2s²
3s²

сріблясто – білий метал;
ковкий;
легко витягується;
tпл = 660 0С;
tкип = 2520 0С;
ρ = 22,7 г/см3;
За кімнатної температури Al не змінюється, його поверхня вкрита тонкою оксидною плівкою.
Фізичні властивості Алюмінію:
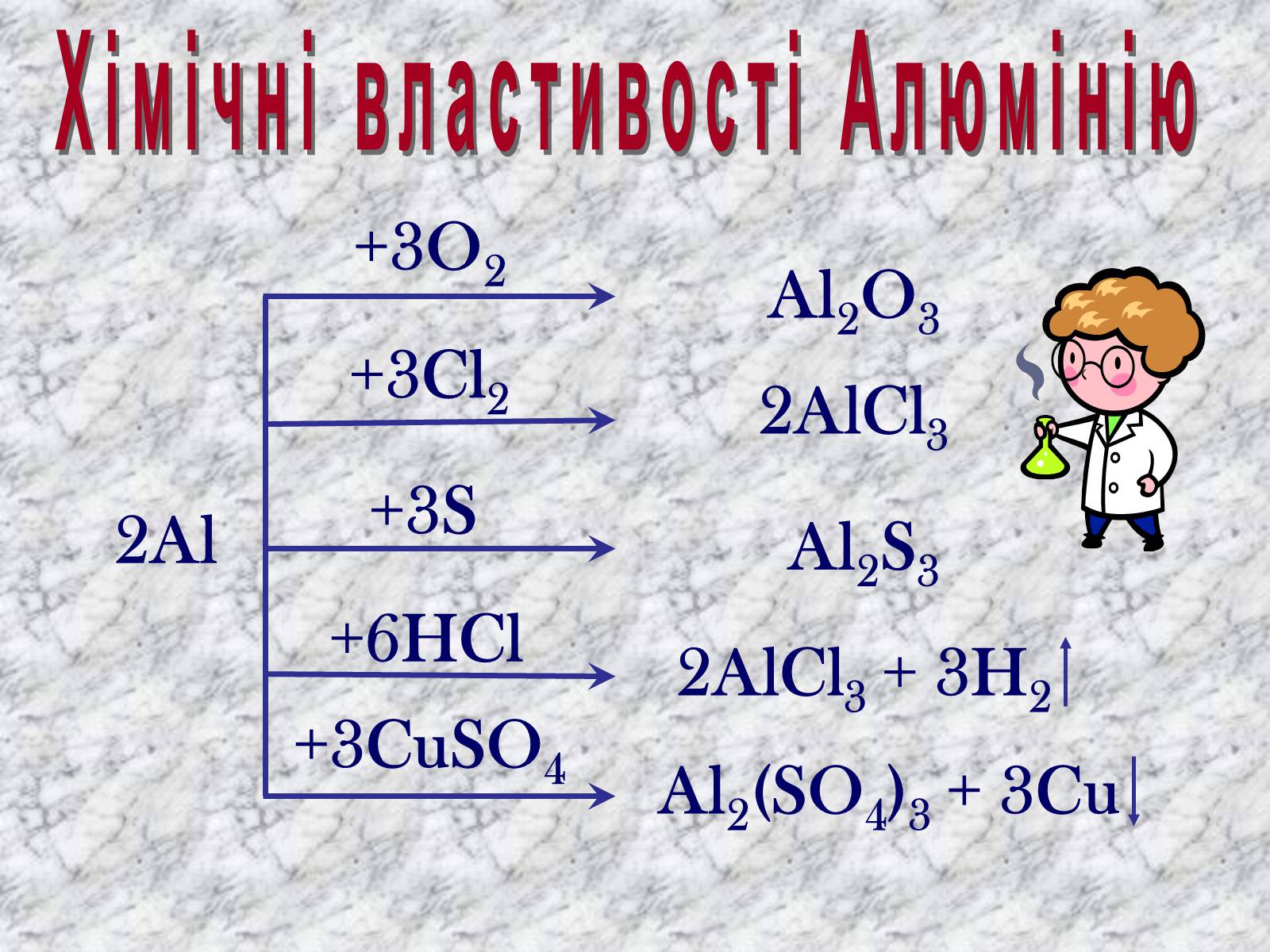
Хімічні властивості Алюмінію
2Al
+3O2
Al2O3
+3Cl2
2AlCl3
+3S
Al2S3
+6HCl
2AlCl3 + 3H2
+3CuSO4
Al2(SO4)3 + 3Cu

Алюміній є амфотерним елементом:
взаємодіє с кислотами та лугами.
2Al + 6HCl(розбавлена) = 2AlCl3 + 3H2
8Al + 15H2SO4(конц.) 4Al2(SO4)3 + 3H2S + 12H2O
Al + 6HNO3 (конц.) Al(NO3)3 + 3NO2 + 3H2O
2Al + 6NaOH 2Na3AlO3 + 3H2
2Al + 2NaOH + 6H2O = 2Na[Al(OН)4] + 3H2
2Al + 6NaOH(надлишок) + 6H2O = 2 Na3[Al(OH)6] + 3H2
t
t
t

Оксид та гідроксид алюмінію також мають амфотерні властивості:
Al2O3 + 6HCl = 2AlCl3 + 3H2O
Al2O3 + 2NaOH = 2NaAlO2 + H2O
2Al(OH)3 + 6HCl = 2AlCl3 + 6H2O
Al(OH)3 + NaOH = NaAlO2 + 2H2O (у процесі сплавлення)
Al(OH)3 + NaOH = Na[Al(OH)4] (у розчинах)
Хімічні властивості сполук Алюмінію

Алюміній дуже добре проводить електричний струм – за електропровідністю він іде після срібла та міді. Тому з чистого алюмінію виготовляють електропроводи.
Алюмінієве покриття добре захищає стальні та чавунні вироби від корозії. Для цього поверхню таких виробів насичують алюмінієм – алітують.
Сплавам алюмінію з міддю, магнієм, силіцієм властиві легкість та висока міцність, тому вони використовуються в авіації, суднобудуванні, залізничному транспорті, у будівництві, приладобудуванні.
Алюміній застосовують для одержання
металів і неметалів.
Застосування Алюмінію та його сполук

Урок закінчено,
Дякуємо усім!