Презентація на тему «Барий»

Барий
Подготовила ученица 10 класса
Баштовая Анастасия

Щелочноземельные металлы. Барий.
Вторая группа главная подгруппа наряду с семейством щелочноземельных металлов включает и два типических элемента –барий и стронций
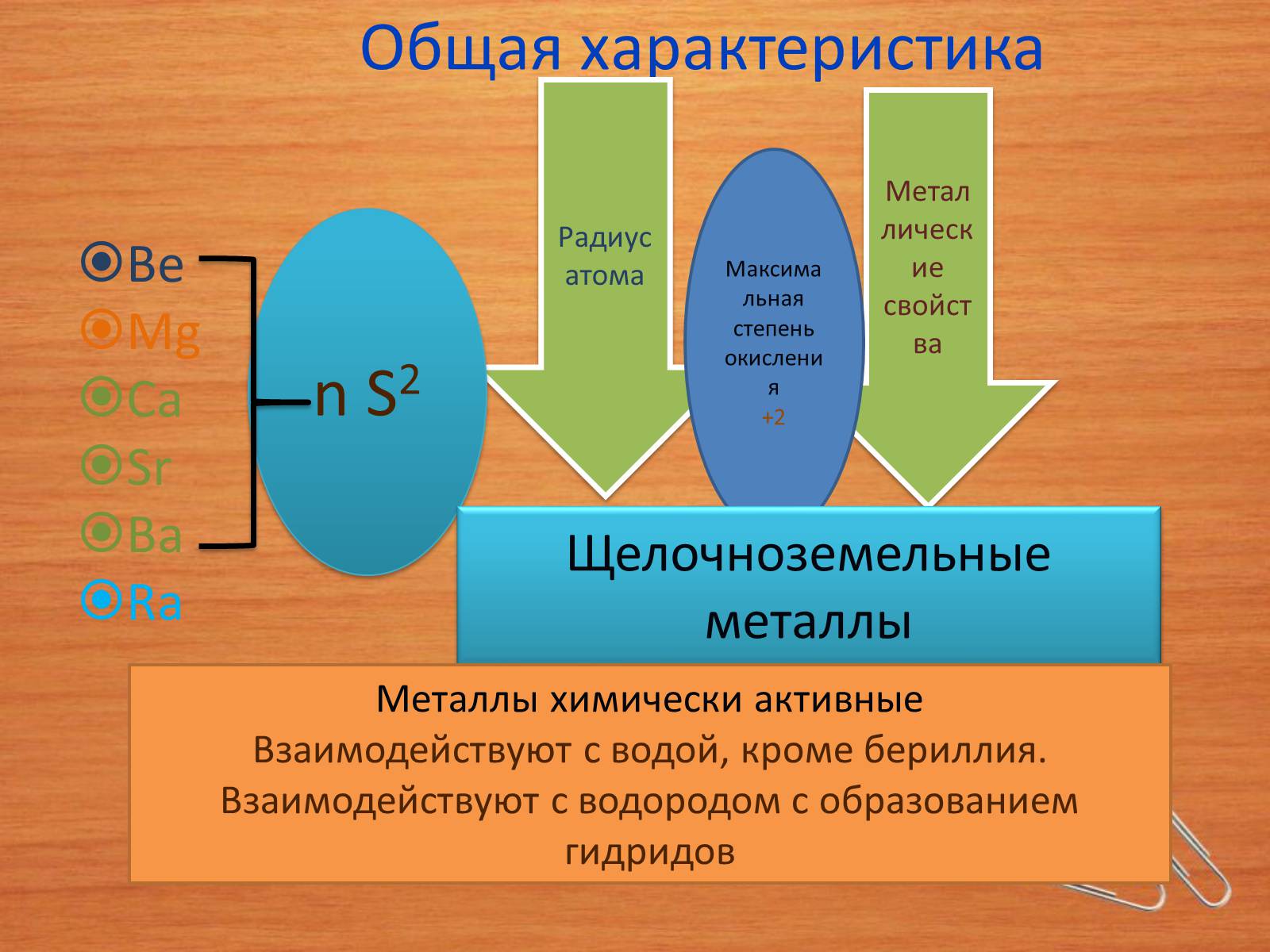
Общая характеристика
Be
Mg
Ca
Sr
Ba
Ra
Радиус атома
Металлические свойства
n S2
Максимальная степень окисления
+2
Щелочноземельные металлы
Металлы химически активные
Взаимодействуют с водой, кроме бериллия.
Взаимодействуют с водородом с образованием гидридов

Барий встречается в виде барита (тяжёлого шпата)
BaSO4
Впервые барий был обнаружен шведским химиком Карлом Вильгельмом Шееле и его учеником в тяжёлом шпате и получил название «барис» тяжёлый.
В виде простых веществ барий и стронций были выделены Г.Деви в 1808 году

Физические свойства
Барий — серебристо-белый ковкий металл. При резком ударе раскалывается. Существуют две аллотропные модификации бария: до 375 °C устойчив α-Ba с кубической объёмно-центрированной решёткой (а = 0,501 нм), выше устойчив β-Ba
Твёрдость по шкале Мооса 1,25.
Хранят металлический барий в керосине или под слоем парафина.

Химические свойства
Барий — щёлочноземельный металл. На воздухе барий быстро окисляется, образуя смесь оксида бария BaO и нитрида бария Ba3N2, а при незначительном нагревании воспламеняется. Энергично реагирует с водой, образуя гидроксид бария Ba(ОН)2:
Активно взаимодействует с разбавленными кислотами. Многие соли бария нерастворимы или малорастворимы в воде: сульфат бария BaSO4, сульфит бария BaSO3, карбонат бария BaCO3, фосфат бария Ba3(PO4)2. сульфид бария BaS, в отличие от сульфида кальция CaS, хорошо растворим в воде. Растворимые соли бария позволяют определить наличие в растворе серной кислоты и её растворимых солей по выпадению белого осадка сульфата бария, нерастворимого в воде и кислотах.
Легко вступает в реакцию с галогенами, образуя галогениды.
При нагревании с водородом образует гидрид бария BaH2, который в свою очередь с гидридом лития LiH дает комплекс Li[BaH3].
Реагирует при нагревании с аммиаком:

Нитрид бария Ba3N2 при нагревании взаимодействует с СО, образуя цианид:
С жидким аммиаком дает темно-синий раствор, из которого можно выделить аммиакат [Ba(NH3)6], имеющий золотистый блеск и легко разлагающийся с отщеплением NH3. В присутствии платинового катализатора аммиакат разлагается с образованием амида бария:
Карбид бария BaC2 может быть получен при нагревании в дуговой печи ВаО с углем.
С фосфором образует фосфид Ba3P2.
Барий восстанавливает оксиды, галогениды и сульфиды многих металлов до соответствующего металла.

Качественный и количественный анализ
Качественно в растворах барий обнаруживается по выпадению осадка сульфата бария BaSO4, отличимого от соответствующих сульфатов кальция и сульфатов стронция крайне низкой растворимостью в неорганических кислотах.
Родизонат натрия выделяет из нейтральных солей бария характерный красно-бурый осадок родизоната бария. Реакция является очень чувствительной, специфичной, позволяя определить 1 часть ионов бария на 210000 массовых частей раствора.
Соединения бария окрашивают пламя в желто-зеленый цвет (длина волн 455 и 493 нм).
Количественно барий определяют гравиметрическим образом в виде BaSO4 или BaCrO4.

Применение
Соединения кальция, стронция и бария применяют в разных отраслях промышленности и строительстве.
Соединения стронция(нитрат, карбонат ,хлорид, оксалат) используют в производстве осветительных ракет, химического и термически устойчивого стекла. Оксид стронция входит в состав эмалей для защиты металлических предметов.
BaSO4
Используют в производстве белой краски литопон, обладающей высокой кроющей способностью
Добавка в производстве бумаги дорогих сортов- денежных знаков и документов
Изготовление защитных материалов для рентгеновских установок, в медицине

Биологическая роль и токсичность
Все растворимые в воде соединения бария высокотоксичны. Вследствие хорошей растворимости в воде из солей бария опасен хлорид, а также нитрат, нитрит, хлорат и перхлорат. Хорошо растворимые в воде соли бария быстро резорбируются в кишечнике. Смерть может наступить уже через несколько часов от паралича сердца.
Симптомы острого отравления солями бария: слюнотечение, жжение во рту и пищеводе. Боли в желудке, колики, тошнота, рвота, понос, повышенное кровяное давление, твердый неправильный пульс, судороги, позже возможны и параличи, синюха лица и конечностей (конечности холодные), обильный холодный пот, мышечная слабость, в особенности конечностей, доходящая до того, что отравленный не может кивнуть головой. Расстройство походки, а также речи вследствие паралича мышц глотки и языка. Одышка, головокружение, шум в ушах, расстройство зрения.
В случае тяжелого отравления смерть наступает внезапно или в течение одних суток. Тяжелые отравления наступают при приеме внутрь 0,2 — 0,5 г солей бария, смертельная доза 0,8 — 0,9 г.
Для оказании первой помощи необходимо промыть желудок 1%-ным раствором сульфата натрия или магния. Клизмы из 10%-ных растворов тех же солей. Приём внутрь раствора тех же солей (20,0 ч. соли на 150,0 ч. воды) по столовой ложке каждые 5 мин. Рвотные средства для удаления из желудка образовавшегося нерастворимого сульфата бария. Внутривенно 10-20 мл 3%-ного раствора сульфата натрия. Подкожно — камфора, кофеин, лобелин — по показаниям. Тепло на ноги. Внутрь слизистые супы и молоко.