Презентація на тему «Солі» (варіант 2)

План:
Основні відомості
Формула
Назви солей
Класифікація
Фізичні властивості
Хімічні властивості
Термічний розклад солей
Добування
Використання
Солі

Основні відомості:
Со́лі — речовини, до складу молекул яких входять кислотні залишки (аніони), поєднані з катіонами різного походження (атоми металів, металоподібні групи, як NH+4, та ін.). Утворюються солі внаслідок реакції нейтралізації кислот, або основ. Як правило, солі є кристалічними речовинами.

Формула:
Men(зал)m
Me-метал,n m-валентність,зал.-кислотний залишок
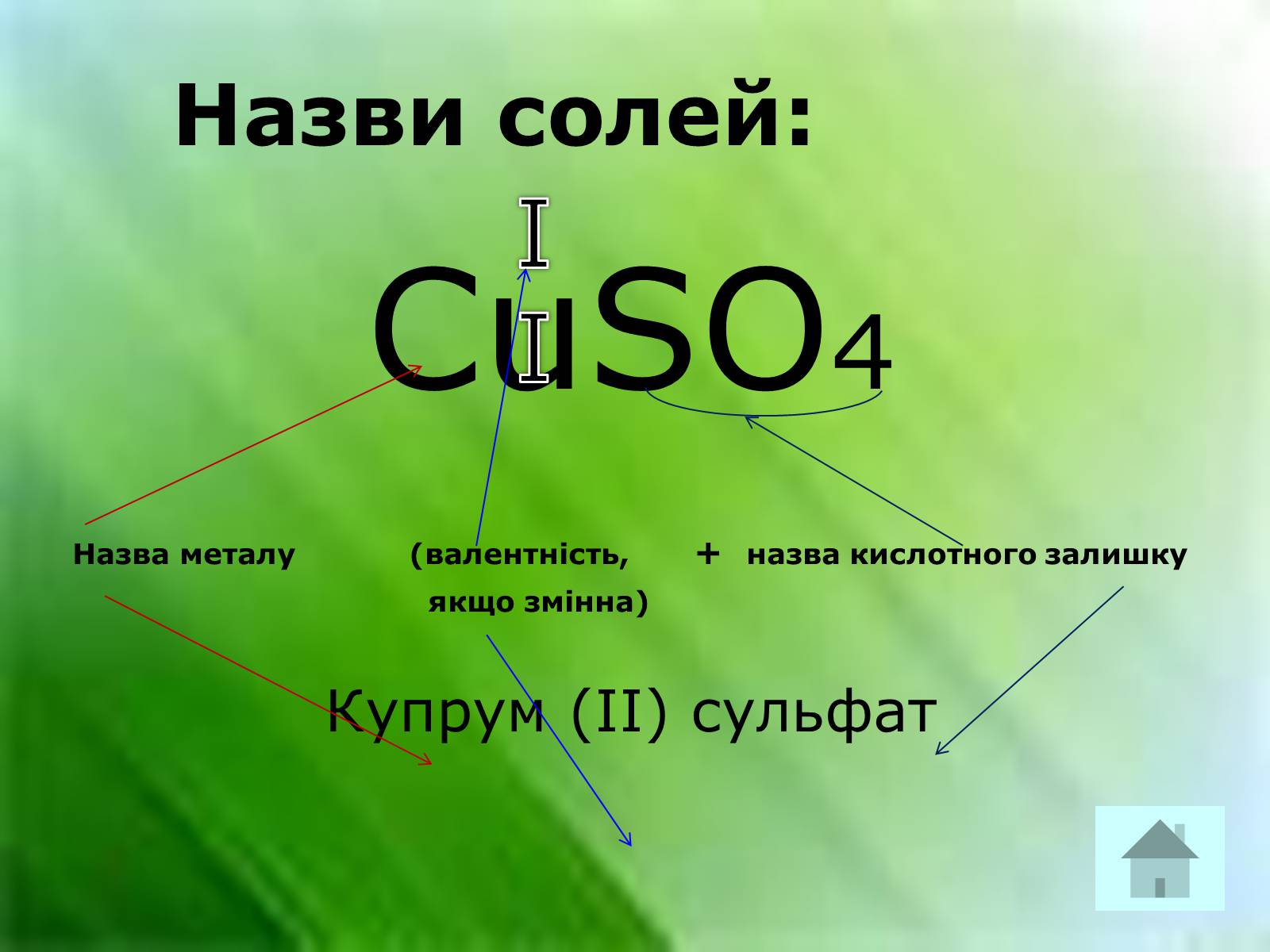
Назви солей:
CuSO4
Назва металу (валентність, + назва кислотного залишку
якщо змінна)
Купрум (ІІ) сульфат
II
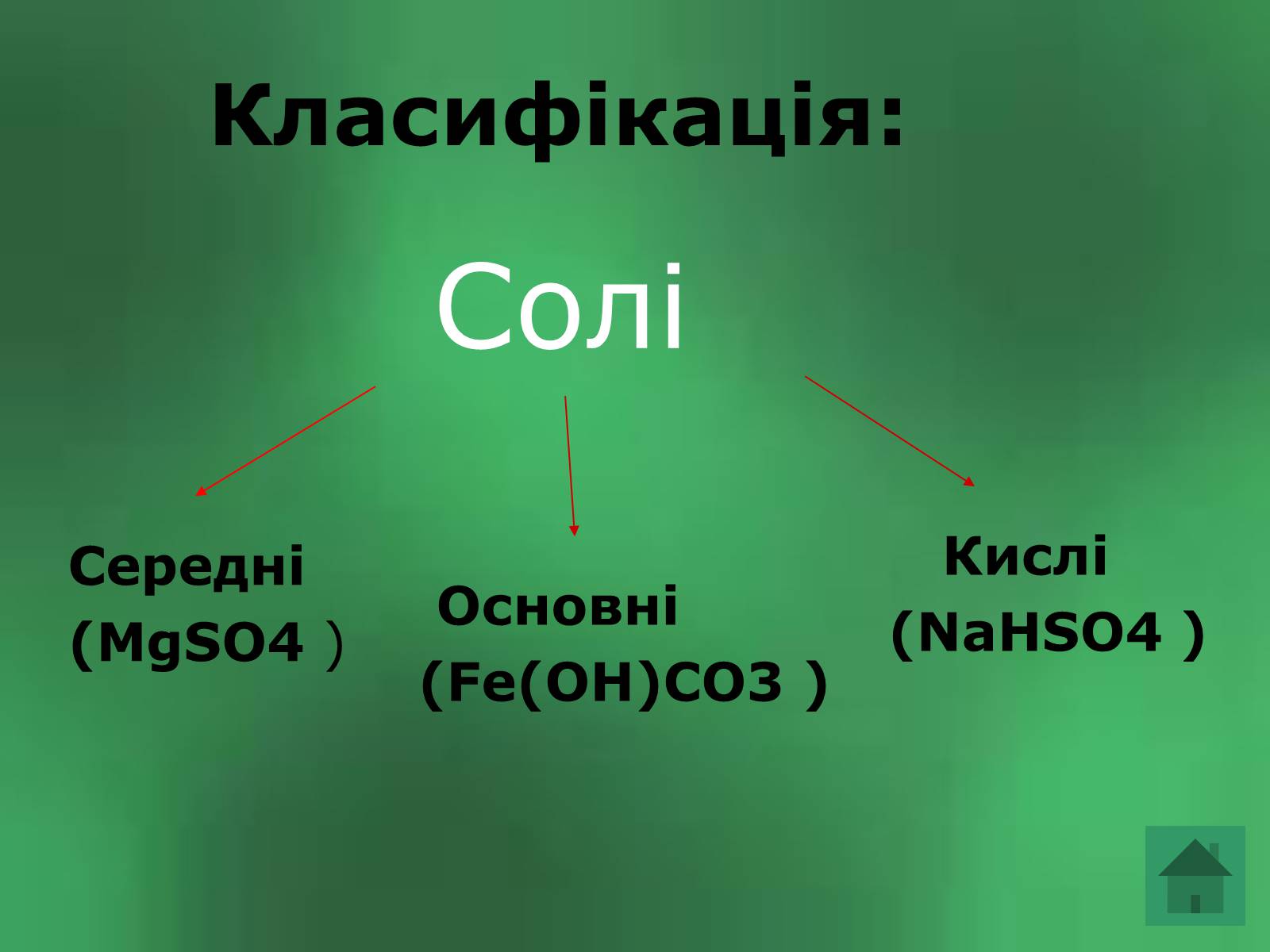
Класифікація:
Солі
Середні
(MgSO4 )
Кислі
(NaHSO4 )
Основні
(Fe(OH)CO3 )

Фізичні властивості:
Солі в основному – тверді кристалічні речовини. Їх можна поділити на розчинні, малорозчинні та практично нерозчинні. Хімічні властивості солей зумовлюються їх відношенням до металів, кислот і солей.

Хімічні властивості:
1.Взаємодія з металами
Ме№1+сіль№1=ме№2+сіль№2
(знаходиться лівіше Н2)
2.Взаємодія з солями
Сіль№1+сіль№2=сіль№3+сіль№4
(р+р=н+р)
3.Взаємодія з лугами
Сіль+луг=основа+сіль

Термічний розклад солей:
Me(NО3)n
лів.Mg Me(NO3)n+O2
Mg-Cu MenOm+NO2+O2
прав.Mg Me+NO2+O2

1. Реакція нейтралізації:
КОН + HNО3 = KNО3 + Н2О
2. Взаємодія кислот з основними оксидами:
CuO + H2SО4 = CuSO4 + Н2О
3. Взаємодія кислот із солями:
ВаСl2 + H2S04 = BaS04u95; + 2НСl
4. Взаємодія кислот з металами:
Mg + 2HCl = MgCl2 + H2u93;
5. Взаємодія двох різних солей:
AgNО3 + КСl = AgClu95; + KNО3
Добування солей:

6. Взаємодія солей з металами:
Fe + CuSO4 = FeSО4 + Cu7. Взаємодія солей з лугами:
ЗКОН + FeCl3 = Fe(OH)3u95; + ЗКСl
8. Взаємодія лугів з кислотними оксидами:
Са(ОН)2 + СО2 = СаСО3 + Н2О9. Взаємодія основних оксидів з кислотними:
СаО + SiО2 = CaSiО3
10. Взаємодія металів із неметалами:
Fe + S = FeS

Солі соляної кислоти. З хлоридів
найбільше використовують хлорид
натрію і хлорид калію. Хлорид натрію
(кухонну сіль) виділяють з озерної та
морської води, а також
добувають у соляних
шахтах. Кухонну сіль
використовують у їжу. У
промисловості хлорид натрію
служить сировиною для отримання
хлору, гідроксиду натрію і соди.
Хлорид калію використовують у
сільському господарстві як калійне добриво.
Використання:

Солі сірчаної кислоти. У будівництві і в медицині широко використовують напівводний гіпс, одержуваний при випаленні гірської породи (дигідрат сульфату кальцію). Будучи змішаний з водою, він швидко застигає, утворюючи дигідрат сульфату кальцію, тобто гіпс. Декагідрат сульфату натрію використовують в якості сировини для отримання соди.

Солі азотної кислоти. Нітрати найбільше використовують в якості добрив у сільському господарстві. Найважливішим із них є нітрат натрію, нітрат калію, нітрат кальцію і нітрат амонію. Зазвичай ці солі називають селітрами.

Солі вугільної кислоти. Карбонат кальцію використовують в якості сировини для отримання вапна.Карбонат натрію (соду) застосовують у виробництві скла і при варінні мила. Карбонат кальцію в природі зустрічається і у вигляді вапняку, крейди і мармуру.