Презентація на тему «Силіцій» (варіант 3)

Виконала:
учениця 10-А класу
Сушко Анастасія

Періодична система хімічних елементів Д.І.Менделєєва
Періоди
1
2
3
4
5
6
7
Ряди
1
2
3
4
10
9
8
7
5
6
Групи елементів
I
II
VI
V
VII
III
IV
VIII
Характеристика
1.
У 1811 р. французькі хіміки Ж.Л. Гей-Люссак і Л.Ж. Тенар добули чистий силіцій.
2.
У Періодичній системі знаходиться в 3 періоді, ІV група, головна підгрупа.
3.
У природі зустрічається тільки у зв'язаному стані.
4.
Як проста речовина має кристалічну будову, крихкий, темно-сірого кольору з металічним блиском.
5.
Е=1,9; найнижчий ступінь окислення –4, найвищий ступінь окислення +4.
28
+14
Si
Хімічні властивості
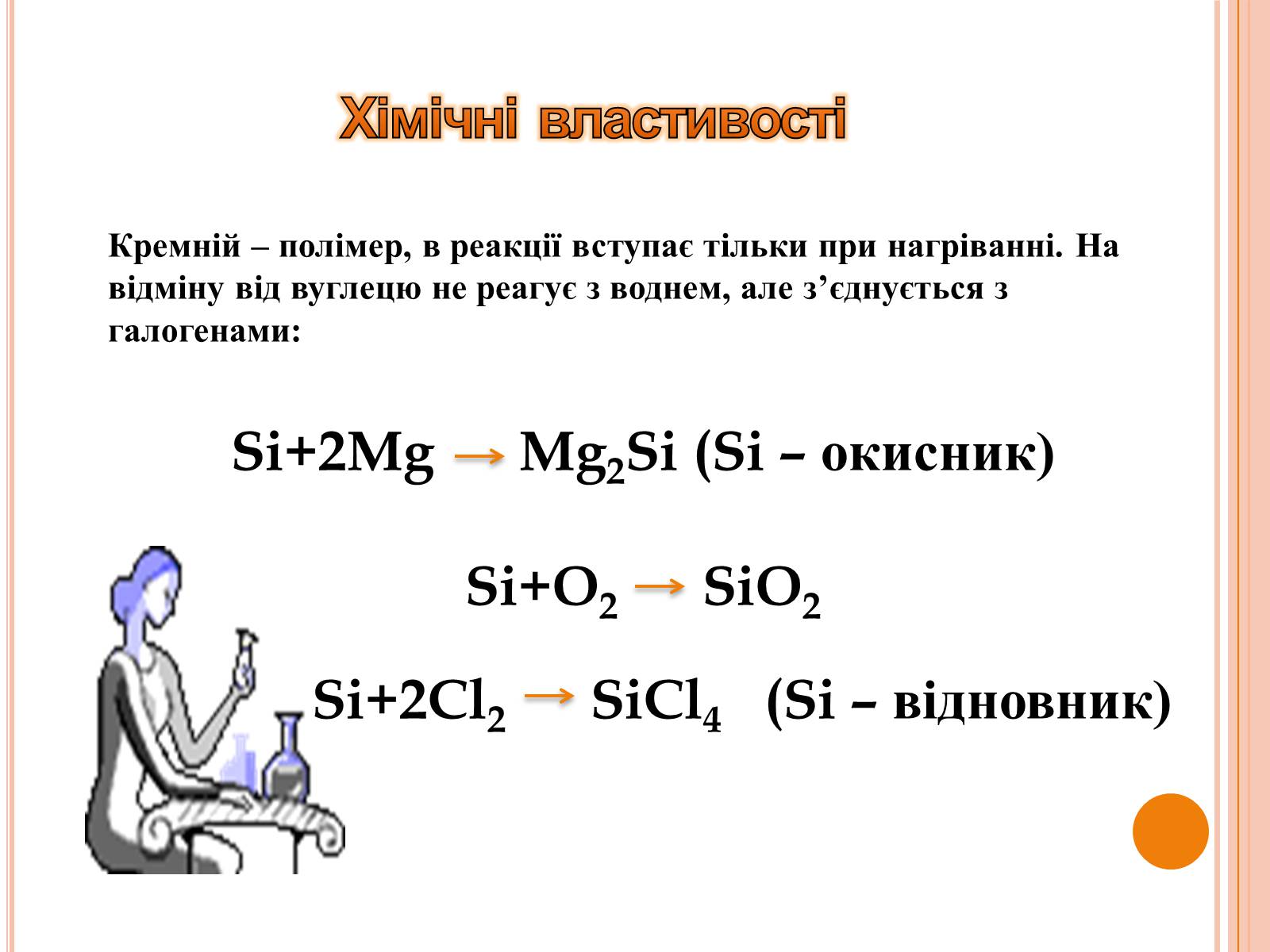
Кремній – полімер, в реакції вступає тільки при нагріванні. На відміну від вуглецю не реагує з воднем, але з'єднується з галогенами:
Si+2Mg Mg2Si (Si – окисник)
Si+O2 SiO2
Si+2Cl2 SiCl4 (Si – відновник)

Характеристика сполук Силіцію
SiO2 – тугоплавкий і хімічно малоактивний, при звичайних температурах. З водою не реагує, свої кислотні властивості проявляє в реакціях з лугами, основними оксидами і деякими солями, які проходять з достатньою швидкістю при підвищених температурах:
2NaOH+SiO2=Na2SiO3+H2O
Na2CO3+SiO2=Na2SiO3+CO2
З кислотами SiO2 не реагує, виняток складає плавикова кислота:
SiO2+4HF=SiF4+2H2O.
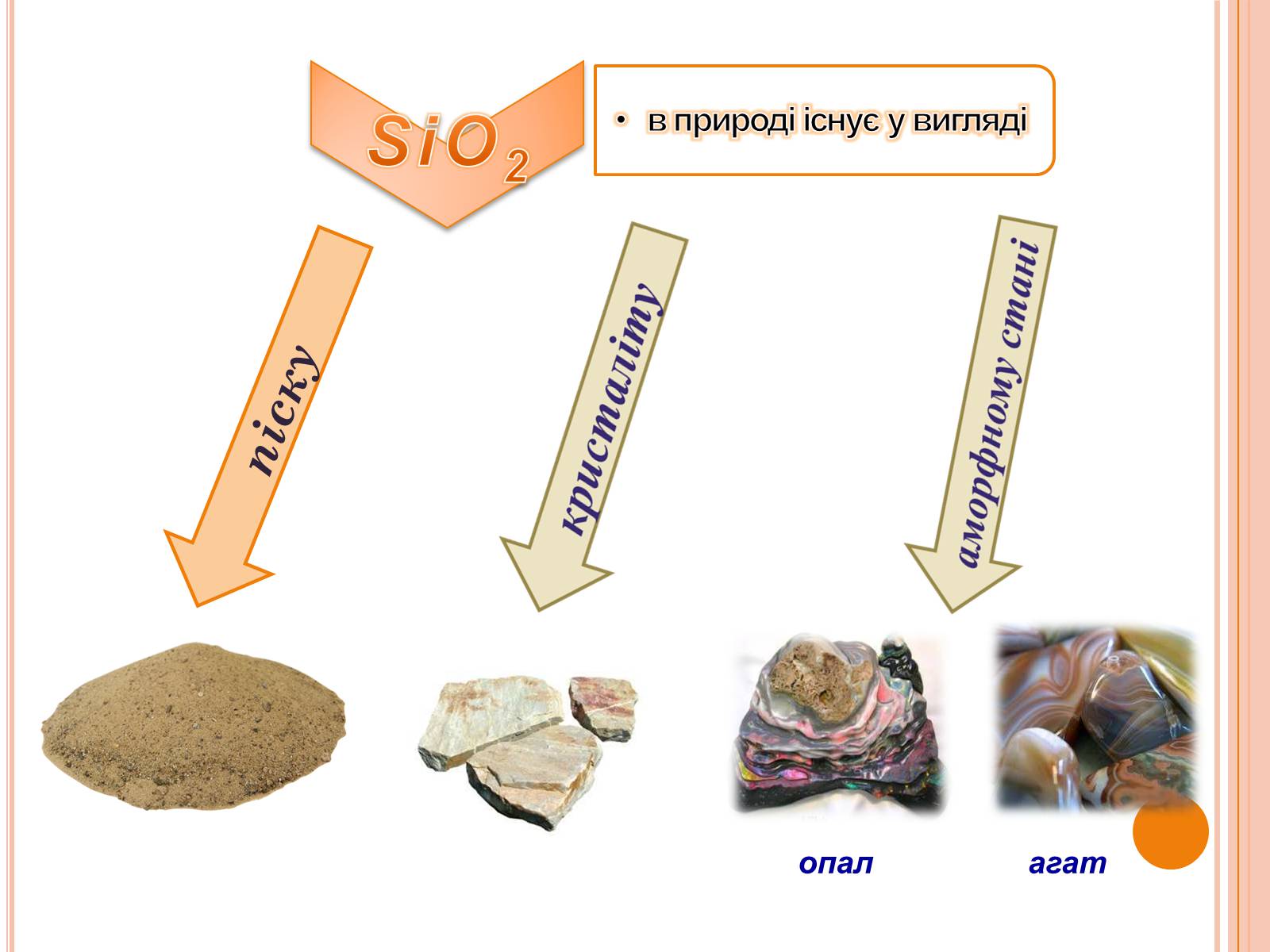
піску
опал
агат

Силікатні матеріали
цегла
кварцовий
пісок
цемент
рідке скло

Силікатні матеріали
скло
фарфор
фаянс

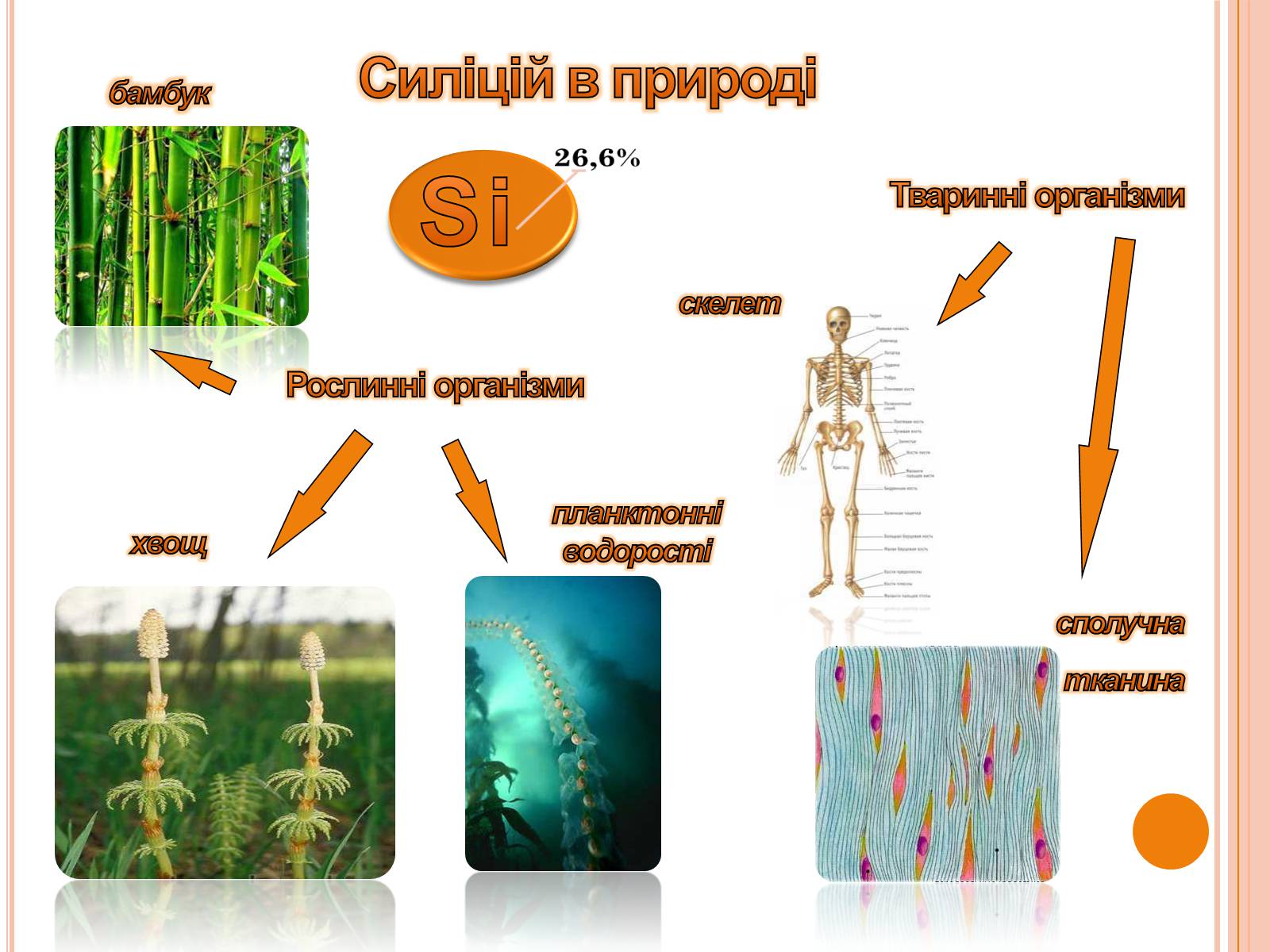
Силіцій в природі
Si
Силікати
алюмосилікати
азбест
тальк
польовий шпат
каолін
нефелін
слюда
Si
Рослинні організми
бамбук
хвощ
Тваринні організми
планктонні
водорості
скелет
сполучна
тканина
Силіцій в природі