Презентація на тему «Степень окисления»

Степень окисления. Бинарные соединения металлов и не металлов: оксиды, хлориды, сульфиды и др.

ОПРЕДЕЛЕНИЕ:
Степень окисления – это условный заряд атомов химического элемента в соединении, вычисленный на основе предположения, что все соединения состоят только из ионов.

Степень окисления бывает: «+», «-», «0».
I. Степень окисления «0» - ноль:
1. Простые вещества: Н2, Са, О2, К…
2. Сложные в-ва (в сумме): Са+2О-2
(+2 – 2 =0)

Табл. 1:Степени окисления элементов в соединениях:
I – группа: С.О. +1 Na+1Cl, K+1Cl…
II - группа: С.О. +2 Сa+2Cl2…
III - группа: С.О. +2 Al+3Cl3…
Кислород: С.О. -2 Na+12О-2, Сa+2О-2.
Водород: С.О. +1, с металлами -1.
F (фтор) С.О. -1,
Cl (хлор) С.О -1 почти всегда.

Определить степени окисления. Упр2, стр. 64.
Пример: Cl2O7
Выпишем степень окисления кислорода.
Обозначим неизвестную с.о. хлора через Х:
Cl2+х O7-2 ,
3. составим уравнение:
2∙х+(-2)∙7=0
2∙х -14=0
2∙х=+14
Х=+7
Ответ: Cl2+7O7-2
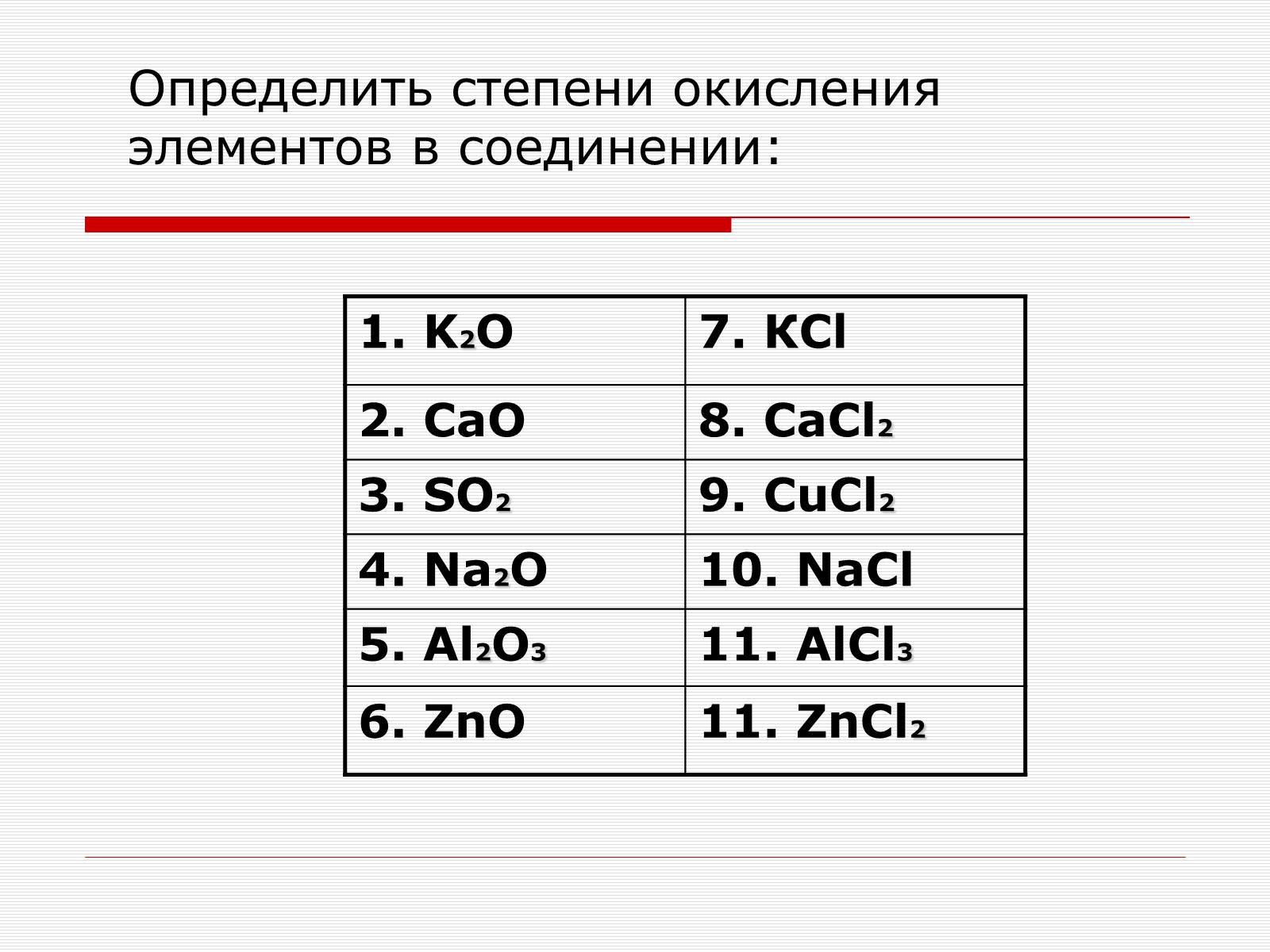
Определить степени окисления элементов в соединении:
1. K2O
7. КCl
2. CaO
8. СaCl2
3. SO2
9. СuCl2
4. Na2O
10. NaCl
5. Al2O3
11. AlCl3
6. ZnO
11. ZnCl2
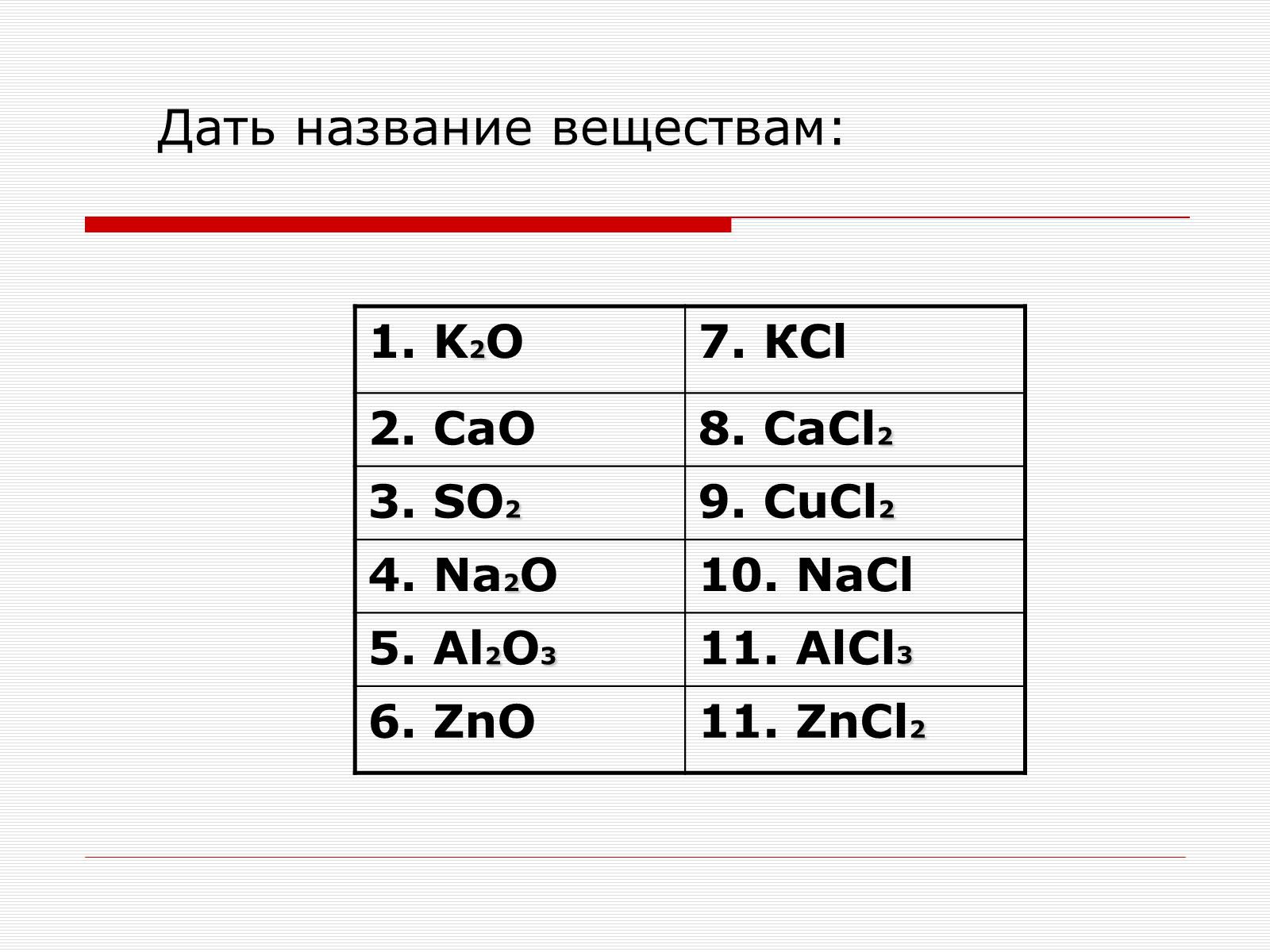
Дать название веществам:
1. K2O
7. КCl
2. CaO
8. СaCl2
3. SO2
9. СuCl2
4. Na2O
10. NaCl
5. Al2O3
11. AlCl3
6. ZnO
11. ZnCl2