Презентація на тему «Клітинна інженерія» (варіант 1)
— це самостійна галузь біологічних та медичних наук, в завдання входить створення нових, не існуючих раніше в природі клітин із заданими властивостями.
розробка методів
штучного злиття клітин,
що ростуть в культурі;
ефективна трансфекція
соматичних та
статевих клітин
отримання реконструйованих клітин
шляхом злиття – об'єднання ядра
та цитоплазми від різних клітин
у раніше невідомих комбінаціях
Історично клітинна інженерія
пройшла наступні етапи:
Клітинна інженерія
Типові
гібридні
Клітини:
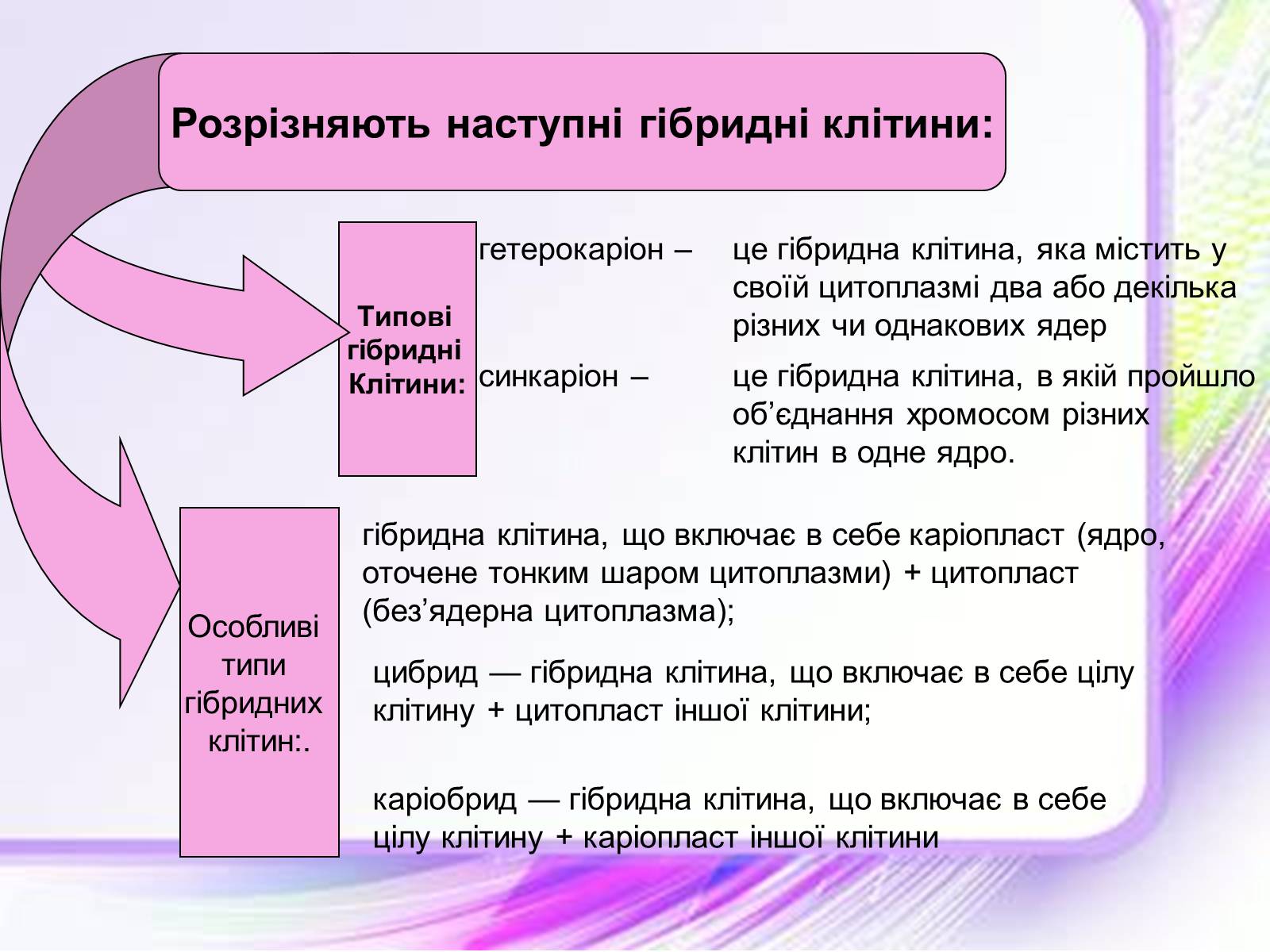
гетерокаріон – tце гібридна клітина, яка містить у ttсвоїй цитоплазмі два або декілька ttрізних чи однакових ядер
синкаріон – tце гібридна клітина, в якій пройшло ttоб'єднання хромосом різних tttклітин в одне ядро.
гібридна клітина, що включає в себе каріопласт (ядро, оточене тонким шаром цитоплазми) + цитопласт (без'ядерна цитоплазма);
цибрид — гібридна клітина, що включає в себе цілу клітину + цитопласт іншої клітини;
каріобрид — гібридна клітина, що включає в себе цілу клітину + каріопласт іншої клітини
Особливі
типи
гібридних
клітин:.
Розрізняють наступні гібридні клітини:

1.
Використання інактивного вірусу Сендай, який відноситься до групи вірусів парагрипу, який інактивований УФ–випромінюванням. Цей метод вже майже не використовується (лише у тих випадках, коли клітини іншими методами не зливаються — при роботі з ядерними еритроцитами птахів).
Основний метод — використання поліетиленгліколю (ПЕГ). Це стандартний спосіб, який використовується при злитті клітин тварин та рослин, між собою та один з одним. При отриманні гібридом.
Злиття клітин з використанням лазерного та нейтронного опромінення.
Електрозлиття — клітини попередньо зближені між собою, піддають впливу електричного поля; спочатку проходить об'єднання мембран, потім об'єднуються цитоплазми і формується гібридна клітина.
2.
4.
3.
Основні методи злиття клітин

1.
2.
Авдин – біоновий метод. Клітини одного типу (мієлома) з'єднують з авдином, клітини іншого типу (імунні лімфоцити) безпосередньо або через антитіла з'єднують з біотином (вітамін Н). Такі мічені клітини у суспензії з'єднуються попарно і в результаті дії електричного поля, в яке їх поміщають, утворюються гібридомні клітини.
Метод проточної цитометрії.
Цей метод застосовують:
а) для виділення клітин, що знаходяться на певній стадії клітинного циклу та їх синхронізації. Отримані таким шляхом клони життєздатні і дають початок клітинним клонам;
б) для відбору (селекції гібридних клітин).
Не всі клітини, що піддаються різним впливам для злиття, зливаються. Для видалення клітин, що не злилися, суміш гібридних і клітин, що не злилися, вирощують на селективному середовищі, де виживають лише гібридні клітини
Нові методи злиття

Першим
практичним застосування досягнень клітинної інженерії стала розробка гібридомної технології та отримання з її допомогою моноклональних антитіл.
Другим
практичним застосуванням досягнень клітинної інженерії є доказ можливості направленої генетичної трансформації соматичних та статевих клітин тварин і рослин та отримання таким шляхом клітин-продуцентів заданих білкових продуктів.

- Пряма (позитивна) селекція, при якій виживає лише певний шуканий tмутантний тип клітин; - Непряма (негативна) селекція, заснована на виборчій загибелі tклітин, які tділяться дикого типу та виживання метаболічно неактивних клітин, tале вимагає додаткової ідентифікації у них мутаційних змін; - Тотальна селекція, при якій індивідуально тестуються всі клітинні tклони; - Візуальна селекція і неселективний відбір, коли варіантна лінія tможе бути tідентифікована серед всієї популяції клітин візуально або при tвикористанні біохімічних методів(тонкошарова або рідинна tхроматографія, радіоімуннийаналіз, мікроспектрофотометрія та ін.)
Значний інтерес представляє питання про використання клітинної селекції в комплексі з отриманням сомаклонов. Одна з найбільш сильних сторін культури in vitro у створенні технологій для сільського господарства - можливість на основі сомаклональних варіацій або індукованих мутацій відбирати в жорстких селективних умовах клітини, які характеризуються шуканими ознаками.
Селекція рослин на клітинному рівні.
Для проведення клітинної селекції використовують такі прийоми:

Для проведення робіт з клітинної селекції рослин в умовах in vitro в якості об'єкта дослідження можуть бути використані калюсна, суспензійні культури або ізольовані протопласти. Вибір об'єкта залежить від наявності розроблених технологій стосовно до різних видів рослин, а також від кінцевих цілей дослідження. Калюсна тканина являє собою легко доступний матеріал, який найбільш часто використовують для клітинної селекції. Як правило, роботу проводять на первинній або пересадковою калюсна тканини, яка не втрачає здатності до регенерації протягом ряду субкультівірованій. Однак при роботі з калюсних культур багато дослідників відзначають істотні недоліки даного об'єкта, повільний ріст тканини, нерівноцінні для всіх клітин дію токсичних речовин, які застосовуються в якості селективного фактора, а також втрата регенераційної здатності в процесі культивування калюсних клітин. Безсумнівно, проводити селекцію доцільно на рівні поодиноких клітин (суспензійна культура, протопласти). Однак для багатьох видів рослин не розроблені ефективні технології та способи культивування поодиноких клітин. Тому, незважаючи на перераховані вище недоліки використання калюсних культур, цей спосіб селекції залишається для деяких видів рослин поки єдиним

Як правило, селекція починається з отримання достатньої кількості калюсна маси з ізольованих рослинних експлантів, що використовується в подальшому для визначення концентрації селективного фактора (побудова дозової кривої), при якій спостерігається одночасно зростання калюсна тканини, і в той же час частина калюсних колоній гине. Обрана концентрація селективного фактора визнається оптимальною і використовується в подальших експериментах. Так як первинно отримані на середовищах з селективними факторами колонії клітин могли виникнути внаслідок фізіологічної адаптації чи певного стану диференціювання клітин і не бути генетично стійкими, то протягом наступних 4-6 субкультівірованій на селективної середовищі перевіряється стабільність стійкості отриманих клонів. Потім їх переносять на середовище без селективного фактора і субкультівіруют ще 2-3 пасажу. І тільки після повторного повернення в селективні умови відбирають стабільні клони, з яких намагаються отримати рослини-регенеранти. Однак роботи, проведені з отриманням рослин, стійких до підвищених солей, а також до токсинів, виділеним із грибів-збудників хвороб, показали, що стійкість клітини і рослини до досліджуваного селективного фактора може збігатися і не збігатися. Пряма кореляція між стійкістю рослин і клітин in vitro відзначена лише для низьких температур, стійкістю до гербіцидів, високих концентрацій алюмінію та інших факторів.

Велика кількість робіт з культивування калюсу, з метою отримання нового селекційного матеріалу, проведено на пшениці, ячмені, рисі, сорго, а також на картоплі, томатах, люцерні, вкрай рідко, на деревних. Вже досягнуто перші позитивні результати з отримання рослин пшениці, рису, картоплі, стійких до NaCl або Na 2 S0 4. Отримано клітини, а з них рослини моркви, які синтезують в 20 разів більше метіоніну, в 30 разів - триптофану, в 5 разів - лізину шляхом додавання в живильне середовище токсичних аналогів амінокислот. Для картоплі отримані рослини, стійкі до кільцевої гнилі. Що стосується деревних, то для них роботи в цьому напрямку вкрай рідкісні і часто мають пошуковий характер. Таким чином, використання калюсна культури в селекційних цілях відкриває величезні можливості у створенні нових форм рослин, що несуть цінні ознаки, необхідні для людства. Поряд з перерахованими вище об'єктами (калюсна, суспензійна культура, ізольовані протопласти), в якості вихідного матеріалу для селекції можуть бути використані культури соматичних або андрогенних ембріоїдів, такі органогенні експлантів, як сегменти листя або різні меристематические і стеблові частини рослин, а також культура ізольованих зародків .

Таким чином, проведення селекції на клітинному рівні дозволяє створювати нові форми рослин в 2-4 рази швидше в порівнянні з традиційними способами селекції.
шляхом культивування та селекції in vitro зародків з насіння отримані рослини ячменю, стійкі до аналогів амінокислот, з поліпшеним вмістом білка
Для картоплі розроблено ефективний метод обробки пагонів і черешків мутагеном, що приводив до отримання химерних мутантів хлорофіллдефектності і резистентності до антибіотиків.
Наприклад
При культивуванні
пиляків ярої пшениці сорту Саратовська-29 і Москов-ська-35 на поживних середовищах з підвищеним вмістом солей хлориду натрію отримані соматичні ембріоїдів, а в подальшому рослини-регенеранти, що проявили підвищену солестійкість

Виконала
учениця 10-А класу
Чайка Ірина