Презентація на тему «Явище ізомерії»

Явище ізомерії. Структурна ізомерія гомологів метану. Хімічна будова. Поняття про номенклатуру вуглеводнів.
Близнюки органічного світу

Мета.
Поглибити уявлення про гомологічний ряд, ознайомити із загальною формулою алканів, їх структурою.
Ознайомити з міжнародною номенклатурою.
З'ясувати явище ізомерії.
Почати формувати вміння складати графічні формули та називати ізомери парафінів за міжнародною номенклатурою.
Структурні формули органічних речовин
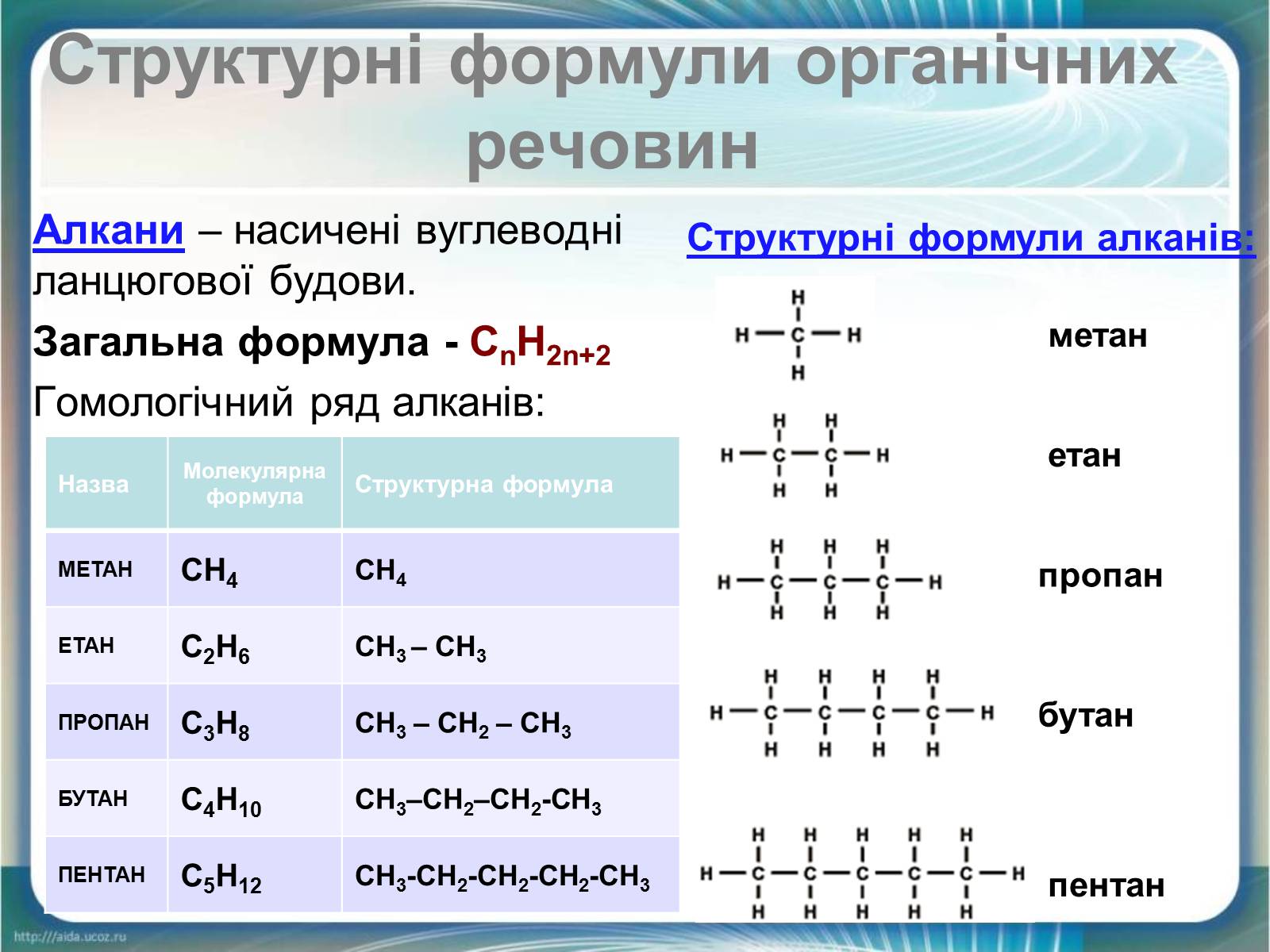
Алкани – насичені вуглеводні ланцюгової будови.
Загальна формула - СnH2n+2
Гомологічний ряд алканів:
Назва
Молекулярна формула
Структурна формула
МЕТАН
СН4
СН4
ЕТАН
С2Н6
СН3 – СН3
ПРОПАН
С3Н8
СН3 – СН2 – СН3
БУТАН
С4Н10
СН3–СН2–СН2-СН3
ПЕНТАН
С5Н12
СН3-СН2-СН2-СН2-СН3
метан
етан
пропан
бутан
пентан
Структурні формули алканів:

Структурні формули органічних речовин
Алкани – насичені вуглеводні ланцюгової будови.
Загальна формула - СnH2n+2
Гомологічний ряд алканів:
Назва
Молекулярна формула
Структурна формула
МЕТАН
СН4
СН4
ЕТАН
С2Н6
СН3 – СН3
ПРОПАН
С3Н8
СН3 – СН2 – СН3
БУТАН
С4Н10
СН3–СН2–СН2-СН3
ПЕНТАН
С5Н12
СН3-СН2-СН2-СН2-СН3
метан
етан
пропан
бутан
пентан
Структурні формули алканів:
Система з правил складання формул та назв
Н
С
С
С
С
С
Н
Н
Н
Н
Н
О
Н
О
Н
О
Н
О
Н
О
Н
О
Н
С
Номенклатура
органічних
речовин
СН3
│
СН3 – С – СООН
│
СН3
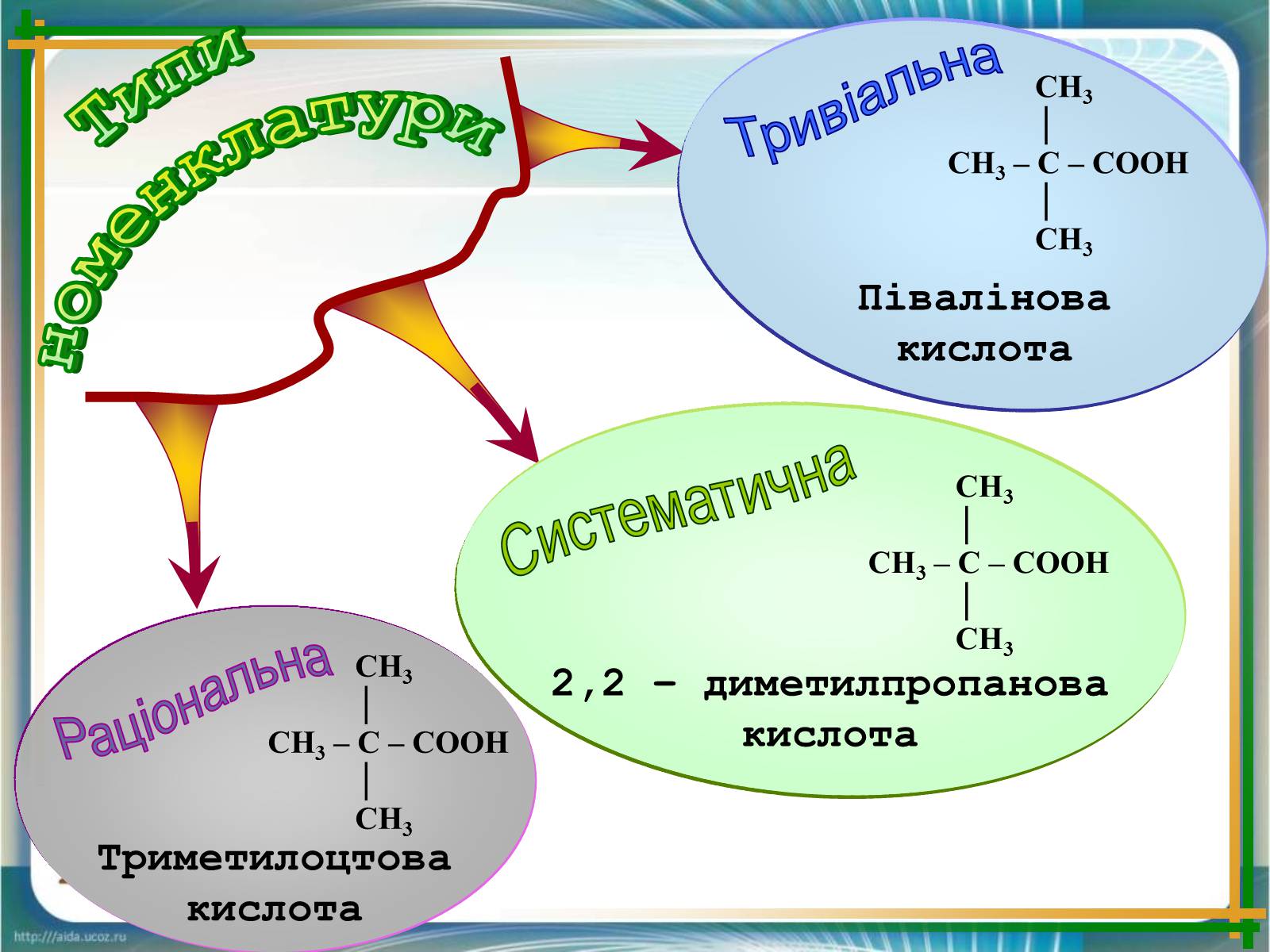
Триметилоцтова кислота
Типи
номенклатури
СН3
│
СН3 – С – СООН
│
СН3
2,2 – диметилпропанова кислота
Систематична
СН3
│
СН3 – С – СООН
│
СН3
Півалінова кислота
Тривіальна
Раціональна

Правила номенклатури IUPAC:
(IUPAC - Міжнародний союз чистої та прикладної хімії, ІЮПАК)
префікс
корінь
суфікс
Назви замісників та номера атомів карбону, до яких вони приеднані
Назва головного ланцюга, залежить від кількості атомів в ньому
Показує кратність зв'язків чи головну функціональну групу

Правила номенклатури IUPAC
Замісники-атоми чи групи атомів, що не увійшли до головного ланцюга
Замісник (радикал) називают, використовуючи суфікс –ил.
Замісники перераховують за абеткою.
Приклад
Позначення кількості замісників:
Два – ди;
Три – три;
Чотири – тетра;
П'ять – пента;
и т. д.
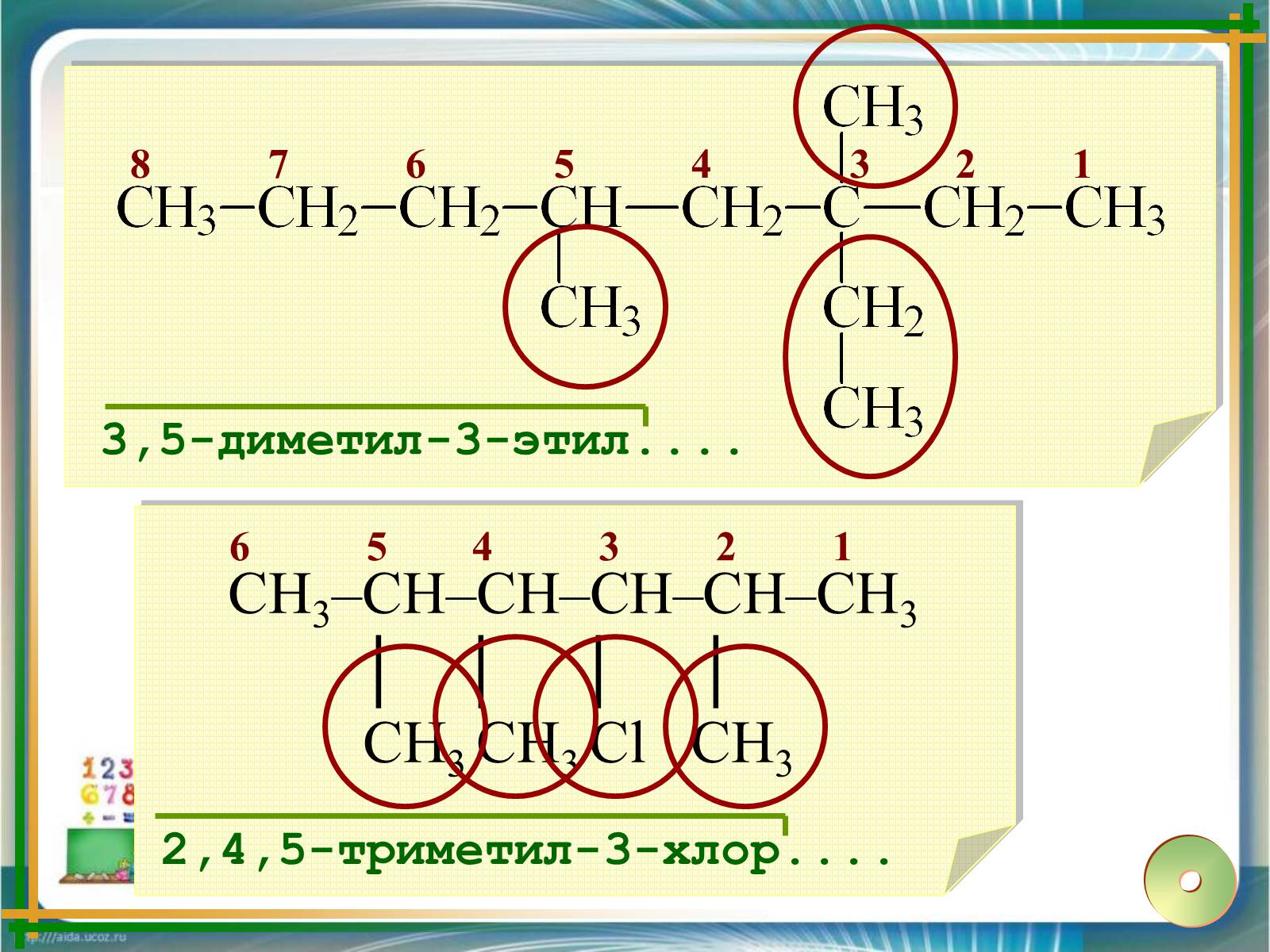
8 7 6 5 4 3 2 1
3,5-диметил-3-этил....
СН3–СН–СН–СН–СН–СН3
│ │ │ │
СН3 СН3 Сl СН3
6 5 4 3 2 1
2,4,5-триметил-3-хлор....

1 – мет; 2 – ет; 3 – проп; 4 – бут; 5 – пент; 6 – гекс; 7 – гепт; 8 – окт; 9 – нон; 10 – дек;
Правила номенклатури IUPAC
Головний ланцюг - карбоновий ланцюг найбільшої довжини, до, якого належить найбільша кількість розгалужень чи кратні зв'язки, чи функціональні групи
Головний ланцюг називають за кількістю атомів карбону в ній
Приклад

Якщо кратні зв‘язки або функціональні групи в головному ланцюгу повторюються декілька разів, використовують приставки: ди-, три-, тетра- і т.д.
Правила номенклатури IUPAC
Кратність зв'язків в головному ланцюгу:
Одинарний (С-С) -ан
подвійний (С=С) –ен
потрійний (С=С) -ин
Таблиця
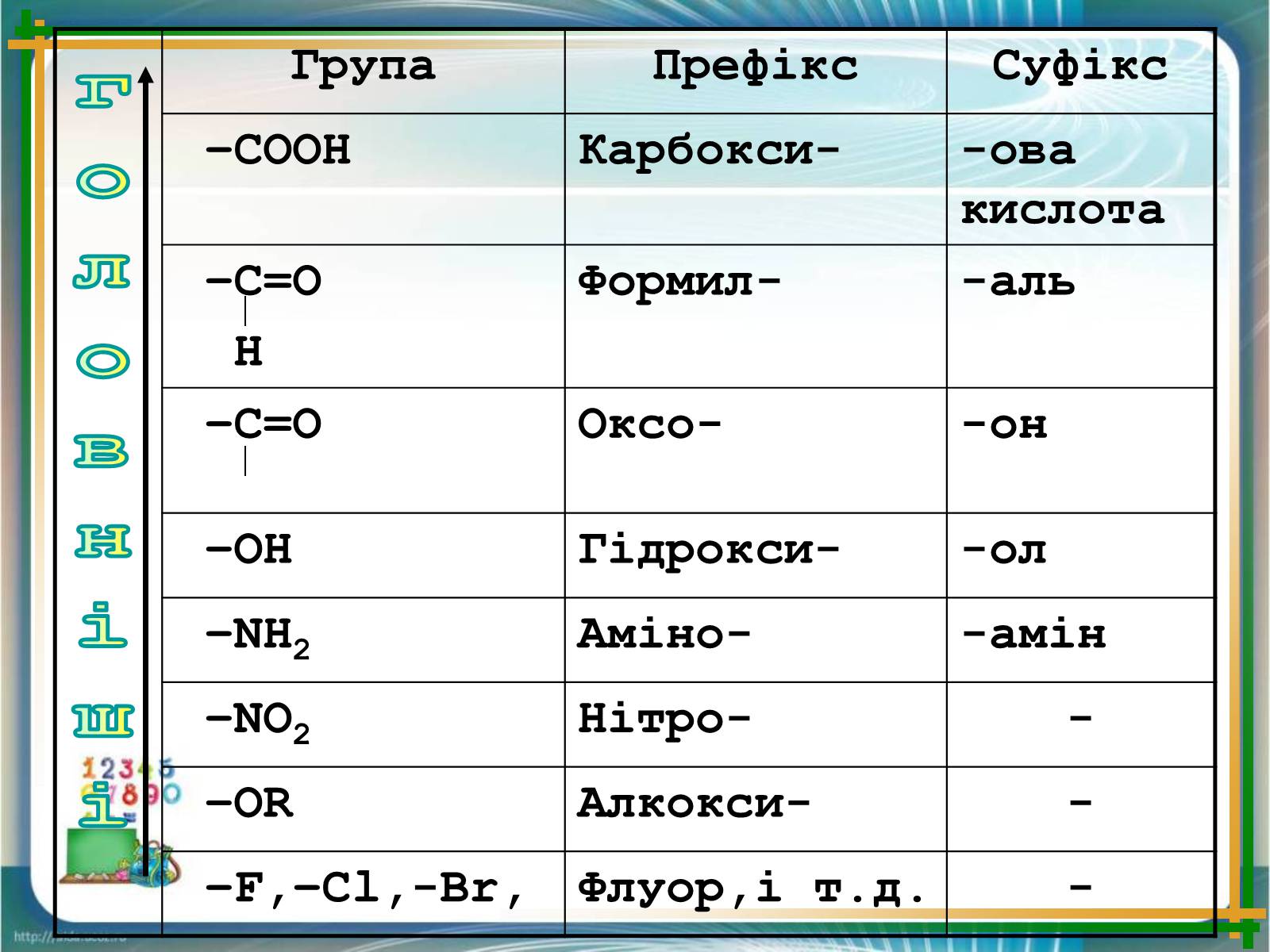
Група
Префікс
Суфікс
–СООН
Карбокси-
-ова кислота
–С=О
Н
Формил-
-аль
–С=О
Оксо-
-он
–ОН
Гідрокси-
-ол
–NН2
Аміно-
-амін
–NО2
Нітро-
-
–ОR
Алкокси-
-
–F,–Cl,-Br,
Флуор,і т.д.
-
головніші
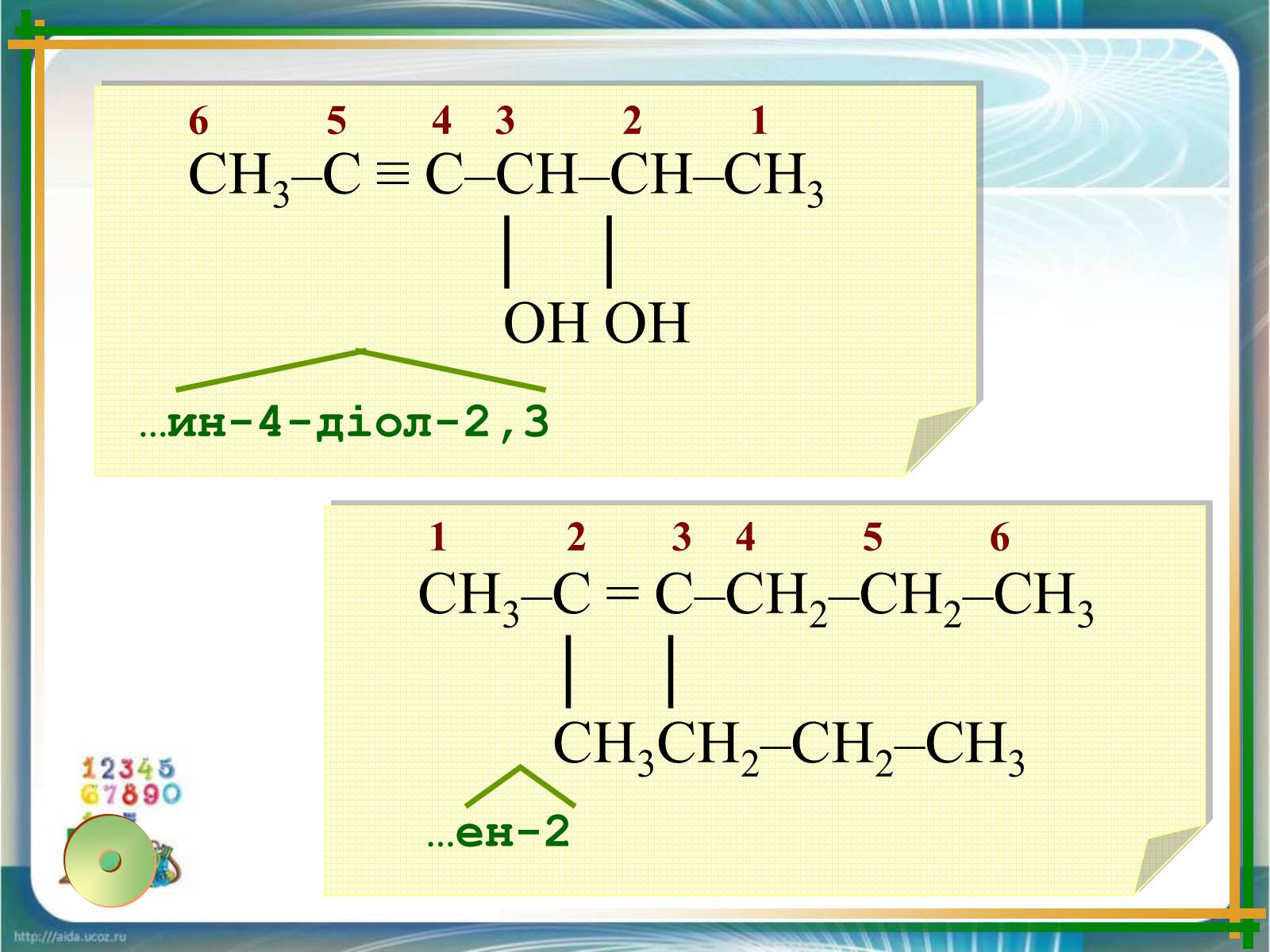
СН3–С = С–СН2–СН2–СН3
│ │
СН3СН2–СН2–СН3
СН3–С ≡ С–СН–СН–СН3
│ │
ОН ОН
1 2 3 4 5 6
…ен-2
6 5 4 3 2 1
…ин-4-діол-2,3

Якщо ланцюгів однакової довжини декілька, вибираємо найбільш розгалужений
Найдемо головний ланцюг (найдовший)
Невірно!
1 2 3 4 5 6 7
3
2
1
4 5 6 7 8
6
7
8
5 4 3
2
1
Вірно!
Приклад
6
7
8
5 4 3
2
1
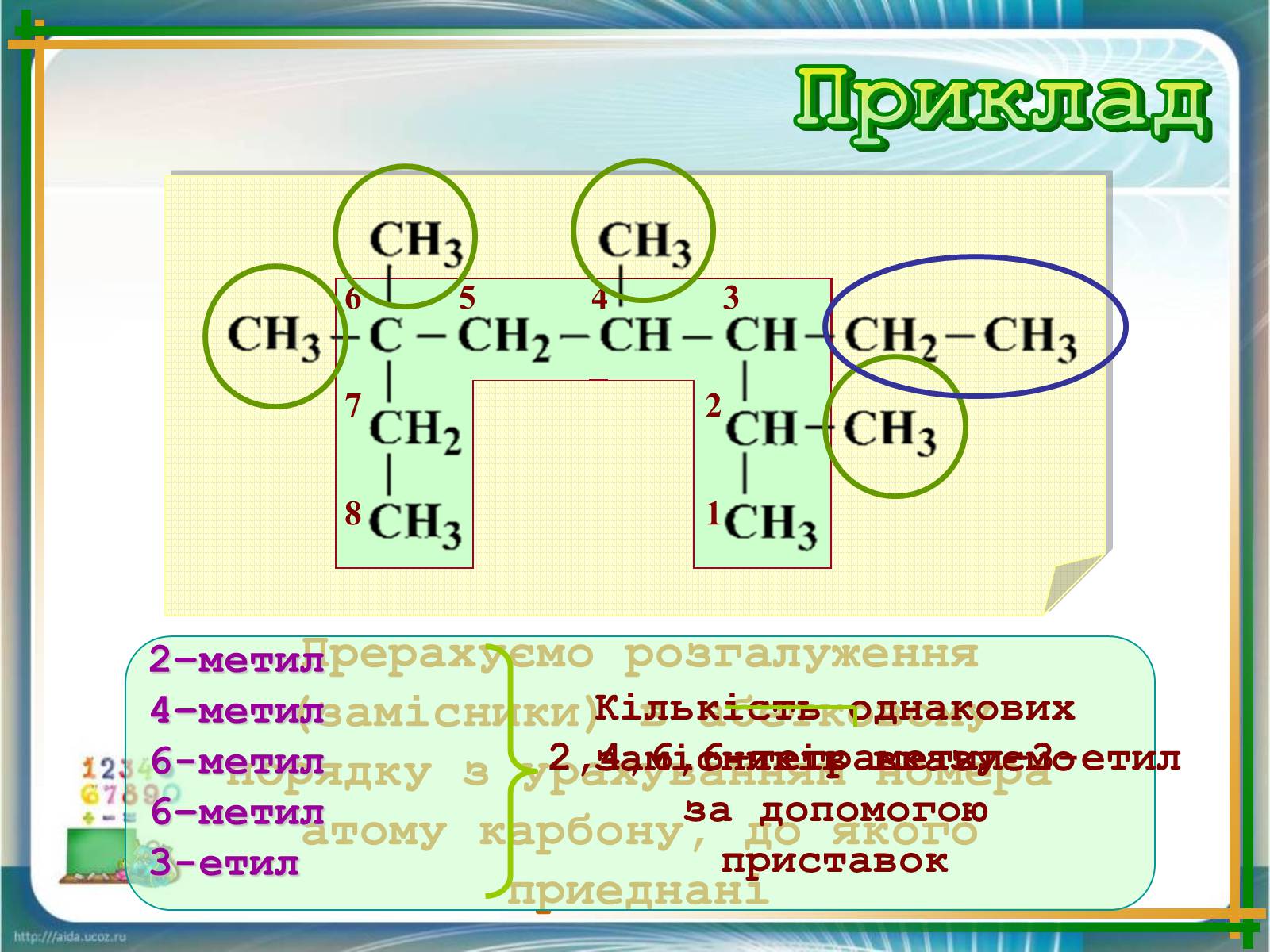
Прерахуємо розгалуження (замісники) в абетковому порядку з урахуванням номера атому карбону, до якого приеднані
2–метил
4–метил
6-метил
6–метил
3-етил
Кількість однакових замісників вказуємо за допомогою приставок
2,4,6,6–тетраметил–3-етил
Приклад
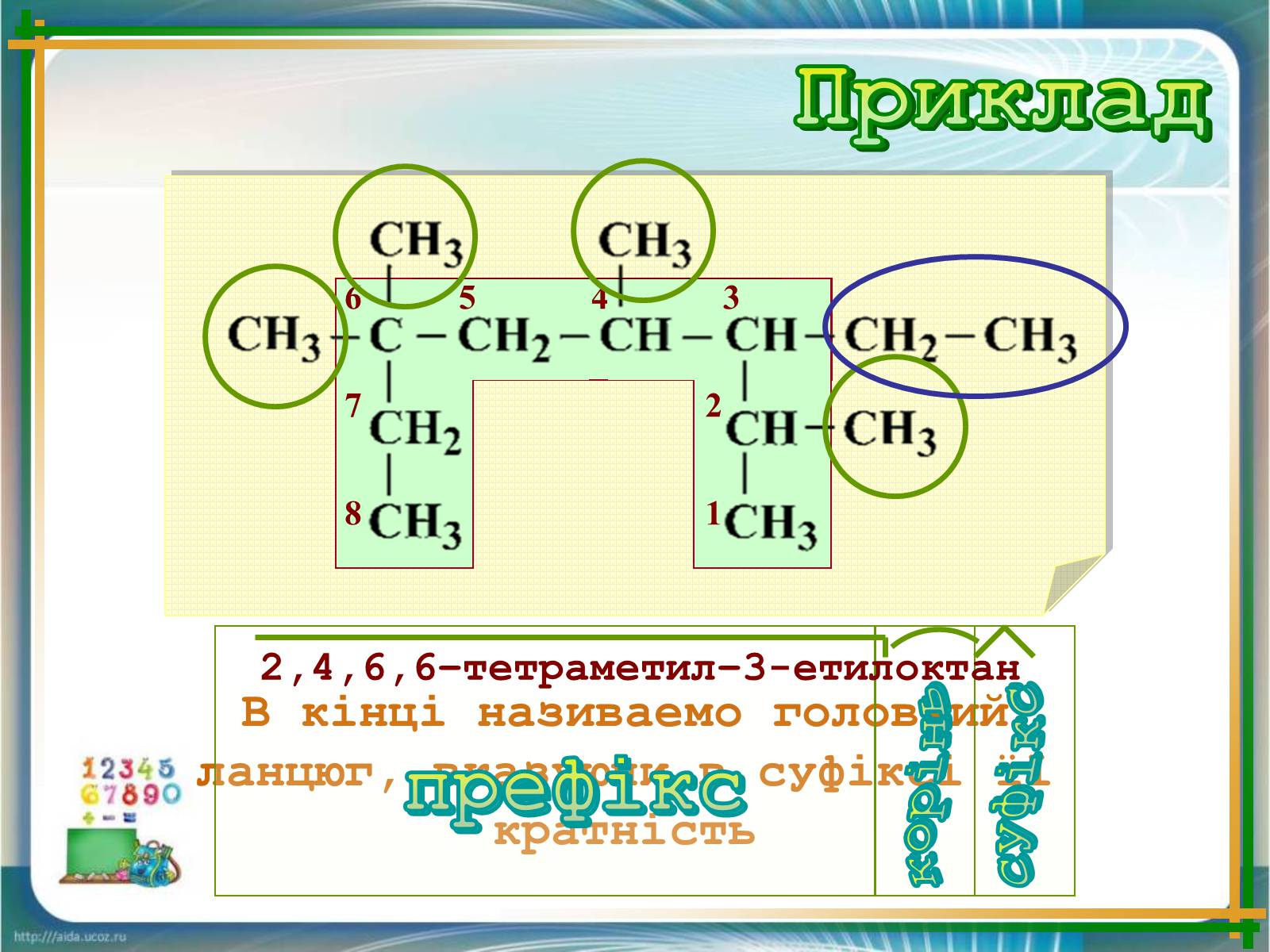
В кінці називаемо головний ланцюг, вказуючи в суфіксі її кратність
префікс
корінь
суфікс
Приклад
6
7
8
5 4 3
2
1
2,4,6,6–тетраметил–3-етилоктан

Назвіть речовину
3,5-диметил-3-етилоктан
С С С С С
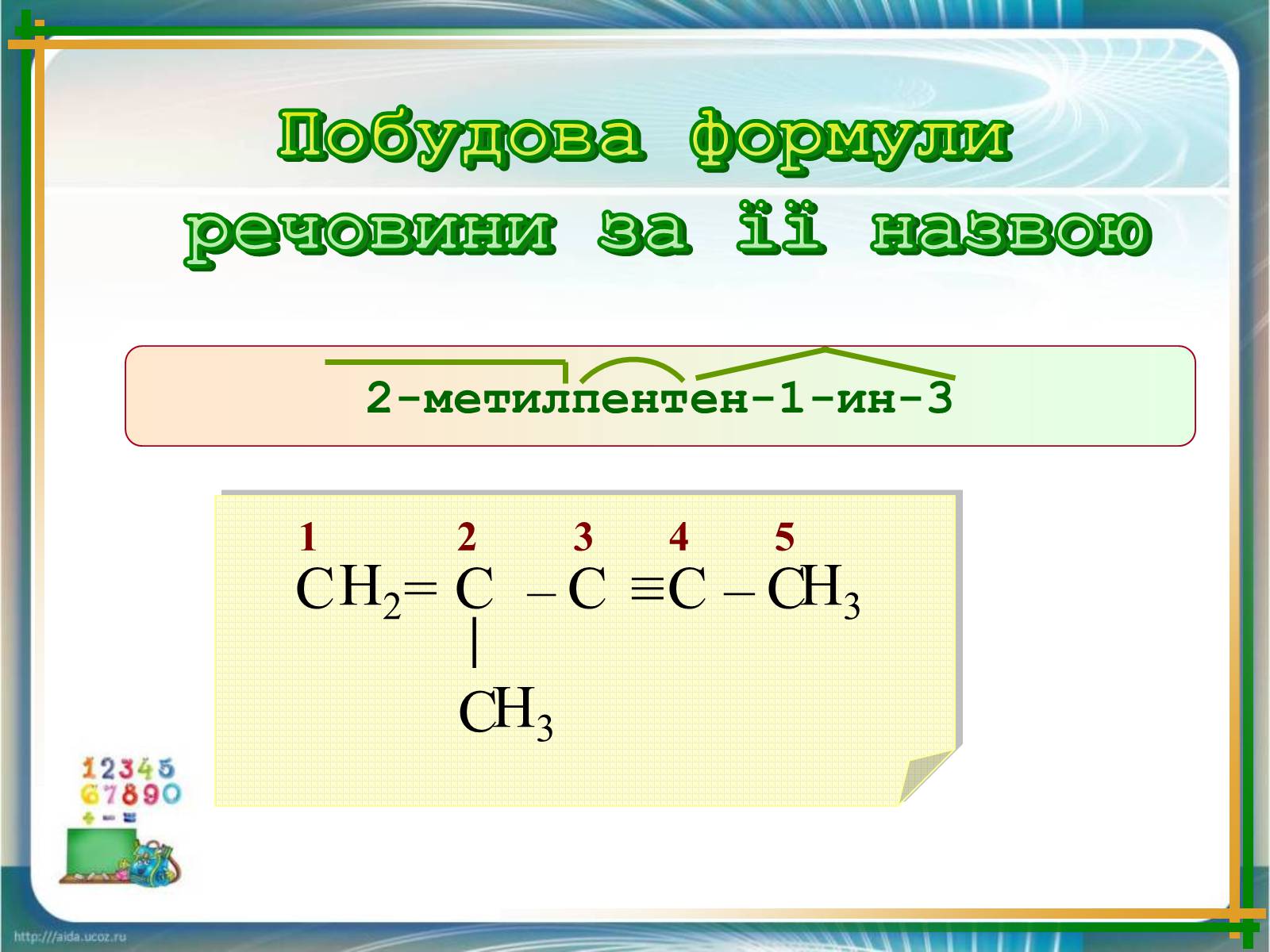
Побудова формули
речовини за її назвою
2-метилпентен-1-ин-3
= – ≡ –
1 2 3 4 5
│
С
Н2 Н3
Н3
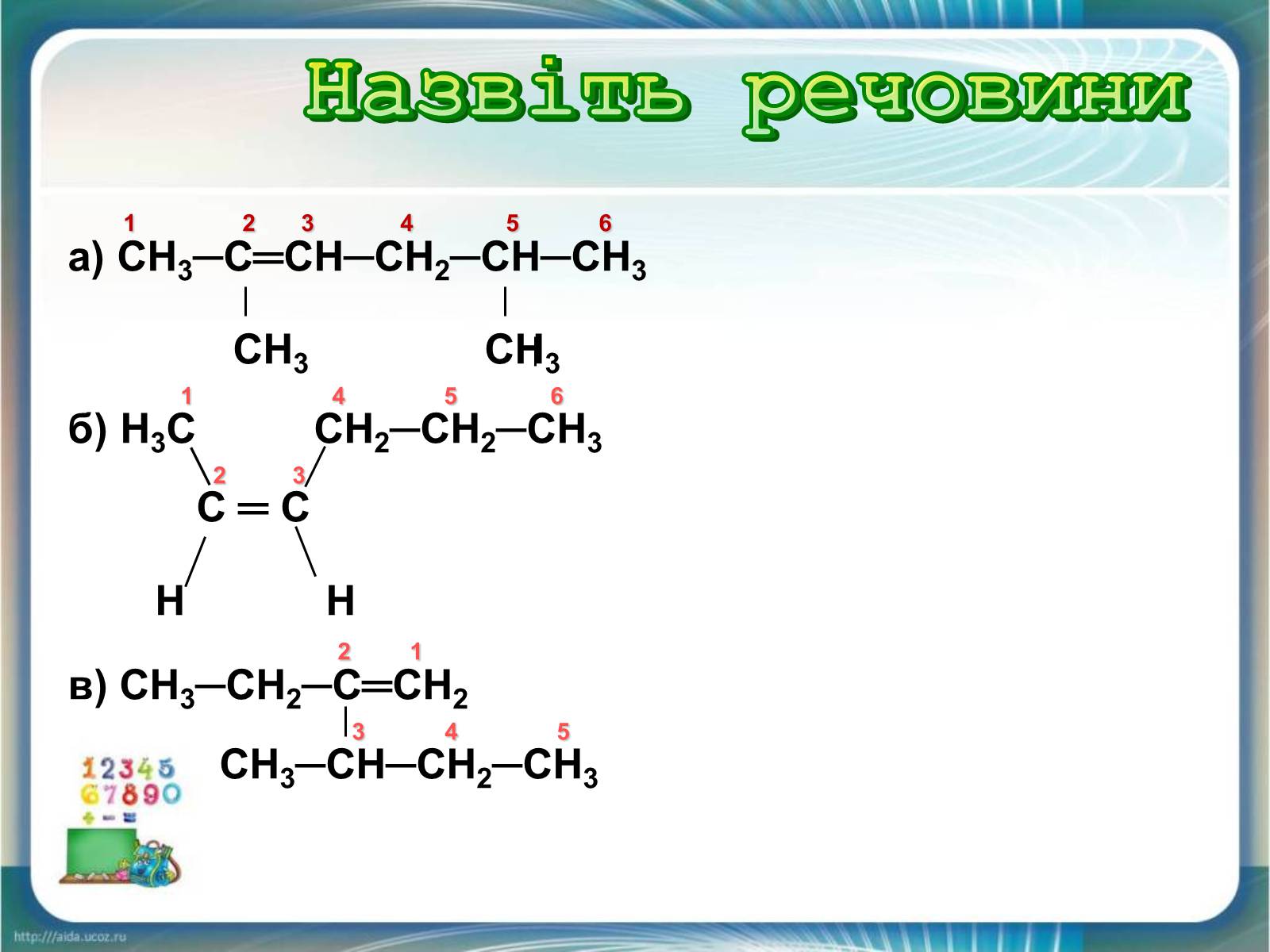
1 2 3 4 5 6
а) СН3─С═СН─СН2─СН─СН3
СН3 СН3
1 4 5 6
б) Н3С СН2─СН2─СН3
2 3
С ═ С
Н Н
2 1
в) СН3─СН2─С═СН2
3 4 5
СН3─СН─СН2─СН3
Назвіть речовини
